
科目: 来源:设计必修一化学鲁科版 鲁科版 题型:058
下图是实验室制备SO2并验证SO2某些性质的装置图.试完成下列问题:

(1)⑥中发生反应的化学方程式为________.
(2)①中的实验现象为________,此实验证明SO2是________气体.
(3)②中的品红溶液________,证明SO2有________性.
(4)③中的实验现象是________,证明SO2有________性.
(5)④中的实验现象是________,证明SO2有________性.
(6)⑤的作用是________,反应方程式为________.
查看答案和解析>>
科目: 来源:设计必修一化学鲁科版 鲁科版 题型:058
回忆实验室制取O2的反应原理和实验装置,完成下列问题:
(1)写出加热NH4Cl和Ca(OH)2制取NH3的反应方程式:________.
(2)按(1)反应原理设计实验室制氨气装置图(可用简笔画表示).
(3)下列气体能用排水法收集的是________(填选项编号;下同),能用排空气法收集的是________.
a.NH3 b.NO c.NO2
查看答案和解析>>
科目: 来源:设计必修一化学鲁科版 鲁科版 题型:058
已知NaHCO3的溶解度很小.在饱和的NH3和NaCl混合溶液中通入CO2,可析出NaHCO3(s):
NaCl+NH3+CO2+H2O![]() NaHCO3↓+NH4Cl
NaHCO3↓+NH4Cl
据此,我国杰出的化学家侯德榜博士设计出了生产纯碱的方法:
这被人们称为侯氏制碱法,打破了帝国主义对我国经济的一种封锁,大长了中国人的民族志气.
试完成下列问题:
(1)写出由NaHCO3制取Na2CO3的化学方程式:________.
(2)如果Na2CO3(s)中混有NaHCO3(s),应如何除去?________(写出方法);如果NaHCO3(aq)中混有Na2CO3(aq),应如何除去?________(写出化学方程式).
(3)某课外活动小组,接受实验室的任务,因Na2CO3制取NaOH,提供的原料只有纯碱和石灰石.请将你的实验方案用流程图表示出来:
![]() ________.
________.
查看答案和解析>>
科目: 来源:设计必修一化学鲁科版 鲁科版 题型:058
甲、乙两个同学都来制取较纯净的碳酸钠溶液,分别设计了下列实验方案:
甲:用如图左所示实验装置,将大理石与稀盐酸反应得到的CO2直接通入氢氧化钠溶液中.
乙:用如图右所示,将氢氧化钠溶液分成两等份,用下列实验装置,再将大理石与稀盐酸反应得到的CO2经饱和碳酸氢钠洗涤后长时间通入其中一份氢氧化钠溶液中,并将所得溶液小心加热煮沸1-2分钟,以赶走溶解在溶液中的过量CO2;再将另一份氢氧化钠溶液与此份溶液混合.哪位同学能获得较纯净的碳酸钠?为什么?

查看答案和解析>>
科目: 来源:设计必修一化学鲁科版 鲁科版 题型:058
自己设计实验完成下列两项内容:①用C还原Fe2O3,②用C还原Al2O3.
(1)画出所设计的实验装置(可用简笔画表示).
(2)很早人类就能冶铁,但铝的冶炼却较晚,是何原因?
查看答案和解析>>
科目: 来源:101网校同步练习 高一化学 山东科学技术出版社 鲁教版 题型:058
某同学探究同周期元素性质的递变规律,并讨论影响化学反应速率的因素.选用的试剂如下:镁条、铝条、铝粉、钠、新制Na2S溶液、新制氯水、0.5 mol·L-1盐酸、3 mol·L-1盐酸、酚酞试液.其设计的实验方案及部分实验现象如下表:

请回答下列问题:
(1)实验③的现象是_____________,该反应的离子方程式为_____________.
(2)由实验③得出的实验结论是________.
(3)由实验②可得出决定化学反应快慢的主要因素是______________________.
(4)实验④中,因为铝粉消失所用的时间短,因此,该同学得出结论:铝比镁易失电子,该结论是否正确?________(填“是”或“否”)
(5)通过实验④说明要加快化学反应速率可________或________.
查看答案和解析>>
科目: 来源:101网校同步练习 高一化学 山东科学技术出版社 鲁教版 题型:058
某兴趣小组设计了如图所示的实验装置,既可用于制取气体,又可用于验证物质的性质.
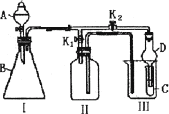
(1)利用Ⅰ、Ⅱ装置可制取收集气体(K2关闭,K1打开)
①下列各组物质中能直接利用这套装置进行实验的是________(填正确选项的标号)
A.锌和稀硫酸
B.双氧水和二氧化锰
C.浓氨水和氧化钙
D.浓盐酸和二氧化锰
②在不改变Ⅰ、Ⅱ装置及位置的前提下,若要制取收集NO气体,可采取的改进方法是装置Ⅱ内充满水;若要制取收集NO2气体,可采取的改进方法是:________.
(2)利用Ⅰ、Ⅲ装置可验证物质的性质(K2打开,K1关闭)
①若要证明氧化性:KMnO4>C12>Br2,则A中加浓盐酸,B中加KMnO4,C中发生的离子反应方程式____________________________________________________________.
②若要证明乙炔为不饱和烃,则I中发生的化学反应方程式为:
_________________________________.
C中的现象为_________________________________.
(3)装置Ⅲ中使用球形干燥管D可防止液体倒吸,其原因是________________.
查看答案和解析>>
科目: 来源:101网校同步练习 高一化学 山东科学技术出版社 鲁教版 题型:058
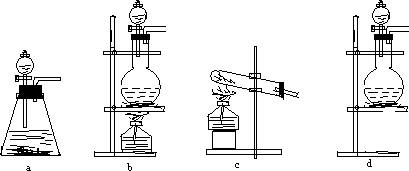
某研究性学习小组查阅资料得知,漂白粉与硫酸溶液反应可制得氯气,化学方程式为:Ca(ClO)2+CaCl2+2H2SO4![]() 2CaSO4+2Cl2↑+2H2O,他们设计如图所示装置制取氯气并验证其性质的实验.
2CaSO4+2Cl2↑+2H2O,他们设计如图所示装置制取氯气并验证其性质的实验.

试回答(1)该实验中A部分的装置是________(填写装置的序号)
(2)请你帮助他们设计一个实验,证明洗气瓶C中的Na2SO3已被氧化(简述实验步骤)______________________.
(3)写出在D装置中发生反应的离子方程式__________________.
(4)该实验存在明显的缺陷,请你提出改进的办法____________.
(5)该小组又进行了如下实验:称取漂白粉2.0 g,研磨后溶解,配制成250 mL溶液,取出25 mL加入到锥形瓶中,再加入过量的KI溶液和过量的H2SO4溶液,静置.待完全反应后,用0.1 mol·L-1 Na2S2O3溶液反应生成的碘,已知反应式为2Na2S2O3+I2=Na2S4O6+2NaI,反应完成时,共消耗Na2S2O3 20 mL.则漂白粉中Ca(ClO)2的质量分数为________________.
查看答案和解析>>
科目: 来源:101网校同步练习 高一化学 山东科学技术出版社 鲁教版 题型:058
在实验室用下图装置制取溴苯,回答:
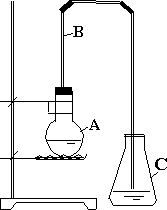
(1)烧瓶A中装有________、________和铁粉,铁粉在反应中是__________________.
(2)未加入铁粉时溴溶于苯不反应,当加入铁粉后观察到A中反应混合物逐渐沸腾,B管中有红棕色的蒸气.C出口附近有白雾.导管B起________和________的作用.导管C不插入水中是因为________________.
(3)反应完毕,向锥形瓶中滴入AgNO3溶液,有________生成;烧瓶A中的液体倒入盛水烧杯中烧杯底部有褐色不溶于水的油状物生成.
(4)纯净的溴苯无色液体,密度大于水.不纯的则显褐色,是由于其中________,可将其用________溶液通过洗涤、________来提纯.
(5)完成该反应的化学方程式:
_________________________________________________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com