
科目: 来源:山东省青州一中2012届高三化学一轮跟踪训练:第3章 第6讲 氯及其化合物(鲁科版) 题型:058
如图是某研究性学习小组设计制取氯气并以氯气为反应物进行特定反应的装置.

(1)要将C装置接入B和D之间,正确的接法是a→________→________→d.
(2)实验开始先点燃A处的酒精灯,打开夹子K,让Cl2充满整个装置,再点燃D处的酒精灯.Cl2通过C装置后进入D,D装置内盛有炭粉,发生氧化还原反应,生成CO2和HCl(g),发生反应的化学方程式为________.
为了使C装置发挥更好的作用,可向烧杯中加入浓硫酸,加入浓硫酸的作用是________.
(3)D处反应完毕后,关闭夹子K,移去两个酒精灯,由于余热的作用,A处仍有少量Cl2产生,此时B中的现象是________,B的作用是________.
(4)用量筒量取20 mL E中溶液,倒入已检查完气密性良好的分液漏斗中,然后再注入10 mL CCl4,盖好玻璃塞(如图),振荡,静置于铁架台上,等分层后取上层液和下层液,呈黄绿色的是________(填“上层液”或“下层液”),再装入如图所示的烧杯中,能使有色布条褪色的是________(填“上层液”或“下层液”).
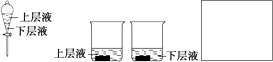
(5)在A、B、C、D、E装置中有一处需要改进,说明需要改进的理由并在方框中画出改进后的装置图________.
查看答案和解析>>
科目: 来源:吉林省长春市2012届高三上学期第一次调研测试化学试题 题型:058
Cu2S是火法炼铜一种重要的原料,下面是由Cu2S冶炼铜及制取CuSO4·5H2O的流程图:
(1)Cu2S中铜元素的化合价为________,火法炼铜的反应原理是________(用化学方程式表示).
(2)Cu2O,CuO加入足量稀硫酸得到的体系A中看到溶液呈蓝色,且有红色物质生成,请写出生成红色物质的离子方程式:________.
(3)若将A中单质反应,操作加入试剂最好是________.
A.加入适量的NaNO3
B.适量的HNO3
C.适量的H2O2
(4)若B溶液的体积为0.2 L,电解B溶液一段时间后溶液的pH值由2变为1(体积变化忽略不计),此时电解过程中转移电子数的物质的量是________.
(5)取5.0 g胆矾样品逐渐升高温度使其分解,分解过程的热重曲线如下图所示:通过计算确定258℃时发生反应的化学方程式________,e点的化学式________(计算过程略去).

查看答案和解析>>
科目: 来源:上海市普陀区2012届高三上学期期末质量抽测化学试题 题型:058
高氯酸铵(NH4ClO4)是复合火箭推进剂的重要成分,实验室可通过下列反应制取:
NaClO4(aq)+NH4Cl(aq)![]() NH4ClO4(aq)+NaCl(aq)
NH4ClO4(aq)+NaCl(aq)
1.用氨气和浓盐酸代替NH4Cl,上述反应不需要外界供热就能进行,其原因是:________.
2.反应得到的混合溶液中NH4ClO4和NaCl的质量分数分别为0.30和0.l5(相关物质的溶解度曲线如下图).从混合溶液中获得较多NH4ClO4晶体的实验操作依次为(填操作名称)蒸发浓缩,________,过滤,________、干燥.
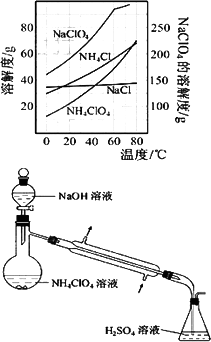
为了测定样品中NH4ClO4的含量,装置如上图所示(加热装置、仪器固定装置已略去),实验步骤如下:
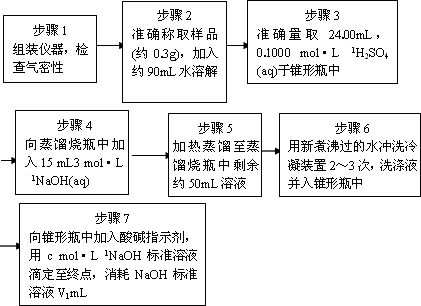
3.步骤3中,准确取用24.00 mL H2SO4(aq)的玻璃仪器是________.
4.实验中确保生成的氨被稀硫酸完全吸收的实验步骤是________(填写步骤编号).
5.必须重复实验2~3次,其原因是________.
6.如果0.320 g试样中含NH4ClO4的准确值为0.095 g,而实验测定结果是0.092 g.该实验的相对误差为________.
查看答案和解析>>
科目: 来源:福建省厦门六中2010-2011学年高一下学期期中考试化学试题 题型:058
[探究实验一]:某同学探究同周期主族元素性质递变规律时,自己设计了一套实验方案,并记录了有关实验现象(见下表,表中的“实验方案”与“实验现象”前后不一定是对应关系):
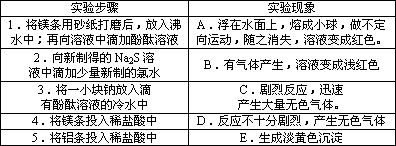
请你帮助该同学整理并完成实验报告.
(1)实验目的:探究同周期主族元素性质递变规律.
(2)实验用品:试剂:金属钠,镁条,铝条,稀盐酸,新制氯水,新制Na2S溶液.仪器:①________,②________,③________,试管夹,镊子,小刀,玻璃片,砂纸,酒精灯等.
(3)实验内容:(填写与实验步骤对应的实验现象的编号和离子方程式)
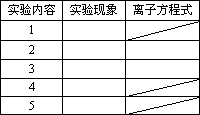
(4)若用最高价氧化物的水化物的碱性相对强弱来验证Mg、Al失电子能力的
强弱,请你设计实验(实验用品自选,不要求写化学方程式):________;
(5)实验结论:________;
[探究实验二]:一定条件下,氯化镁与四氯化钛的混合物可作烯烃聚合反应的催化剂.为了探究温度、氯化镁固体的含水量以及粉碎方式对该催化剂催化效果的影响,设计如下对比实验:
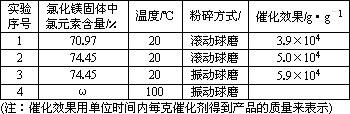
(6)表中ω=________;
(7)从实验1、2可以得出的结论是:________;
(8)设计实验2、3的目的是:________.
查看答案和解析>>
科目: 来源:海南省嘉积中学2010-2011学年高二教学质量监测化学理科试题(二) 题型:058
某同学用标准NaOH溶液来测定未知浓度的盐酸的浓度:
(1)配制250 mL 0.5 mol/L的NaOH溶液所需的玻璃仪器为________.
(2)用滴定管准确量取20.00 mL未知浓度的盐酸于锥形瓶中,加入酚酞作指示剂,用NaOH溶液滴定到终点.
该同学进行了三次实验,实验数据如下表:

滴定中误差较大的是第________次实验,造成这种误差的可能原因是________(填选项编号)
a、在盛装未知浓度的盐酸之前锥形瓶里面有少量蒸馏水,未烘干
b、滴定管在盛装标准NaOH溶液前未润洗
c、滴定开始前盛装标准NaOH溶液的滴定管尖嘴部分有气泡,滴定终点读数时未发现气泡
d、滴定开始前盛装标准NaOH溶液的滴定管尖嘴部分没有气泡,在滴定终点读数时发现尖嘴部分有气泡
e、滴定过程中,锥形瓶摇荡得太剧烈,以致有些液滴飞溅出来
f、达到滴定终点时,俯视溶液凹液面最低点读数
g、滴定到终点时,溶液颜色由无色变到了红色
(3)该同学所测得盐酸的物质的量浓度为________(结果保留三位小数).
查看答案和解析>>
科目: 来源:新疆乌鲁木齐一中2010-2011学年高一上学期期末考试化学试题 题型:058
工业生产的纯碱常含有少量的NaCl等杂质.下图是测定产品中Na2CO3质量分数的实验装置.操作步骤有:

A.在干燥管内填满碱石灰,质量为mg
B.取ng样品装入广口瓶中
C.检查装置气密性
D.关闭止水夹
E.打开止水夹
F.缓慢鼓入空气数分钟,再称干燥管质量为Wg
G.缓慢加入稀硫酸至不再产生气体为止
H.缓缓鼓入空气数分钟
(1)正确的操作顺序是(填符号):C→________→E→________→D→________→G→________→F
(2)步骤F中,要缓缓鼓入空气数分钟,鼓入空气的目的是________,装置甲的作用是________,装置乙的作用是________.
(3)计算溶液中Na2CO3的质量分数的计算式是________.
(4)若去掉装置甲,测定结果会________,若去掉装置乙,测定结果会________.(填“偏大”、“偏小”或“无影响”)
查看答案和解析>>
科目: 来源:新疆乌鲁木齐一中2010-2011学年高一上学期期末考试化学试题 题型:058
(1)浓硫酸与木炭粉在加热条件下反应的化学方程式是:________.
(2)试用下图所列各装置设计一个实验,来验证上述反应所产生的各种产物.

这些装置的连接顺序(按产物气流从左至右的方向)是(填装置的编号):________→________→________→________.
(3)实验时可观察到装置①中A瓶的溶液褪色,C瓶的溶液不褪色.A瓶溶液的作用是________,B瓶溶液的作用是________,C瓶溶液的作用是________.
(4)装置②中所加固体药品是________,可验证的产物是________,确定装置②在整套装置中位置的理由是________.
(5)装置③中所盛溶液是________,可验证的产物是________.
查看答案和解析>>
科目: 来源:辽宁省沈阳二中2011届高三第四次阶段测试化学试题 题型:058
甲醇被称为21世纪的新型燃料,工业上用CH4和H2O为原料通过下列反应①和②,来制备甲醇.
①CH4(g)+H2O(g)![]() CO(g)+3H2(g) ΔH1
CO(g)+3H2(g) ΔH1
②CO(g)+2H2(g)![]() CH3OH(g) ΔH2
CH3OH(g) ΔH2
将0.20 mol CH4和0.30 mol H2O(g)通入容积为10 L的密闭容器中,在一定条件下发生反应①,达到平衡时,CH4的转化率与温度、压强的关系如下图.

(1)温度不变,缩小体积,①的逆反应速率________(填“增大”、“减小”或“不变”)
(2)反应①的ΔH1________0(填“<”“=”或“>”)100℃时的平衡常数值K=________.
(3)在压强为0.1 Mpa条件下,将a mol CO与3a mol H2的混合气体在催化剂作用下进行反应②再生成甲醇.为了发寻找合成甲醇的适宜的温度和压强,某同学设计了二组实验,部分实验条件已经填在下面实验设计表中.请在空格中填入剩余的实验条件数据.
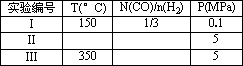
300℃时,其他条件不变,将容器的容积压缩到原来的1/2,对平衡体系产生的影响是________(填字母)
A.c(H2)减少
B.正反应速率加快,逆反应速率减慢
C.CH3OH的物质的量增加
D.重新平衡时c(H2)/c(CH2OH)减小
(4)已知在常温常压下:
①2CH2OH(l)+3O2(g)=2CO2(g)+4H2O(g)ΔH=-1275.6 kJ/mol
②2CO(g)+O2(g)=2CO2(g)ΔH=-556.0 kJ/mol
③H2O(g)=H2O(l)ΔH=-44.0 kJ/mol
写出甲醇不完全燃烧生成一氧化碳的液态水的热化学方程式________.
(5)某实验小组依据甲醇燃烧的反应原理,设计如下图所示的电池装置.

①该电池正极的电极反应为________.
②工作一段时间后,测得溶液的pH减小,该电池总反应的化学方程式为
________.
查看答案和解析>>
科目: 来源:辽宁省锦州市2010-2011学年度高二第一学期期末考试化学试题 题型:058
如图所示,甲、乙两池电极材料都是铁棒和碳棒,

请回答下列问题:
(1)若两池中均为CuSO4溶液,反应一段时间后:
①有红色物质析出的是甲池中的________棒,乙池中的________棒.
②乙池中阳极的电极反应式是________.
(2)若两池中均为饱和NaCl溶液:
①写出乙池中总反应的离子方程式________.
②甲池中碳极上电极反应式是________,乙池碳极上电极反应属于________(填“氧化反应”或“还原反应”).
③将湿润的KI淀粉试纸放在乙池碳极附近,发现试纸变蓝,反应的化学方程式为________.
④若乙池转移0.02 mol e-后停止实验,池中溶液体积是200 mL,则溶液混合均匀后的PH=________.
查看答案和解析>>
科目: 来源:黑龙江“五校联谊”2010-2011学年高一上学期期末考试化学理科试题 题型:058
Fe(OH)2很不稳定,露置在空气中容易被氧化,Fe(OH)2被氧化的化学方程为:________.为了获得白色的Fe(OH)2沉淀,可以用不含Fe3+的FeSO4溶液与用不含O2的蒸馏水配制的NaOH溶液反应制备.
(1)用硫酸亚铁晶体配制上述FeSO4溶液时你觉得还需加入________.
(2)除去蒸馏水中溶解的O2常采用________的方法.
(3)生成白色Fe(OH)2沉淀的操作是用长滴管吸取不含O2的NaOH溶液,插入FeSO4
溶液液面下,再挤出NaOH溶液,这样操作的理由是________.
(4)检验Fe3+存在的最佳试剂是________,现象是________.
(5)写出Fe与
H2O在一定条件下反应的化学方程式________.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com