
科目: 来源:物理教研室 题型:013
现有如下各说法:
①在水中氢、氧原子间均以化学键相结合.
②金属和非金属化合形成离子键.
③离子键是阳离子、阴离子的相互吸引.
④根据电离方程式: ,判断HCl分子里存在离子键.
,判断HCl分子里存在离子键.
⑤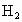 分子和
分子和 分子的反应过程是
分子的反应过程是 分子里共价键发生断裂生成H、Cl原子,而后H、Cl原子形成离子键的过程.
分子里共价键发生断裂生成H、Cl原子,而后H、Cl原子形成离子键的过程.
上述各种说法正确的是
[ ]
查看答案和解析>>
科目: 来源:物理教研室 题型:013
某元素X的原子核外电子数等于核内中子数,取该元素的单质2.8g跟氧气充分作用,可得到6.0g化合物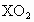 ,该元素在周期表中的位置是
,该元素在周期表中的位置是
[ ]
查看答案和解析>>
科目: 来源:物理教研室 题型:013
下列对元素的叙述中,可肯定是主族元素的是
[ ]
A.最高价氧化物的水化物是酸的元素
B.原子核外电子排布中次外层为18个电子的元素
C.最高正化合价为+7的元素
D.原子核外电子排布中最外层为5个电子的元素
查看答案和解析>>
科目: 来源:物理教研室 题型:013
镭是元素周期表中第七周期ⅡA族元素,下列关于镭的叙述中不正确的是
[ ]
查看答案和解析>>
科目: 来源:物理教研室 题型:013
下列关于元素周期律和元素周期表的叙述中正确的是
[ ]
A.同一主族的元素,从上到下单质熔点逐渐升高
B.同一周期的元素,从左到右元素的原子半径逐渐增大
C.周期表中ⅣA~ⅦA族,元素均可表现正化合价
D.同一周期的元素,从左到右其最高价氧化物的水化物的碱性逐渐减弱而酸性逐渐增强
查看答案和解析>>
科目: 来源:物理教研室 题型:013
X、Y、Z三种主族元素,如果 与
与 具有相同的电子层结构,
具有相同的电子层结构, 的半径大于
的半径大于 的半径,则三种元素的原子序数由大到小的顺序是
的半径,则三种元素的原子序数由大到小的顺序是
[ ]
查看答案和解析>>
科目: 来源:物理教研室 题型:013
根据中学化学教材所附元素周期表判断,下列叙述不正确的是
[ ]
A.K层电子为奇数的所有元素所在族的序数与该元素原子的K层电子数相等
B.L层电子为奇数的所有元素所在族的序数与该元素原子的L层电子数相等
C.L层电子为偶数的所有主族元素所在族的序数与该元素原子的L层电子数相等
D.M层电子为奇数的所有主族元素所在族的序数与该元素原子的M层电子数相等
查看答案和解析>>
科目: 来源:物理教研室 题型:013
下列说法正确的是
[ ]
A.常温常压下,只有一种元素的单质呈液态
B.周期表中所有元素都是从自然界中发现的
C.过渡元素不全是金属元素
D.常温常压下,气态单质的分子都是由非金属元素的原子形成的
查看答案和解析>>
科目: 来源:物理教研室 题型:013
下表为元素周期表前四周期的一部分,下列有关R、W、X、Y、Z五种元素的叙述中,正确的是
[ ]

A.常压下五种元素的单质中Z单质的沸点最高
B.Y、Z的阴离子电子层结构都与R原子的相同
C.W的氢化物的沸点比X的氢化物的沸点高
D.Y元素的非金属性比W元素的非金属性强
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com