
科目: 来源:物理教研室 题型:021
下列叙述中,可以说明金属甲的活泼性比金属乙的活泼性强的是
[ ]
A.在氧化还原反应中,甲原子失去的电子比乙原子失去的电子多
B.同价态的阳离子,甲比乙的氧化性强
C.甲能,跟稀盐酸反应放出氢气而乙不能
D.将甲、乙作电极组成原电池时,甲是负极
查看答案和解析>>
科目: 来源:物理教研室 题型:021
据报道,美国正在研究的锌电池可能取代目前广泛使用的铅蓄电池,它具有容量大等优点,其电池反应为![]() ,其原料为锌、电解液和空气,则下列叙述正确的是
,其原料为锌、电解液和空气,则下列叙述正确的是
[ ]
A.锌为正极,空气进入负极反应
B.负极反应为
C.正极发生氧化反应
D.电解液肯定不是强酸
查看答案和解析>>
科目: 来源:物理教研室 题型:021
以锌片和铜片为两极,以稀硫酸为电解质溶液组成原电池,当导线中通过2mol电子时,下列说法正确的是
[ ]
A.锌片溶解了1mol,铜片上析出1mol氢气
B.两极上溶解和析出的物质质量相等
C.锌片溶解了1g,铜片上析出1g氢气
D.锌片溶解了lmol,硫酸消耗了lmol
查看答案和解析>>
科目: 来源:物理教研室 题型:021
有4种金属a、b、c、d.,当它们两两组成原电池时,金属a都是正极;在这4种金属组成的混合物中,加入足量的盐酸,可使金属b和c溶解;过滤后,在滤液中加入过量NaOH溶液,得到c离子形成的沉淀.由此可知这4种金属的活动性由强到弱的正确顺序可能是下列中的
[ ]
查看答案和解析>>
科目: 来源:物理教研室 题型:021
下列说法正确的是
[ ]
A.钢铁因含杂质而容易发生电化腐蚀,所以合金都不耐腐蚀
B.原电池反应是导致金属腐蚀的主要原因,故不能用来减缓金属的腐蚀
C.钢铁电化腐蚀的两种类型主要区别在于水膜的pH不同,引起的正极反应不同
D.无论哪种类型的腐蚀,其实质都是金属被氧化
查看答案和解析>>
科目: 来源:物理教研室 题型:021
对于mA(g)+nB(g)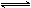 pC(g)+qD(g)的平衡体系,当升高温度时,体系的平均密度对H2的相对密度从16.5变为16.9,则下列说法正确的是
pC(g)+qD(g)的平衡体系,当升高温度时,体系的平均密度对H2的相对密度从16.5变为16.9,则下列说法正确的是
[ ]
Am+n>p+q,正反应是放热反应
B.m+n>p+q,正反应是吸热反应
Cm+n<p+q,逆反应是放热反应
D.m+n<p+q,逆反应是吸热反应
查看答案和解析>>
科目: 来源:物理教研室 题型:021
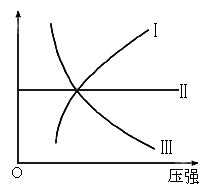
图Ⅰ、Ⅱ、Ⅲ分别代表反应①③、②、④,则y轴是指
[ ]
①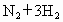
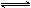
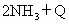
②
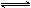 2HI+Q
2HI+Q
③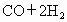
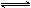
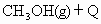
④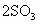
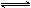
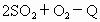
A.平衡混合气中一种生成物的百分含量
B.平衡混合气中一种反应物的百分含量
C.平衡混合气中一种生成物的转化率
D.平衡混合气中一种反应物的转化率
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com