
科目: 来源:学习高手选修化学(反应原理人教版) 人教版 题型:021
|
在容积相同的A、B两个密闭容器中,分别充入2 mol SO2和1 mol O2,使它们在相同的温度下发生反应:2SO2+O2 | |
A. |
25% |
B. |
>25% |
C. |
<25% |
D. |
12.5% |
查看答案和解析>>
科目: 来源:选修高手化学苏教·化学反应原理 苏教版 题型:021
|
当反应L(s)+aG(g)
| |
A. |
上述反应是放热反应 |
B. |
上述反应是吸热反应 |
C. |
a>b |
D. |
d<b |
查看答案和解析>>
科目: 来源:选修高手化学苏教·化学反应原理 苏教版 题型:021
|
在容积固定的密闭容器中存在如下反应: A(g)+3B(g) 某研究学习小组研究了其他条件不变时,改变某一条件对上述反应的影响,并根据实验数据作出下列关系图:
下列判断一定错误的是 | |
A. |
图Ⅰ研究的是不同催化剂对反应的影响,且乙使用的催化剂效率较高 |
B. |
图Ⅱ研究的是压强对反应的影响,且甲的压强较大 |
C. |
图Ⅱ研究的是温度对反应的影响,且甲的温度较高 |
D. |
图Ⅲ研究的是不同催化剂对反应的影响,且甲使用的催化剂效率较高 |
查看答案和解析>>
科目: 来源:浙江省兰溪一中2010-2011学年高二下学期期中考试化学试题 题型:021
|
某温度时,AgCl在水中的沉淀溶解平衡曲线如图所示(提示:AgCl(s) Ksp(AgCl)=1 .8×10-10,Ksp(Ag2S)=6.3×10-50).下列说法正确的是:
| |
A. |
加入NaCl可以使溶液由a点变到b点 |
B. |
b点和d点均无AgCl沉淀生成 |
C. |
a点对应的Ksp大于c点对应的Ksp |
D. |
向0 .1 mol/L的硝酸银溶液中滴加0.1 mol/L的NaCl溶液至不再有白色沉淀生成,再向其中滴加0.1 mol/L的Na2S溶液,白色沉淀转化为黑色沉淀.其沉淀转化的反应方程式为:2AgCl(s)+S2-(aq)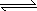 Ag2S(s)+2Cl-(aq). Ag2S(s)+2Cl-(aq).
|
查看答案和解析>>
科目: 来源:湖南省嘉禾一中2011届高三1月高考押题卷化学试题 题型:021
|
已知同温度下的溶解度:Zn(OH)2>ZnS,MgCO3>Mg(OH)2;就溶解或电离出S2-的能力而言,FeS>H2S>CuS,则下列离子方程式错误的是 | |
A. |
Mg2++2HCO3-+2Ca2++4OH- |
B. |
Cu2+ +H2S |
C. |
Zn2++S2-+2H2O |
D. |
FeS +2H+ |
查看答案和解析>>
科目: 来源:高中化学新课标鲁科版 必修Ⅱ 鲁科版 题型:021
| |||||||||||||||||||||||||||||||||||||||
查看答案和解析>>
科目: 来源:导学大课堂必修二化学人教版 人教版 题型:021
|
已知乙烯分子是平面结构,乙炔分子是直线型结构,由此推断对CH3-CH | |
A. |
6个碳原子有可能都在一条直线上 |
B. |
6个碳原子不可能在一条直线上 |
C. |
6个碳原子有可能在同一平面上 |
D. |
6个碳原子不可能都在同一平面上 |
查看答案和解析>>
科目: 来源:导学大课堂必修二化学人教版 人教版 题型:021
|
巴豆酸的结构式为CH3-CH ②溴水 ③纯碱溶液 ④丁醇 ⑤酸性KMnO4溶液,试根据其结构特点判断在一定条件下能与巴豆酸反应的物质的组合是 | |
A. |
②④⑤ |
B. |
①③④ |
C. |
①②③④ |
D. |
①②③④⑤ |
查看答案和解析>>
科目: 来源:导学大课堂必修二化学人教版 人教版 题型:021
|
有A、B、C、D四块金属片,用导线两两相连插入稀硫酸中,可以组成各种原电池.若A与B相连时,A为负极;C与D相连时,C溶解,D上有氢气生成;A与C相连时,C为正极;B与D相连时,电子由D极经导线流向B极,则这四种金属的活泼性由强到弱的顺序为 | |
A. |
ABCD |
B. |
ACDB |
C. |
CADB |
D. |
BDCA |
查看答案和解析>>
科目: 来源:导学大课堂必修二化学人教版 人教版 题型:021
|
日常所用干电池的电极分别为碳棒(上面有铜帽)和锌皮,以糊状NH4Cl和ZnCl2作电解质(其中加入MnO2吸收H2),电极反应式可简化为Zn→Zn2++2e-,2 | |
A. |
Zn为正极,碳为负极 |
B. |
Zn为负极,碳为正极 |
C. |
工作时,电子由碳极经过电路流向Zn极 |
D. |
长时间连续使用时,内装糊状物可能流出腐蚀用电器 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com