
科目: 来源: 题型:022
短周期的三种元素X、Y、Z,原子序数依次变小,原子核外电子层数之和是5。X元素原子最外电子层上的电子数是Y和Z两元素原子最外电子层上的电子数的总和;Y元素原子的最外电子层上的电子数是它的电子层数的2倍,X和Z可以形成XZ3的化合物。请回答:
(1)X元素的名称是________;Y元素的名称是________;Z元素的名称是:________。
(2)XZ3化合物的化学式是________,电子式是________。
(3)分别写出X、Y的含氧酸的化学式________、________。
查看答案和解析>>
科目: 来源: 题型:022
下面是元素周期表的一部分:
|
族 周期 |
ⅠA |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
|
1 |
① |
|
|||||
|
2 |
② |
③ |
④ |
|
⑤ |
⑥ |
|
|
3 |
|
⑦ |
⑧ |
|
|
⑨ |
⑩ |
(1)表中元素⑩的氢化物的化学式为________,此氢化物的还原性比元素⑨的氢化物的还原性________(填强或弱)。(2)某元素原子的校外p电子数比s电子数少1,则该元素的元素符号是________,其单质的电子式为________。(3)俗称为“矾”的一类化合物通常含有共同的元素是________。(4)已知某些不同族元素的性质也有一定的相似性,如元素③与元素⑧的氢氧化物有相似的性质。写出元素③的氢氧化物与NaOH溶液反应的化学方程式________,又如表中与元素⑦的性质相似的不同族元素是________(填元素符号)。
查看答案和解析>>
科目: 来源: 题型:022
第三周期元素A、B、C、D、E、F的原子序数依次递增。 A、C、F三种元素原子的最外层电子数之和为11,这三种元素的最高价氧化物对应的水化物之间两两反应生成盐和水,D元素原子的最外层电子数比次外层电子数少4,E元素原子的次外层电子数比最外层电子数多3。回答下列问题:
(1)用电子式表示B的氧化物和D的氢化物的形成过程:________,________
(2)写出C的最高价氧化物对应的水化物与F的最高价氧化物对应的水化物反应的化学方程式________,与A的最高价氧化物对应的水化物反应的离子方程式________
查看答案和解析>>
科目: 来源: 题型:022
下表是元素周期表的一部分,回答下列有关问题:
|
族周期 |
ⅠA |
ⅡA |
ⅢA |
ⅣVA |
ⅤA |
ⅥA |
ⅦA |
O |
|
2 |
|
|
|
|
① |
|
② |
|
|
3 |
③ |
④ |
⑤ |
⑥ |
|
⑦ |
⑧ |
⑨ |
|
4 |
⑩ |
11 |
|
|
|
|
12 |
|
(1)写出下列元素符号:①________,⑥_______,⑦________,11________.
(2)在这些元素中,最活泼的金属元素是________,最活泼的非金属元素是________,最不活泼的元素是________.
(3)在这些元素的最高价氧化物对应水化物中,酸性最强的是________,碱性最强的是________,呈两性的氢氧化物是________,写出三者之间相互反应的化学方程式.
(4)在这些元素中,原子半径最小的是________,原子半径最大的是________.
(5)在③与④中,化学性质较活泼的是________,怎样用化学实验证明?答:________.在⑧与12中,化学性质较活泼的是________,怎样用化学实验证明?答:________.
查看答案和解析>>
科目: 来源:江苏省建陵中学2006-2007学年度第一学期期中高二年级调研测试、化学(选修) 题型:022
以下列出的是一些原子的2p能级和3d能级中电子排布的情况.试判断,哪些违反了泡利不相容原理,哪些违反了洪特规则.



违反泡利不相容原理的有________,违反洪特规则的有________.
查看答案和解析>>
科目: 来源:江苏省建陵中学2006-2007学年度第一学期期中高二年级调研测试、化学(选修) 题型:022
某元素的原子获得能量后的电子排布式为1s2 2s22p6 3s23p3 4s1,则该元素的原子获得能量前的电子排布式为________;元素符号为________;其最高价氧化物对应的水化物的化学式是________.
查看答案和解析>>
科目: 来源:江苏省建陵中学2006-2007学年度第一学期期中高二年级调研测试、化学(选修) 题型:022
下面是s能级和p能级的原子轨道图,试回答问题:

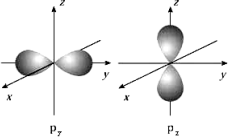
s电子的原子轨道呈________形,每个s能级有________个原子轨道;p电子的原子轨道呈________形,每个p能级有________个原子轨道.
查看答案和解析>>
科目: 来源:淮阴师院附中2006~2007学年度高二第一学期期中考试 化学试卷(文科) 题型:022
氨基酸是具有两性特点的有机物,在结构上都具有的官能团名称是________、________.我们从食物中摄取的________在胃液中的胃蛋白酶和胰蛋白酶的作用下发生________反应,生成氨基酸,它被人体吸收后,重新合成人体所需要的各种________.
查看答案和解析>>
科目: 来源:淮阴师院附中2006~2007学年度高二第一学期期中考试 化学试卷(文科) 题型:022
链状结构的塑料具有________性,而多数网状结构的塑料一经加工成型就不会受热熔化,因而具有________性.聚乙烯塑料的单体为________(写结构简式),它属于________塑料
查看答案和解析>>
科目: 来源:广东省2006年高一化学期中考试卷 题型:022
如右图所示,把试管放入盛有饱和澄清石灰水的烧杯中(温度为25℃),试管中放有几块镁片,向试管中滴入5 ml盐酸.
试回答下列问题:

⑴实验中观察到的现象有_________________________________________
⑵产生上述现象的原因是_________________________________________
⑶有关反应的离子方程式是_______________________________________
⑷由实验推知,MgCl2溶液和H2的总能量__________________________(填“大于”“小于”或“等于”)镁片和盐酸的总能量.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com