
科目: 来源: 题型:022
银器皿日久表面逐渐变黑色,这主要是由于生成硫化银.有人设计用原电池原理进行抛光,其处理方法为:将一定浓度的食盐溶液放入一铝制容器中,再将变黑的银器浸入溶液中,放置一段时间后,黑色会褪去而银恢复光泽,且不会损失.试回答:
(1)食盐的作用是________________.
(2)在此原电池反应中,负极发生的电极反应为________________,正极发生的反应为________________.
(3)反应过程中产生臭鸡蛋气味的气体,溶液中发生的反应为________________.
(4)实验操作中配置食盐水时,通常还加入一定量的小苏打,其主要作用是________________.
(5)原电池总反应方程式为________________________.
查看答案和解析>>
科目: 来源: 题型:022
实验室分析白口铁(镀锌铁皮)样品成分的步骤为:①称取1.00g样品放入烧杯中,加入过量盐酸,然后用玻璃片盖好烧杯.首先观察到有大量气体冒出,后来放出气体速率变慢,最后完全反应.
②接着加入过量的NaOH溶液,过滤分离出灰绿色沉淀;该沉淀在空气中加热至质量不变;最后得到1.20g红色粉末.试回答:
(1)白口铁镀锌的作用是________________;
(2)盖玻璃片的作用是________________;
(3)放出气体速率由快到慢的原因是
_____________________________________________________________;
(4)加入过量NaOH溶液的理由是
_____________________________________________________________;
(5)在空气中加热灰绿色沉淀的化学方程式是
_____________________________________________________________;
(6)锌在样品中的质量分数是________________.
查看答案和解析>>
科目: 来源: 题型:022
(2002·杭州)烧过菜的铁锅未及时洗净(残液中含NaCl),第二天便出现红棕色锈斑(主要成分为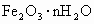 ).试用有关的电极反应式、离子方程式和化学方程式表示锈斑的生成.
).试用有关的电极反应式、离子方程式和化学方程式表示锈斑的生成.
(1)负极:________________.(2)正极:________________.
(3)离子方程式:________________.
(4)总的化学方程式:________________.
查看答案和解析>>
科目: 来源: 题型:022
银器皿用久表面逐渐变黑,这是由于生成硫化银.有人设计原电池加以除去,其处理方法为:将一定浓度的食盐溶液放入一铝制容器中,再将变黑的银器浸入溶液中,放置一段时间后,黑色会褪去而银不会损失.试回答在此原电池反应中,负极发生的反应为________________;正极
发生的反应为________________;反应过程中产生臭鸡蛋气味的气体,原电池的总反应方程式为________________.
查看答案和解析>>
科目: 来源: 题型:022
(2000·全国)测量一定质量的铝锌合金与强酸溶液反应产生的氢气的体积,可以求得合金中铝和锌的质量分数.现有下列实验用品:中学化学实验常用仪器、800mL烧杯、100mL量筒、短颈玻璃漏斗、铜网、铝锌合金样品、浓盐酸(密度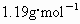 )、水.按图所示装置进行实验,回答下列问题.(设合金样品全部反应,产生的气体不超过100mL)
)、水.按图所示装置进行实验,回答下列问题.(设合金样品全部反应,产生的气体不超过100mL)
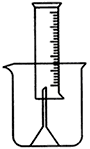
(1)补充下列实验步骤,直到反应开始进行(铁架台和铁夹安装可省略):
①将称量后的合金样品用铜网小心包裹好,放在800mL烧杯底部,把短颈漏斗倒扣在样品上面.
_______________________________________________________.
(2)合金样品用铜网包裹的目的是_______________________.
查看答案和解析>>
科目: 来源: 题型:022
(2003·上海)已知A、B、C三种元素均为短周期元素,它们的原子序数关系为:C>B>A.A元素原子的最外层电子数是次外层电子数的2倍,B和C可形成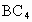 型化合物.用化学符号填空:
型化合物.用化学符号填空:
(1)三种元素中A是________、B是________、C是________.
(2)A、B、C的最高价氧化物的对应水化物分别是________、________、________,在这些水化物中,酸性最弱的是________.
(3)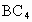 的电子式是________.
的电子式是________.
(4)已知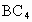 不能在空气中燃烧,理由是________.
不能在空气中燃烧,理由是________.
(5)用离子方程式表示出用B的氧化物制得B的氧化物的对应水化物的原理.
查看答案和解析>>
科目: 来源: 题型:022
(2004·长沙)某铝合金中含有合金元素镁、铜、硅,为了测定该合金中铝的含量,设计了如下实验,请回答有关问题:
(1)称取样品a g,称量时应该使用的主要仪器的名称是________.
(2)将样品溶解于足量的稀盐酸,过滤.滤液中主要含有________,滤渣中含有________,溶解、过滤用到的玻璃仪器是________.
(3)滤液中加过量NaOH溶液、过滤.有关的离子方程式是____________.
(4)步骤(3)的滤液中通入足量 气体,可产生沉淀,过滤.有关的离子方程式是________________.
气体,可产生沉淀,过滤.有关的离子方程式是________________.
(5)步骤(4)过滤后的滤渣用蒸馏水洗涤数次,烘干并灼烧至恒重,冷却后称量,其质量为bg,原样品中铝的质量分数为________.
(6)若步骤(3)中加入NaOH的量不足,则实验结果偏________(填“高”“低”或“无影响”,下同);若步骤(5)中滤渣没有洗涤,则实验结果偏________.
查看答案和解析>>
科目: 来源: 题型:022
某铝合金(硬铝)中含有镁、铜、硅,为了测定该合金中铝的含量,有人设计如下实验:
(1)取样品ag,称取时使用的仪器名称为________.
(2)将样品溶于足量的稀盐酸中,过滤,滤液中主要含有________离子,滤渣中含有________,在溶解过滤时使用的仪器________.
(3)在滤液中加入过量的氢氧化钠溶液,过滤,写出该步骤操作中反应的化学方程式________________.
(4)在第(3)步的滤液中通入足量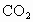 ,过滤,将沉淀用蒸馏水洗涤数次后,烘干并灼烧质量不再减少为止,冷却后称量,质量为bg.
,过滤,将沉淀用蒸馏水洗涤数次后,烘干并灼烧质量不再减少为止,冷却后称量,质量为bg.
(5)计算合金中铝的质量分数________________.
查看答案和解析>>
科目: 来源: 题型:022
(2000·全国)紫杉醇是一种新型抗癌药,其分子式为 ,这是由如下的A酸和B醇生成的一种酯.
,这是由如下的A酸和B醇生成的一种酯.
A.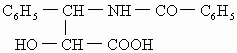 (
( 是苯基)
是苯基)
B.R—OH(R是一个含C、H、O的基团)
(1)A可在无机酸催化下水解,其反应方程式是_______________.
(2)A水解所得的氨基酸不是天然蛋白质水解产物,因为氨基不在(填希腊字母)_________位.
(3)写出ROH的分子式________________.
查看答案和解析>>
科目: 来源: 题型:022
(2000·全国)氯普鲁卡因盐酸盐是一种局部麻醉剂,麻醉作用较快、较强,毒性较低,其合成路线如下:
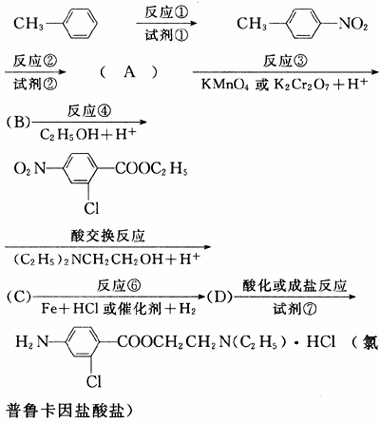
请把相应反应名称填入下表中,供选择的反应名称如下:
氧化、还原、硝化、碘化、氯代、酸化、碱化、成盐、酯化、酯交换、水解

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com