
科目: 来源:福建师大附中2010-2011学年高二下学期期中考试化学试题 题型:022
已知[Ni(NH3)2Cl2]可以形成A、B两种固体,则[Ni(NH3)2Cl2]分子的空间构型是________.若A在水中溶解度较大,B在CCl4中溶解度较大,试画出A、B分子的几何构型:A________,B________.
查看答案和解析>>
科目: 来源:浙江省兰溪一中2010-2011学年高二下学期期中考试化学试题 题型:022
在含有Cl-.Br-.I-的溶液中,已知其浓度均为0
.1 mol/L,而AgCl.AgBr.AgI的浓度积(mol2/L2)分别为:1.6×10-10.4.1×10-15.1.5×10-16.若向混合溶液中逐滴加入AgNO3溶液并充分搅拌时,首先析出的沉淀是________,最后析出的沉淀是________;当AgBr沉淀开始析出时,溶液中Ag+的浓度是________.查看答案和解析>>
科目: 来源:江苏省扬州中学2010-2011学年高二下学期期中考试化学试题 题型:022
工业上常以废铜屑(含少量铁、油污)制取胆矾(CuSO4·5H2O),流程如下(已知Ksp[Cu(OH)2]=2.2×10-20,Ksp[Fe(OH)2]=8.0×10-16,Ksp[Fe(OH)3]=4.0×10-38):

回答:(1)步骤①中纯碱的作用是________________.
(2)步骤②中鼓入空气需足量,否则制得的胆矾晶体中会含杂质________.
(3)步骤③中A试剂可以是________,作用是________________.
查看答案和解析>>
科目: 来源:辽宁省抚顺市六校联合体2011届高三二模理综化学试题 题型:022
纯碱是一种重要的化工原料.目前制碱工业主要有“氨碱法”和“联合制碱法”两种工艺.请按要求回答下列问题:
(1)“氨碱法”产生大量CaCl2废弃物,请写出该工艺中产生CaCl2的化学方程式________.
(2)写出“联合制碱法”有关反应的化学方程式________;________.
(3)CO2是制碱工业的重要原料,“联合制碱法”和“氨碱法”中CO2的来源有何不同?
________________.
(4)绿色化学的重要原则之一是提高反应的原子利用率.根据联合制碱法的总反应,列出计算原子利用率的表达式:原子利用率(%)=________.
查看答案和解析>>
科目: 来源:江苏省东台市2010-2011学年高一上学期期未考试化学试题 题型:022
海水占地球总储水量的
97.2%.若把海水淡化和化工生产结合起来,既可以解决淡水资源缺乏的问题,又可以充分利用海洋资源.(1)海水中含有大量的氯化钠.请写出氯原子的原子结构示意图
________;(2)目前国际上实用的
“海水淡化”主要技术之一是蒸馏法.蒸馏法是将海水变成蒸汽,蒸汽经过冷却而得高纯度淡水,由此可判断蒸馏法是________(填物理变化、化学变化);(3)工业上利用电解饱和食盐水可制得重要化工产品,又称为“氯碱工业”.电解饱和食盐水的化学方程式为
________;(4)近年来有人提出了一种利用氯碱工业产品及氯化钠循环治理含二氧化硫废气并回收二氧化硫的方法,该方法的流程如下:
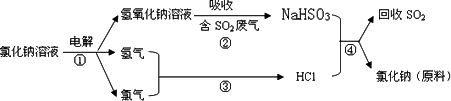
试写出④的化学反应方程式
________.查看答案和解析>>
科目: 来源:江苏省宿豫中学2011届高三第二次模拟考试化学试题 题型:022
锂被誉为“高能金属”.工业上用硫酸与β-锂辉矿(LiAlSi2O6和少量钙镁杂质)在250~300℃反应,生成Li2SO4以及硅铝化合物、MgSO4等,其工业生产流程如下:
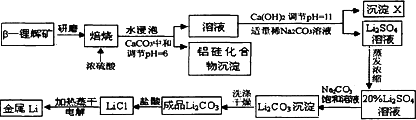
(1)用氧化物形式表示LiAlSi2O6的组成:________.
(2)沉淀X的主要成分是(写化学式)________.
(3)流程中两次使用了Na2CO3溶液,试说明前后浓度不同的原因:____________.
(4)锂和氢气在加热时能反应生成白色固体氢化锂,氢化锂遇到水就立即溶解并释放出大量的气体.试写出氢化锂遇水反应的化学方程式:________.
(5)将盐酸与Li2CO3完全反应后的溶液,加热蒸干得到固体,再将其熔融电解生产锂.电解时产生的氯气中会混有少量氧气,原因是________________.
查看答案和解析>>
科目: 来源:河北省魏县一中2010-2011学年高二3月份月考化学试题 题型:022
选择下列某种答案的序号,填入下表的空格
①同位素 ②同素异形体 ③同分异构体 ④同系物 ⑤同种物质

查看答案和解析>>
科目: 来源:江苏省常州市横山桥高级中学2011届高三第一次调研考试化学试题 题型:022
钛在地壳中的含量比铜多61倍,排第十位.钛及其化合物大量应用于航空、造船、电子、化学、医疗器械、电讯器材等各个领域.
由钛铁矿(FeTiO3)提取金属钛(海绵钛)的主要工艺过程如下(部分产物省略):
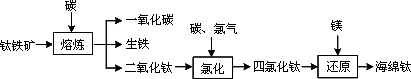
(1)氯化的过程为:将二氧化钛、炭粉混合,在高温条件下通入氯气制得TiCl4和一种可燃性气体.该反应的化学方程式为________.
(2)还原过程为:用过量的镁在高温条件下与TiCl4反应制得海绵钛.
①写出此反应的化学方程式:________.
②简述如何从上述所得产物中获得金属钛?简述步骤并写出有关反应方程式.
(3)还原过程必须
在1070 K的温度下进行,你认为还应该控制的反应条件是________.查看答案和解析>>
科目: 来源:辽宁省宽甸第二中学2011届高三第一次月考试化学试题 题型:022
质子核磁共振谱(NMR)是研究有机物结构的有力手段之一.
(1)现有分子式均为C2H4O2的两种链状分子组成的混合物,如果在NMR谱上观察到氢原子给出的信号有两种情况:第一种情况峰的强度比为3∶1;第二种情况峰的强度比为2∶1∶1.由此推断该混合物的组成(写结构简式)是:________或________.
(2)A、B两种有机物均由C、H、N、O四种元素组成,且分子中都含有苯环,A是天然蛋白质的水解产物,其中含氧元素的质量分数为19.4%,A有如下转化关系(假设每步反应完全进行)
0.01 mol A![]() 盐C
盐C![]() 盐D
盐D
①光谱测定显示:A分子结构中不存在甲基,A的结构简式为________;
②B是A同分异构体,它是苯的某种同系物经硝化反应后的唯一产物,B的结构简式为________.
查看答案和解析>>
科目: 来源:辽宁省宽甸第二中学2011届高三第一次月考试化学试题 题型:022
按要求回答下列问题:某有机物的一个分子含50个电子.
(1)若它为烃,则它的分子式可能为________;如果该烃在一定条件下不能与氢气反应,且该烃的一氯代物只有两种同分异构体,则该烃的结构简式为________.
(2)若它为含碳、氢、氧的有机物,它的分子式可能有________.(同一个碳原子上连接两个-OH的结构不稳定)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com