
科目: 来源: 题型:022
X、Y、Z三种元素的原子序数依次增大,且位于第三周期,价电子数之和为10。它们的最高价氧化物对应的水化物之间任意两种都能反应生成盐和水。M元素原子的L层上有6个电子。
(1)写出X、Y、Z、M的元素符号:X________、Y________、Z________、M________。
(2)X单质跟水反应的离子方程式为_________________________________。
(3)Z、M的氢化物的稳定性顺序:________>________。
(4)Y元素最高价氧化物对应水化物在水溶液中的电离方程式为__________________。
(5)这四种元素的原子半径的大小顺序是________,所形成的简单离子半径的大小顺序是________。
(6)X、Y、Z的最高价氧化物对应的水化物之间两两反应生成盐和水的离子方程式为
________________、________________、________________。
查看答案和解析>>
科目: 来源: 题型:022
X、Y、Z三种常见的短周期元素,可以形成XY2、Z2Y、XY3、Z2Y2、Z2X等化合物.已知Y的离子和Z的离子有相同的电子层结构,X离子比Y离子多一个电子层.试回答:
(1)X离子的结构简图为________.
(2)工业上由XY2制取XY3的化学方程式为________________________.
(3)Z2Y对应水化物的碱性比LiOH________.
(4)Z2Y2的电子式为________,其中含有________键和________键.Z2Y2溶在水中的反应方程式为________.
(5)Z2X属于________晶体,它与水反应的离子方程式为________.
查看答案和解析>>
科目: 来源: 题型:022
(1)天然放射性元素![]() (钍)经过一系列α衰变和β衰变之后,变成
(钍)经过一系列α衰变和β衰变之后,变成![]() (铅).下列判断正确的是( )
(铅).下列判断正确的是( )
A.铅核比钍核少24个中子
B.衰变过程中共有4次α衰变和8次β衰变
C.铅核比钍核少8个质子
D.衰变过程中共有6次α衰变和4次β衰变
(2)铅在周期表中位于第________周期,第________族.
(3)铅的主要化合价有+2、+4价,其中________价的铅的化合物不稳定.预测Pb3O4与浓盐酸反应的化学方程式___ _____.
查看答案和解析>>
科目: 来源: 题型:022
不同元素的气态原子失去最外层一个电子所需要的能量(设其为E)如下图所示。
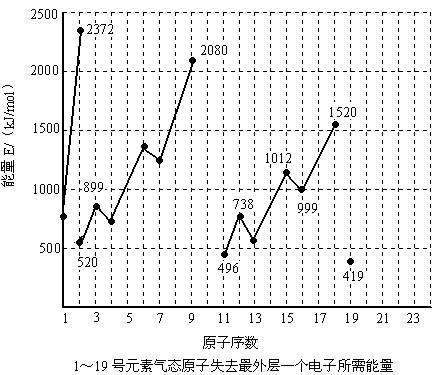
试根据元素在周期表中的位置,分析图中曲线的变化特点,并回答下列问题。
(1)同主族内不同元素的E值变化的特点是___ __ __ _ 。各主族中E值的这种变化特点体现了元素性质的__ ___变化规律。
(2)同周期内,随原子序数增大,E值增大。但个别元素的E值出现反常现象。试预测下列关系中正确的是________(填写编号,多选倒扣)。
①E(砷)>E(硒); ②E(砷)<E(硒); ③E(溴)>E(硒); ④E(溴)<E(硒)
(3)估计1mol气态Ca原子失去最外层一个电子所需能量E值的范围:_________<E<___________。
(4)10号元素E值较大的原因是________。
查看答案和解析>>
科目: 来源: 题型:022
将正确的答案填入下列空格中。在原子序数为1~20的元素中:
(1)与水反应最剧烈的金属、非金属分别是________、________。
(2)自然界中硬度最大的单质是________。
(3)常温下有颜色的单质气体是________。
(4)最高价氧化物对应的水化物碱性最强的是________,酸性最强的是________。
(5)气态氢化物最稳定的是________。
(6)气态氢化物中含氢量最高的是________。
(7)原子半径最小的是________,最大的是________。
(8)常温下既能溶于强酸,又能溶于强碱的氧化物是________。
查看答案和解析>>
科目: 来源: 题型:022
门捷列夫在19世纪中叶,曾根据他所发现的周期律,预言过第四周期ⅣA族的锗(当时他称为类硅)元素的性质。试根据周期律推测:
(1)锗的金属性和非金属性,锗能否与酸、碱作用;
(2)GeO2在水中的溶解性;
(3)Ge(OH)4的酸、碱性;
(4)GeH4的热稳定性。
查看答案和解析>>
科目: 来源: 题型:022
已知五种元素的原子序数的大小顺序为C>A>E>D>E,A、C同周期,B、C同主族。A与B形成离子化合物A2B中所有离子的电子数相同,其电子总数为30;D和E可形成4核10个电子分子。试回答下列问题:
(1)写出五种元素的元素符号:A________、B________、C________、D________、E________。
(2)用电子式表示离子化合物A2B的形成过程:________。
(3)写出下列物质的电子式:
①D元素形成的单质________。
②E与B形成的化合物________。
③A、B、E形成的化合物________。
④D与E形成的化合物________。
⑤D、C、E形成的离子化合物________。
查看答案和解析>>
科目: 来源: 题型:022
今有A、B、C、D四种短周期元素,它们的核电荷数依次增大,A与C、B与D分别是同族元素,B、D两元素的质子数之和是A、C两元素质子数之和的两倍,这四种元素中有一种元素的单质能溶解于CS2溶剂中,则四种元素是A________,B________,C________,D________。
查看答案和解析>>
科目: 来源: 题型:022
元素周期表中前7周期的元素如下表所示:
表 元素周期表中前7周期的元素数目
|
周期数 |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
|
元素数 |
2 |
8 |
8 |
8 |
18 |
32 |
32 |
(1)第六、七周期比第四、五周期多了14种元素,其原因是________。
(2)周期表中________族所含元素最多,________族元素形成化合物最多。
(3)请分析周期数与元素数的关系,然后预言第八周期最多可能含有的元素种数为 ( )
A.18
B.2
C.50
D.64
(4)居里夫人发现的镭是元素周期表中第七周期的ⅡA族元素,下列关于镭的性质的描述中不正确的是 ( )
A.在化合物中呈+2价
B.氢氧化物呈两性
C.单质使水分解,放出氢气
D.碳酸盐难溶于水
查看答案和解析>>
科目: 来源: 题型:022
有A、B、C、D四种短周期元素,它们的核电荷数依次增大。A与C、B与D分别是同族元素。B、D两元素的质子数之和是A、C两元素质子数之和的2倍。这四种元素中有一种元素易溶解于CS2溶剂中。则四种元素是:A_____ B_____ C_____ D_____两种均含四种元素的化合物相互反应放出气体的化学方程式为:____________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com