
科目: 来源: 题型:022
原子序数为114号的稳定同位素![]() 预测。
预测。
(1)114X元素位于元素周期表第________周期________族,为________(填“金属”、“非金属”)元素。
(2)其最高价氧化物及其对应水化物的分子式分别是________、________(用含X的式子表示),并估计后者为________性(填“酸”、“碱”或“两性”)。
(3)它与氯生成化合物的分子式:________、________(用含X的式子表示)。
查看答案和解析>>
科目: 来源: 题型:022
在短周期元素中,均用化学符号表示。
(1)常温下有颜色的气体单质是________。
(2)除稀有气体外,原子半径最大的元素是________;原子半径最小的元素是________。
(3)气态氢化物中最稳定的是________,含氢的质量分数最大的是________,其氢化物水溶液呈碱性的元素是________。
(4)在最高价氧化物中呈最高正价的元素是________。
(5)地壳中含量最多的元素是________。
查看答案和解析>>
科目: 来源: 题型:022
根据周期律对角线规则,金属Be与铝单质及其化合物的性质相似.又知AlCl3熔、沸点较低,易升华.试回答下列问题:
(1)写出Be与NaOH溶液反应的离子方程式(生成Na2BeO2)___ _____.
(2)Be(OH)2和Mg(OH)2可用试剂________鉴别,其离子方程式为____ ____.
(3)BeCl2是________(填“离子化合物”或“共价化合物”),其电子式为_____ ___.BeCl2水溶液呈酸性,其水解的离子方程式为_____ ___.
查看答案和解析>>
科目: 来源: 题型:022
下表是元素周期表的一部分。表中所列的字母分别代表某一化学元素。
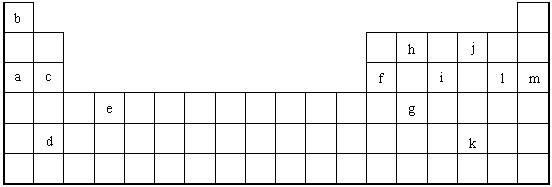
(1) 下列______(填写编号)组元素的单质可能都是电的良导体。
①a、c、h ②b、g、k ③ c、h、l ④d、e、f
(2) 如果给核外电子足够的能量,这些电子便会摆脱原子核的束缚而离去。核外电子离开该原子或离子所需要的能量主要受两大因素的影响:原子核对核外电子的吸引力和形成稳定结构
的倾向。
下表是一些气态原子失去核外不同电子所需的能量(kJ×mol-1);
|
|
锂 |
X |
Y |
|
失去第一个电子 |
519 |
502 |
580 |
|
失去第二个电子 |
7296 |
4570 |
1820 |
|
失去第三个电子 |
11799 |
6920 |
2750 |
|
失去第四个电子 |
|
9550 |
11600 |
①通过上述信息和表中的数据分析为什么锂原子失去核外第二个电子时所需的能量要远远大于失去第一个电子所需的能量_ _______。
②表中X可能为以上13种元素中的________(填写字母)元素。用元素符号表示X和j形成化合物的化学式________。
③Y是周期表中________族元素。
④以上13种元素中,________(填写字母)元素原子失去核外第一个电子需要的能量最多。
查看答案和解析>>
科目: 来源: 题型:022
砷(As)是第四周期的主族元素。砷及其几种化合物的部分性质如下:
(1)砷和热的浓H2SO4反应,生成As2O3,反应的化学方程式为________。
(2)As2O3俗称砒霜,溶解在热水中,生成砷酸(H3AsO3),反应的化学方程式为________。
(3)砷的气态氢化物砷化氢AsH3(也称胂),在常温下能在空气中自燃,反应式为________,在缺氧条件,胂受热分解为砷和氢气。
(4)法医在鉴定砒霜中毒时,常用马氏试砷法。取试样(含砒霜)与锌、盐酸混合,反应生成氯化锌、水和砷化氢,然后将生成的砷化氢气体导入玻璃管中隔绝空气加热,如果试样中含有砷的化合物,则生成的AsH3在管内受热分解生成亮黑色的单质砷,称为“砷镜”。这一方法能检出0.0001毫克的砷。有关反应的化学方程式为_____ ___。
查看答案和解析>>
科目: 来源: 题型:022
1919年,Langmuir提出等电子原理:原子数相同、电子总数相同的分子,互称为等电子体。等电子体的结构相似、物理性质相近。
(1)根据上述原理,仅由第2周期元素组成的共价分子中,互为等电子体的是:________和________;________和________。
(2)此后,等电子原理又有所发展。例如,由短周期元素组成的微粒,只要其原子数相同,各原子最外层电子数之和相同,也可互称为等电子体,它们也具有相似的结构特征。
在短周期元素组成的物质中,与![]() 为等电子体的分子有:________、________。
为等电子体的分子有:________、________。
查看答案和解析>>
科目: 来源: 题型:022
下表是元素周期表的一部分,回答下列有关问题
|
族 周期 |
ⅠA |
ⅡA |
ⅢA |
ⅣVA |
ⅤA |
ⅥA |
ⅦA |
0 |
|
2 |
|
|
|
|
① |
|
② |
|
|
3 |
③ |
④ |
⑤ |
⑥ |
|
⑦ |
⑧ |
⑨ |
|
4 |
⑩ |
⑾ |
|
|
|
|
⑿ |
|
(1)写出下列元素符号:①________,⑥_______,⑦________,⑾________.
(2)在这些元素中,最活泼的金属元素是________,最活泼的非金属元素是________,最不活泼的元素是________.
(3)在这些元素的最高价氧化物对应水化物中,酸性最强的是________,碱性最强的是________,呈两性的氢氧化物是________,写出三者之间相互反应的化学方程式.
(4)在这些元素中,原子半径最小的是________,原子半径最大的是________.
(5)在③与④中,化学性质较活泼的是________,怎样用化学实验证明?答:___ ____ _ .在⑧与⑿中,化学性质较活泼的是________,怎样用化学实验证明?答:_______ _.
查看答案和解析>>
科目: 来源: 题型:022
X、Y、Z三种元素的原子序数依次增大,且位于同一周期,价电子数之和为10.它们的最高价氧化物的水化物之间任意两种都能反应生成盐和水.M元素与上述三种元索位于相邻的周期,而M原子的L电子层上有4个电子.
(1)写出X、Y、Z、M的元素符号:X________,Y________,Z________,M________.
(2)Y位于元素周期表中第________周期,第________族.
(3)Z原子的结构示意图为________.
(4)X单质跟水反应的离子方程式为________________.
查看答案和解析>>
科目: 来源: 题型:022
有X、Y、Z三种短周期元素,X的气态氢化物化学式为H2X,此氢化物的式量与X最高价氧化物的式量之比为17∶40,X原子核内质子数与中子数相等,Y与X可以形成离子化合物Y2X,Y的阳离子电子层结构与Ne相同,Z与X同周期,其气态单质是双原子分子,两原子共用1对电子。试回答:
(1)写出各元素符号:X________、Y________、Z________。
(2)X离子的结构简图为________。X与Y形成的离子化合物的电子式为________,Z和氢形成的化合物的电子式为________________。
(3)Y单质在空气中燃烧的化学方程式为____________________________________,生成物与水反应的化学方程式为_________________________________________________。
查看答案和解析>>
科目: 来源: 题型:022
A、B、C、D是四种常见的非金属单质,这些单质的式量中B最小,C次之.在室温下,它们之中有三种气体,一种固体.这些单质和甲、乙、丙、X、Y五种化合物之间存在如下图所示关系.以上所涉及元素均为短周期元素,据此推断:
(1)化合物乙的化学式是________;
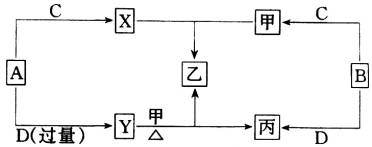
(2)上图中的化学反应共有________种基本反应类型,其中共有________个化合反应;
(3)上述四种单质中存在同素异形体的元素是(写元素符号)________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com