
科目: 来源: 题型:022
A、B、C是三种主族元素,分别位于周期表的三个相连续的不同周期,其原子序数依次增大。已知A原子的次外层电子数是2,A、B原子最外层电子数之和等于C原子的最外层电子数,C和B能发生反应。A的最高价氧化物的水化物是一种强酸,B的氢氧化物难溶于水。则A________,B________,C________。(用符号表示)
查看答案和解析>>
科目: 来源: 题型:022
有原子序数依次增大的A、B、C、D、E五种短周期元素,它们可组成甲、乙、丙、丁四种化合物,各化合物中原子个数比关系如下表:
甲 乙 丙 丁
化合物中
各元素原子
个数比 A∶C=1∶1 B∶A=1∶4 D∶E=1∶3 B∶E=1∶4
其中A、B两种原子的核电荷数之差等于它们的原子最外层电子数之和;B原子最外层电子数比其次外层电子数多2个;在周期表中,C是E的邻族元素,化学性质活泼;D和E则位于同一周期,且D和E的原子序数之和为30。
(1)D和E同属哪一周期元素?推断依据是什么?
_________________________________________。
_________________________________________。
(2)根据题目提供的条件,推断E在周期表中的族序数所必要的条件是什么?
_________________________________________。
_________________________________________。
(3)向甲的水溶液中加入MnO2,反应的化学方程式
_____________________________________________________________________________。
(4)乙可以燃烧,燃烧时火焰呈蓝色,试写出乙燃烧的化学方程式
_____________________________________________________________________________。(5)D形成的单质在浓硫酸中钝化,而在盐酸中反应生成丙,试解释D在浓硫酸中钝化的原因:
_______________________________________________________________________________
_____________________________________________________________________________。
写出D与盐酸反应生成丙的反应式:
_____________________________________________________________________________。
(6)向3mL1mol×L-1的KI溶液中依次注入下列试剂:①1mL5mol×L-1的盐酸;②0.5mL 30%甲溶液;③1mL丁,经充分振荡后,静置,可得一紫色溶液。这种紫色溶液是什么___________________________________________________________________________________。
查看答案和解析>>
科目: 来源: 题型:022
原子核对核外电子的吸收力形成稳定结构的倾向
下表是一些气态原子失去核外不同电子所需的能量(KJ×mol-1)
锂 X Y
失去第一个电子 519 502 580
失去第二个电子 7296 4570 1820
失去第三个电子 11799 6920 2750
失去第四个电子 9550 11600
①通过上述信息和表中的数据分析为什么锂原子失去核外第二个电子时所需的能量要远远大于失去第一个电子所需的能量。
_____________________________________________________________________________。
②表中X可能为以上13种元素中的________(填写字母)元素。用元素符号表示X和j形成化合物的化学式________。
③Y是周期表中________族元素。
④以上13种元素中________(填写字母)元素原子失去核外第一个电子需要的能量最多。
查看答案和解析>>
科目: 来源: 题型:022
已知五种元素的原子序数的大小顺序为C>A>B>D>E;A、C同周期,B、C同主族;A与B形成离子化合物A2B中所有离子的电子数相同,其电子总数为30;D和E可形成4核10个电子分子,试回答下列问题:
(1)A、D两元素的原子序数分别为A________、D________。
(2)指出C元素在元素周期表中的位置________________________________。
(3)写出下列物质的电子式:
D元素形成的单质______________。
D、C、E三元素形成的离子化合物________________________________。
查看答案和解析>>
科目: 来源: 题型:022
X、Y、Z三种常见的短周期元素,可以形成XY2、Z2Y、XY3、Z2Y2、Z2X等化合物。已知Y的离子和Z的离子有相同的电子层结构,X离子比Y离子多一个电子层,试回答:
(1)X是________元素;Y是________元素;Z是________元素。
(2)Z2Y2的电子式______________________,它与水反应的化学方程式是____________
___________________。
(3)工业上制取XY3的化学方程式是____________________________________________
_____________________________。
查看答案和解析>>
科目: 来源:物理教研室 题型:022
有机物A由C、H、O、N四种元素组成.它能溶于盐酸生成B,也能溶于NaOH生成C,两分子A在一定条件下失去一分子水结合成D.D在盐酸存在下水解得到B,在碱性条件下水解得到C.已知D的相对分子质量是312.(A和D分子的烃基中都含有苯环),试推导A的结构式并写出各步化学反应方程式.
查看答案和解析>>
科目: 来源:物理教研室 题型:022
在一定温度下,把2mol 和1mol
和1mol 通入一个一定容积的密闭容器里,发生如下反应:
通入一个一定容积的密闭容器里,发生如下反应:
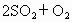

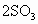
当此反应进行到一定程度时,反应混合物就处于化学平衡状态.现在该容器中,维持温度不变,令a、b、c分别代表初始加入的 和
和 的物质的量(mol).如果a、b、c取不同的数值,它们必须满足一定的关系,才能保证达到平衡时,反应混合物中三种气体的百分含量仍跟上述平衡时完全相同,请填写下列空白:
的物质的量(mol).如果a、b、c取不同的数值,它们必须满足一定的关系,才能保证达到平衡时,反应混合物中三种气体的百分含量仍跟上述平衡时完全相同,请填写下列空白:
(1)若a=0,b=0,则c=______.
(2)若a=0.5,则b=______,c=______.
(3)a、b、c取值必须满足的一般条件是(请用两个方程式表示,其中一个只含a和c,另一个只含b和c):______________.
查看答案和解析>>
科目: 来源:物理教研室 题型:022
恒温下,将amol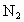 与bmol
与bmol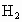 的混合气体通入一个固定容积的密闭容器中,发生如下反应:
的混合气体通入一个固定容积的密闭容器中,发生如下反应:
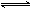
 .
.
(1)若反应进行到某时刻t时, 计算a的值.
计算a的值.
(2)反应达到平衡时,混合气体的体积为716.8L(标况),其中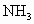 的含量(体积分数)为25%,计算平衡时
的含量(体积分数)为25%,计算平衡时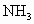 的物质的量.
的物质的量.
(3)原混合气体与平衡混合气体的总物质的量之比(写最简整数比,下同),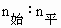 =________________.
=________________.
(4)则原混合气体中,a∶b=_____________.
(5)达到平衡时,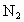 和
和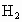 的转化率之比,
的转化率之比, =___________.
=___________.
查看答案和解析>>
科目: 来源: 题型:022
某元素的同位素,它的氯化物XCl2 1.11g溶于水制成溶液后,加入1mol/L的AgNO3溶液20mL恰好完全反应。若这种同位素原子核内有20个中子,求:
(1)Z值和A值;
(2)X元素在周期表中的位置;
(3)把X的单质放入水中,有何现象?写出反应的化学方程式。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com