
科目: 来源:内蒙古呼伦贝尔市牙克石林业一中2012届高三第二次模拟考试化学试题 题型:022
某烃类化合物A的质谱图表明其相对分子质量为84,红外光谱表明分子中含有碳碳双键,核磁共振谱表明分子中只有一种类型的氢.
(1)A的结构简式为________;
(2)A中的碳原子是否都处于同一平面?________(填“是”或者“不是”);
(3)在下图中,D1、D2互为同分异构体,E1、E2互为同分异构体.
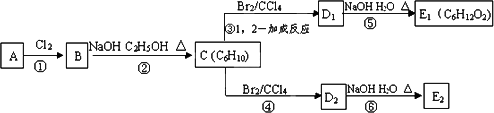
反应②的化学方程式为________;C的化学名称为________;E2的结构简式是________;
④、⑥的反应类型依次是________.
查看答案和解析>>
科目: 来源:选修高手化学苏教·化学反应原理 苏教版 题型:022
蛇纹石矿可以看作由MgO、Fe2O3、Al2O3、SiO2组成.由蛇纹石制取碱式碳酸镁的实验步骤如下:

(1)蛇纹石矿加盐酸溶解后,溶液里除了Mg2+外,还含有的金属离子是________.
(2)进行Ⅰ操作时,控制溶液pH=7-8(有关氢氧化物沉淀的pH见下表)
![]()
Ca(OH)2不能过量,若Ca(OH)2过量可能会导致________溶解、________沉淀.
(3)从沉淀混合物A中提取红色氧化物作颜料,先向沉淀物A中加入________(填入物质的化学式),然后________、________、________(依次填写实验操作名称).
(4)物质循环使用,能节约资源.上述实验中,可以循环使用的物质是________(填写物质化学式).
(5)现设计一个实验,确定产品aMgCO3·bMg(OH)2·cH2O中a、b、c的值,请完善下列实验步骤(可用试剂:浓硫酸、碱石灰):
①样品称量 ②高温分解 ③________ ④________ ⑤MgO称量
(6)18.2 g产品完全分解后,产生6.6 g CO2和8.0 g MgO,由此可知,产品的化学式中:
a=________,b=________,c=________.
查看答案和解析>>
科目: 来源:选修高手化学人教·有机化学基础 人教版 题型:022
| |||||||||||||||||||||||||||||||||
查看答案和解析>>
科目: 来源:江苏省泰州中学2010-2011学年高二下学期期中考试化学试题 题型:022
水体中二价汞离子可以与多种阴离子结合成不同的存在形态.水溶液中二价汞主要存在形态与Cl-、OH-的浓度关系如图所示:
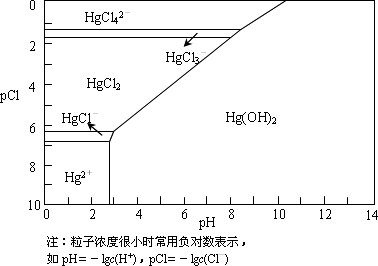
(1)正常海水(Cl-的浓度大于0.1 mol/L)中汞元素的主要存在形态是________.少量Hg(NO3)2溶于0.001 mol/L的盐酸后得到无色透明溶液,其中汞元素的主要存在形态是________.
(2)Hg(NO3)2固体易溶于水,但溶于水时常常会出现浑浊,其原因是________(用离子方程式表示),为了防止出现浑浊,可采取的措施是________.
(3)处理含汞废水的方法很多.下面是常用的两种方法,汞的回收率很高.
①置换法:用废铜屑处理含Hg2+的废水.反应的离子方程式为________.
②化学沉淀法:用硫化钠处理含Hg(NO3)2的废水,生成HgS沉淀.已知:
Ksp(HgS)=1.6
×10-52,当废水中c(S2-)=1×10-5 mol/L时,c(Hg2+)=________.③用难溶的FeS作为沉淀剂也可使Hg2+转化为HgS而除去,该反应的离子方程式:________.有人认为加入FeS作为沉淀剂还可以起到净化水的作用,请运用所学知识解释________
查看答案和解析>>
科目: 来源:高一化学 专题4 化学科学与人类文明(苏教版必修2) 苏教版 题型:022
随着全球淡水资源危机日益严重,世界各国都把目光投向了占全球总水量约97%的汪洋大海,希望从苦涩的海水中提取可以饮用的淡水.
(1)海水淡化由来已久.二次大战时,一艘为盟军运送军事物资的商船遇难漂流到一座荒岛上.为了获取淡水,船员们将救生艇上的铜皮空气箱拆下,在空气箱上加盖一块边缘向内卷曲形成水槽的铜盖,做成一个简易蒸馏器.加热箱内的海水,水蒸气在盖顶冷凝后顺着边缘流进水槽,再滴入淡水桶内.根据上述文字的描述,为下图简易蒸馏器示意图补画铜盖.
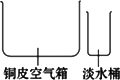
(2)目前海水淡化有了许多新工艺,最广泛应用的为多级闪蒸法,其流程示意图如下图.已知一级闪蒸室和二级闪蒸室内的压强分别是p1和p2,且p2<p1<1.013×105 Pa.

请回答:
a.②处海水的温度比①处海水温度高的原因是________.
b.盐水能够从一级闪蒸室流入二级闪蒸室的原因是________.
(3)为降低能耗,多级闪蒸法采取了降压和________两项措施.降压可以降低能耗的理由是________.
(4)海水淡化亦称海水脱盐.该工艺过程包括海水预处理、脱盐、淡化水的后处理等.下列属于海水预处理的是________、________、________(填序号).
①淡水收集
②除掉悬浮物
③杀灭海洋生物
④除掉海水中的盐分
⑤水质检测
⑥降低海水浑浊度为了检验所收集的淡水中是否含有氯离子,通常采用的试剂是________.
(5)除了从海水中获得淡水之外,人们还可以从中提取其他物质.试比较多级闪蒸海水淡化与海水晒盐的主要异同点,每项至少写两点.
相同点:________.
差异点:________.
(6)海水淡化是解决淡水资源危机的途径之一.它涉及各个领域.如要建立一个以多级闪蒸法为主要工艺的海水淡化厂,涉及的经济问题有________;涉及的技术问题有________.若请你以海水淡化为主题,从一个侧面出发,对其进行探究,你最关注的问题是________;根据该问题拟定的课题名称是________.
查看答案和解析>>
科目: 来源:江苏省宿豫中学2011届高三第二次模拟考试化学试题 题型:022
硫酸钙是一种用途非常广泛的产品.
(1)25℃时,Ksp(CaSO4)=7.10×10-5.在1 L 0.1 mol·L-1 CaCl2溶液中加入1 L 0.2 mol·L-1的Na2SO4溶液,充分反应后(假设混合后溶液的体积变化忽略不计)溶液中Ca2+物质的量的浓度为________mol·L-1.
(2)某校课外活动小组为测定已部分脱水的生石膏的组成(xCaSO4·yH2O),做如下实验:将固体放在坩埚中加热,经测量剩余固体质量随时间变化如图所示.
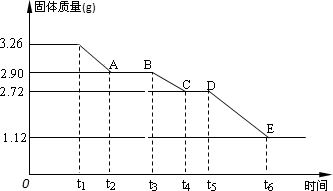
①x∶y=________.
②t2~t3时间段固体的化学式为________.
③t5~t6时间段固体质量减轻的原因是产生了两种气体,其中一种能使品红溶液褪色,则该时间段所发生反应的化学方程式为________.
查看答案和解析>>
科目: 来源:福建省福州市罗源一中2011届高三第一次月考化学试题 题型:022
铜是重要的金属材料.试回答下列问题:
(1)工业上可用Cu2S和Cu2O反应制取粗铜,同时生成了二氧化硫.该反应中氧化剂为________,产生的尾气用足量的氨水来吸收,此反应的化学方程式为________.若用电解粗铜制取精铜,电解时,阳极材料是________,电解液中必须含有的阳离子是________.
(2)电子工业曾用30%的FeCl3溶液腐蚀敷有铜箔的绝缘板制印刷电路板,写出该反应的化学反应方程式________,为了从使用过的废腐蚀液中回收铜,并重新得到FeCl3溶液,设计如下实验流程:
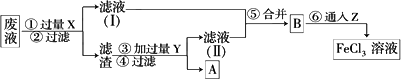
上述流程中,所加试剂的化学式为:X________,Y________,Z________;
第⑥步反应的离子方程式为________.
查看答案和解析>>
科目: 来源:安徽省皖南八校2011届高三年级第一次联考化学试题 题型:022
某芳香族化合物A的分子中含有C.H、O、N四种元素,相同状况下,其蒸气的密度为氢气密度的68.5倍.现以苯为原料合成A,并最终制得F(一种染料中间体),转化关系如下(一些非主要产物己略去):
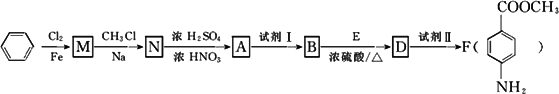
己知:
ⅰ.R-Cl+2Na+Cl-![]() →R-
→R-![]() +2NaCl(R、
+2NaCl(R、![]() 为烃基)
为烃基)
ⅱ.![]()
ⅲ.![]() 苯胺(弱碱性,易氧化)
苯胺(弱碱性,易氧化)
请回答下列问题:
(1)写出A的结构简式________.
(2)N→A的反应类型是________.
(3)①上述转化中试剂I和试剂Ⅱ分别是:试剂Ⅰ________;试剂Ⅱ________(选填字母).
a.KMnO4(H+)
b.Fe/盐酸
c.NaOH溶液
②若上述转化中物质A依次与试剂Ⅱ、试剂I、化合物E(浓硫酸jΔ)作用,能否得到F?________,为什么?________.
(4)用核磁共振氢谱可以证明化合物E中含有________种处于不同化学环境的氢.
(5)写出同时符合下列要求的两种D的同分异构体的结构简式:
①属于芳香族化合物,分子中有两个互为对位的取代基,其中一个取代基是硝基;
②分子中含有![]() 结构.
结构.
(6)有一种D的同分异构体w,在酸性条件下水解后,可得到一种能与FeCl3溶液发生显色反应的产物,写出w在酸性条件下水解的化学方程式:________.
(7)F的水解反应如下:
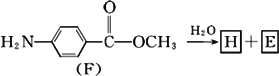
化合物H在一定条件下经缩聚反应可制得高分子纤维,广泛用于通讯、导弹、宇航等领域.请写出该缩聚反应的化学方程式:________
查看答案和解析>>
科目: 来源:广东省高州一中2009-2010学年高二学科竞赛化学试题 题型:022
聚合氯化铝晶体
[A12(OH)nCl6-n.·H2O]m是介于AlCl3和Al(OH)3之间的一种水溶性无机高分子聚合物,其制备原料主要是铝加工行业的废渣——铝灰,它主要含Al2O3、Al,还有SiO2等杂质.聚合氯化铝生产工艺流程如下:
(1)反应中副产品E是________(用化学式表示);
(2)升高pH至4.0~4.5的目的是________;
(3)生产过程中可循环使用的物质是________(用化学式表示);
(4)为使得到的晶体较纯净,生产过程中使pH升高的c物质可选用________(填编号);
a.NaOH b.Al c.氨水 d.A12O3 e.NaAlO2
(5)为测定[A12(OH)nCl6-n.·H2O]m中的n值,进行如下实验:
①称取a g晶体,制成粉末,加热至质量不再变化时,得到b g固体.
②另取a g晶体,进行如下操作:
用A试剂溶解![]() 加足量AgNO3溶液
加足量AgNO3溶液![]() 操作c
操作c![]() 烘干
烘干![]() 称量为c g固体.
称量为c g固体.
操作C为________、________(填操作名称).
n=________(用含a、b、c的代数式表示).
查看答案和解析>>
科目: 来源:重庆市杨家坪中学2009-2010学年高二下学期第二次月考化学试题 题型:022
化合物A是石油化工的一种重要原料,用A和水煤气为原料经下列途径合成化合物D(分子式为C3H6O3).
已知:
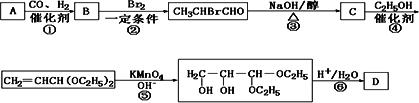
请回答下列问题:
(1)写出下列物质的结构简式:
A:________;B:________;C:________;D:________.
(2)指出反应②的反应类型________.
(3)写出反应③的化学方程式________.
(4)反应④的目的是________________.
(5)化合物![]() 是D的一种同分异构体,它最早发现于酸牛奶中,是人体内糖类代谢的中间产物.
是D的一种同分异构体,它最早发现于酸牛奶中,是人体内糖类代谢的中间产物.![]() 在浓硫酸存在的条件下加热,既可以生成能使溴水褪色的化合物E(C3H4O2),又可以生成六原子环状化合物F(C6H8O4).请分别写出
在浓硫酸存在的条件下加热,既可以生成能使溴水褪色的化合物E(C3H4O2),又可以生成六原子环状化合物F(C6H8O4).请分别写出![]() 生成E和F的化学方程式:
生成E和F的化学方程式:
![]()
![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com