
科目: 来源: 题型:038
化学电池在通讯、交通及日常生活中有着广泛的应用.
(1)目前常用的Ni—Cd电池,其电池总反应可以表示为
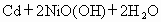

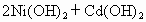
已知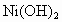 和
和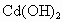 均难溶于水但能溶于酸,以下说法中正确的是
均难溶于水但能溶于酸,以下说法中正确的是
[ ]
①以上反应是可逆反应
②以上反应是不可逆反应
③充电时化学能转变为电能
④放电时化学能转变为电能
(2)废弃的电池已成为重要的环境污染物,有资料表明一节废镍镉电池可以使一平方米面积的耕地失去使用价值,在酸性土壤中这种污染尤为严重.这是因为_________________________________________________.
(3)另一种常用的电池是锂电池,由于它的比容量(单位质量电极材料所能转换的电量)特别大而广泛用于心脏起搏器,一般使用时间可长达十年.该电池反应可表示为: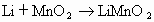
试回答:锂电池比容量特别大的原因是____________________________.
锂电池中的电解质溶液需用非水溶剂配制,而不能用水溶液,请用化学方程式表明原因_______________________________________________.
查看答案和解析>>
科目: 来源: 题型:038
某工厂排出的废水里含 的游离态氯和
的游离态氯和 的氢离子,为了除去废水中的游离态氯,而且使废水变为中性,有人提出用如图所示方案.在废水排出管的A、B处分别注入一定流量的废烧碱溶液和亚硫酸钠溶液.
的氢离子,为了除去废水中的游离态氯,而且使废水变为中性,有人提出用如图所示方案.在废水排出管的A、B处分别注入一定流量的废烧碱溶液和亚硫酸钠溶液.
试写出;(1)A、B处应加入的物质的化学式:A_____________,B____________________________________________________________.
(2)A、B处反应的离子方程式:A:_______________________________,
B:___________________________________________________________.
(3)每处理 的该废水,需加入
的该废水,需加入 的
的 溶液的体积是多少?
溶液的体积是多少?
(4)除去氯后的废水中氢离子浓度约为多少?
查看答案和解析>>
科目: 来源: 题型:038
某地有一池塘,生长着丰富的水生植物和多种鱼、虾.后来,由于化工厂将大量污水排入池塘中,使水质恶化,各种水生生物先后死亡.根据题意回答下列问题:
(1)从生态平衡角度看,池塘这种变化说明了________________________.
(2)造成这种变化的原因是_______________________________________.
(3)经检测,污水中含有0.012mol/L的游离溴,可用亚硫酸钠除去污水中的溴,请写出其化学方程式:____________________________________.
(4)处理5L这种污水,需加入0.05mol/L的亚硫酸钠多少升才能将溴全部除去.
(5)要使池塘恢复本来面目,首先要解决的问题是____________________,首先要恢复的生物是___________________________________________.
查看答案和解析>>
科目: 来源: 题型:038
中央电视台每晚《晚间新闻》后,都要预报42个重点城市的空气质量,它一般将这些城市空气中的 和可吸入颗粒的含量(可用
和可吸入颗粒的含量(可用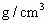 )分为8个等级.目前,测定空气中
)分为8个等级.目前,测定空气中 含量主要用氧化还原反应原理测定.假如给你一个气体流速管(单位时间内通过气体的体积恒定,且无除尘和吸收气体作用),请你设计一个实验装置,测定你所在地区的空气中
含量主要用氧化还原反应原理测定.假如给你一个气体流速管(单位时间内通过气体的体积恒定,且无除尘和吸收气体作用),请你设计一个实验装置,测定你所在地区的空气中 和可吸入颗粒的含量.
和可吸入颗粒的含量.
已知: 气体与酸性
气体与酸性 溶液反应时,
溶液反应时, 被还原为
被还原为 ,
, 被氧化成
被氧化成 .
.
现有药品:0.1mol/L的酸性 溶液、颗粒吸附剂、品红试液、pH试纸.
溶液、颗粒吸附剂、品红试液、pH试纸.
现有仪器:密闭容器用 或
或 表示,敞口仪器用
表示,敞口仪器用 ;导管用
;导管用 ;气体流速管用
;气体流速管用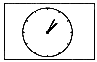 .
.
(1)配制200mL0.1mol/L酸性 溶液,需用仪器有玻璃棒、____________、________________、___________、_______________.玻璃棒的作用是____________________、__________________________.
溶液,需用仪器有玻璃棒、____________、________________、___________、_______________.玻璃棒的作用是____________________、__________________________.
(2)画出测定空气中 和可吸入颗粒含量的实验装置图(并指出仪器中的药品).
和可吸入颗粒含量的实验装置图(并指出仪器中的药品).
(3)若气体流速管中气体流速为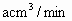 ,当tmin后200mL0.1mol/L
,当tmin后200mL0.1mol/L 溶液恰好褪色.求空气中
溶液恰好褪色.求空气中 的含量(
的含量(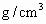 ).
).
(4)若要测定空气中可吸入颗粒的含量,需要测出的数据有___________.
空气中 的含量还可用检测管测定,其原因是:指示剂
的含量还可用检测管测定,其原因是:指示剂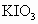 发生作用,可能发生的反应(未配平)有:
发生作用,可能发生的反应(未配平)有:
①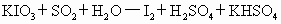
②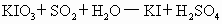
(5)检气管是按照上述两个方程式中的____________方程式设计的.如果是按另一方程式设计的实验程序,能检测出空气中的二氧化硫的含量吗?__________________(填“能”“不能”或“无法确定”),理由是_____________________________________________________________.
(6)为了能够准确地测定出空气中的二氧化硫的含量,拉动采样器的手柄则应该注意的是____________________,理由是____________________.
查看答案和解析>>
科目: 来源: 题型:038
2003年3月27日据广东报道,巨大的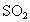 、NO等的排放量使广东成为酸雨重灾区,2002年全省酸雨频率为45.4%,占全省面积63%的17个市已被国务院划为酸雨控制区,酸雨曾使大片水稻突然枯死,并且每年因酸雨污染造成的经济损失就达40亿元左右.问:
、NO等的排放量使广东成为酸雨重灾区,2002年全省酸雨频率为45.4%,占全省面积63%的17个市已被国务院划为酸雨控制区,酸雨曾使大片水稻突然枯死,并且每年因酸雨污染造成的经济损失就达40亿元左右.问:
(1)酸雨导致水稻死亡的原因是什么?
(2)试述酸雨的形成过程,并写出化学方程式.
(3)请提出两条防治酸雨的措施.
查看答案和解析>>
科目: 来源: 题型:038
吸烟有害健康,科学实验表明香烟所产生的烟雾中至少有300多种化合物不同程度上对人体有害.为了鉴定该烟雾中是否存在 和CO,在对香烟燃烧产生的烟雾进行适当处理后依次通过足量的以下试剂:①澄清石灰水 ②浓
和CO,在对香烟燃烧产生的烟雾进行适当处理后依次通过足量的以下试剂:①澄清石灰水 ②浓 ③灼热的黑色氧化铜粉末 ④澄清石灰水发现①、④澄清石灰水变浑浊,其他无明显现象,试回答:
③灼热的黑色氧化铜粉末 ④澄清石灰水发现①、④澄清石灰水变浑浊,其他无明显现象,试回答:
(1)①中现象说明_____________________________________________.
(2)烟雾中是否存在CO____________________________,做出此判断所依据的实验现象为_____________________________________________.
(3)③中无明显变化的原因可能是_________________________________.
查看答案和解析>>
科目: 来源: 题型:038
煤是我国城乡居民普遍使用的一种家用能源.烟煤中含有硫化物(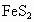 ),其燃烧可产生
),其燃烧可产生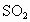 .设某40万户的城市,每户每天燃烧5kg,假设某烟煤中
.设某40万户的城市,每户每天燃烧5kg,假设某烟煤中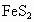 的质量分数为5%,燃烧时有90%的硫转化为
的质量分数为5%,燃烧时有90%的硫转化为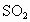 ,被排放到大气中,
,被排放到大气中,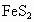 燃烧时的反应式为
燃烧时的反应式为 ,问:
,问:
(1)燃烧1t煤可产生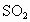 多少千克?
多少千克?
(2)该城市若全部以这种烟煤作燃料,每年(按365天计算),将有多少吨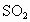 排放到大气中.
排放到大气中.
(3)下雨时测定其雨水呈酸性,写出反应方程式____________________.
(4)测定某份雨水样品,每隔一定时间测定一次pH,发现pH逐渐变小见下表,其原因是:
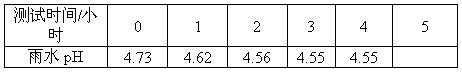
(5)简述这种雨水将给环境中的生物和非生物造成哪些影响?
(6)你能提出两三项减轻这种危害的对策吗?
查看答案和解析>>
科目: 来源: 题型:038
为了研究血红蛋白与不同气体的结合能力,进行了如下实验:
请回答下列问题:
新鲜鸭血(Hb)
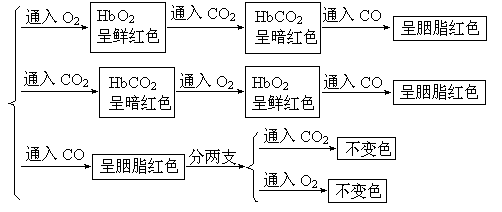
(1)呈胭脂红色的物质是__________________________(用符号表示);
(2)在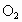 、
、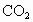 、CO中,与血红蛋白结合能力最强的是_________;
、CO中,与血红蛋白结合能力最强的是_________;
(3)用化学方程式表示动物进行呼吸的过程:
内呼吸______________________________________________________;
外呼吸_______________________________________________________;
(4)下列气体,比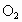 与血红蛋白结合力要强能引起中毒的是___________;
与血红蛋白结合力要强能引起中毒的是___________;
[ ]
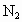
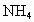
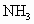
(5)人体进行太快而且太深的呼吸会引起_________(“酸中毒”或“碱中毒”),原因是_________________________________________________.
查看答案和解析>>
科目: 来源: 题型:038
NO分子因污染空气而臭名昭著.近年来,发现少量的NO在生物体内许多组织中存在,它有扩张血管、免疫、增强记忆的功能,而成为当前生命科学的研究的热点,NO亦被称为“明星分子”.请回答下列问题.
(1)NO对环境的危害在于______________________(填以下项目的编号).
[ ]
A.破坏臭氧层
B.高温下能使一些金属被氧化
C.造成酸雨
D.与人体血红蛋白结合
(2)在含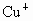 离子的酶的活化中心中,亚硝酸根离子可转化为NO,写出
离子的酶的活化中心中,亚硝酸根离子可转化为NO,写出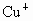 和亚硝酸根离子在酸性水溶液中反应的离子方程式_____________________________________________________________.
和亚硝酸根离子在酸性水溶液中反应的离子方程式_____________________________________________________________.
(3)在常温下,把NO气体压缩到100个大气压,在一个体积固定的容器里加热到50℃,发现气体的压力迅速下降,压力降至略小于原压力2/3就不再改变,已知其中一种产物为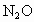 ,写出上述变化的化学方程式_____________________________________________________________.
,写出上述变化的化学方程式_____________________________________________________________.
(4)解释变化(3)中为什么最后的气体总压力小于原压力的2/3?
答案:________________________________________________________.
查看答案和解析>>
科目: 来源: 题型:038
1982年,我国南方某城市降了一场较大的酸雨,使得郊区种植的西瓜全部烂死.
(1)形成酸雨的主要原因是_______________________________________.
(2)酸雨对环境污染的危害表现为_________________________________.
(3)经检验,酸雨中除 和
和 以外,还含有
以外,还含有 、
、 、
、 和
和 等离子,其浓度
等离子,其浓度 、
、 、
、 、
、 ,则该酸雨的pH=_________________________________________________________.
,则该酸雨的pH=_________________________________________________________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com