
科目: 来源:物理教研室 题型:058
某温度下,在2L容器中3种物质间进行反应,X、Y、Z的物质的量随时间的变化曲线如下图.反应在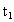 min时到达平衡,依图所示:
min时到达平衡,依图所示:
(1)该反应的化学方程式是___________________.
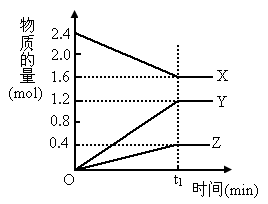
(2)反应起始至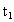 minY的平均反应速率是_________________________.
minY的平均反应速率是_________________________.
(3)物质X的转化率是___________________.
查看答案和解析>>
科目: 来源:物理教研室 题型:058
如图所示,把试管放入盛有25℃时饱和澄清石灰水的烧杯中,试管开始放入几小块镁片,再用滴管滴入5mL盐酸于试管中.回答下列问题:
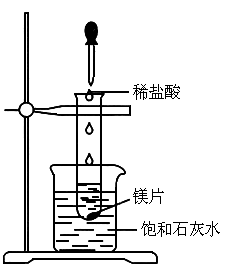
(1)实验中观察到的现象是____________________________________.
(2)产生上述现象的原因______________________________________.
(3)写出有关反应的离子方程式__________________.
(4)由实验推知,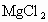 溶液和
溶液和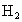 的总能量____________(填“大于”、“小于”或“等于”)镁片和盐酸的总能量.
的总能量____________(填“大于”、“小于”或“等于”)镁片和盐酸的总能量.
查看答案和解析>>
科目: 来源:物理教研室 题型:058
(1)在一定量的硫酸溶液中,加足量的锌,要使产生的氢气的量保持不变,但反应速率加快,可加入_____________溶液,其理由是_____________.
(2)在一定量的盐酸溶液中加入足量的锌,要使产生的氢气的量保持不变,但反应速率变慢.除水外,可加入__________晶体,其理由是__________.
查看答案和解析>>
科目: 来源:物理教研室 题型:058
在锌与某浓度的盐酸起反应的实验中,一个学生得到下面的结果: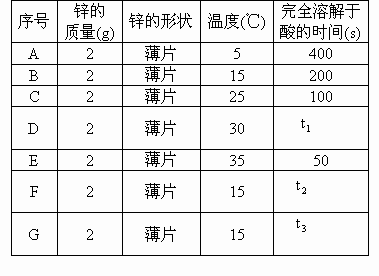
下列说法中①
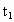 =75.5 ②
=75.5 ②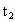 >200>
>200>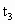 ,③单位时间内消耗锌的质量
,③单位时间内消耗锌的质量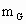 >
> >
>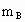 正确的是___________.
正确的是___________.
查看答案和解析>>
科目: 来源:物理教研室 题型:058
在碘化钾和硫酸的混合溶液中加入过氧化氢水溶液,迅速发生反应,放出大量气体,反应过程表示如下:
①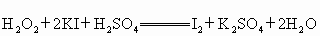 ;
;
② ;
;
③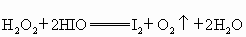
(1)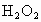 在反应③中__________(填正确选项的标号).
在反应③中__________(填正确选项的标号).
A.是氧化剂
B.是还原剂
C.既是氧化剂又是还原剂
D.既不是氧化剂也不是还原剂
(2)有人认为上述反应说明了碘单质是过氧化氢分解的催化剂,你认为_____________(填“对”或“不对”),其理由是__________________.
(3)上述反应说明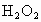 、
、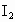 、HIO氧化性从强到弱的顺序是_________.
、HIO氧化性从强到弱的顺序是_________.
(4)已知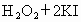
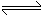
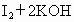 ,试用
,试用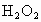 、KI溶液、淀粉溶液、水等药品,设计一个实验来说明与一定量
、KI溶液、淀粉溶液、水等药品,设计一个实验来说明与一定量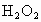 反应的KI溶液浓度越大,反应速率越快.
反应的KI溶液浓度越大,反应速率越快.
_____________________________________________
查看答案和解析>>
科目: 来源:物理教研室 题型:058
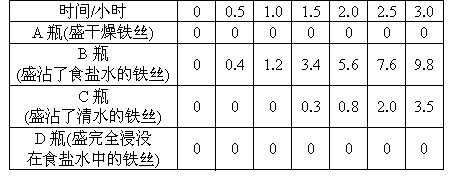
某学生在A、B、C、D四只小烧瓶中分别放入干燥的细铁丝、浸过食
盐水的细铁丝、浸过清水的细铁丝、食盐水及细铁丝,并使铁丝完全浸没在食盐水中,然后装配成如图所示的四套装置,每隔一段时间测量导管中水面上升的高度,结果如下表(表中所列数据为导管中水面上升的高度/cm)所示.
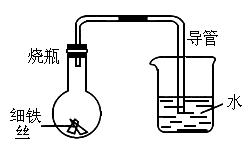
(1)导管中水面为什么会上升?____________________________.
(2)上述实验中,铁生锈的速率由大到小的排列顺序为(填小烧杯号):___________________________.
(3)影响铁生锈的因素有:____________________________.
查看答案和解析>>
科目: 来源:物理教研室 题型:058
(1)下列方法中可以证明
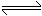
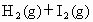 已达平衡状态的是__________________.
已达平衡状态的是__________________.
①单位时间内生成nmol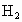 的同时生成nmolHI,
的同时生成nmolHI,
②一个H-H键断裂的同时有两个H—I键断裂,
③百分组成w/(HI)=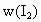 ,
,
④反应速率v(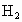 )=
)=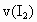 =v(HI)/2时,
=v(HI)/2时,
⑤c(HI)∶c(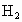 )∶c(
)∶c(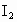 )=2∶1∶1时,
)=2∶1∶1时,
⑥温度和体积一定时,某一生成物浓度不再变化,
⑦温度和体积一定时,容器内压强不再变化,
⑧条件一定,混合气体的平均相对分子质量不再变化,
⑨温度和体积一定时,混合气体的颜色不再变化,
⑩温度和压强一定时,混合气体的密度不再变化.
(2)在上述⑥~⑩的说法中能说明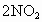
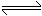
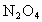 达到平衡状态的是________________.
达到平衡状态的是________________.
查看答案和解析>>
科目: 来源:物理教研室 题型:058
亚硫酸钠和碘酸钾在酸性溶液中发生以下反应:

(1)其中氧化剂是___________,若反应中有5mol电子转移,则生成的碘是___________mol.
(2)该反应的过程和机理较复杂,一般认为发生以下①~④反应:
①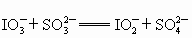 (反应速率慢)
(反应速率慢)
②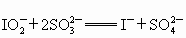 (反应速率快)
(反应速率快)
③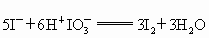 (反应速率快)
(反应速率快)
④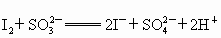 (反应速率快)
(反应速率快)
根据上述步骤推测该反应总的反应速率由___________反应决定(填写上述四步反应的序号).
(3)若预先加入淀粉溶液,由上述四步反应可以看出必须在___________离子消耗完全时,才会有使淀粉变蓝的现象产生.
查看答案和解析>>
科目: 来源:物理教研室 题型:058
实验室分析白铁(镀锌)样品成分,称取1.00g样品放在烧杯中加入过量的盐酸,然后用玻片盖住烧杯,首先观察到有大量的气泡冒出,后来放出气体速度变慢,最后完全反应.接着加入过量的氢氧化钠溶液,过滤,分离出灰绿色沉淀;该沉淀在空气中加热至质量不变,得到1.20g红色粉末.已知锌及其化合物与铝及其化合物性质相似,试回答:
(1)白铁镀锌的作用是__________________________________________.
(2)盖玻片的作用是____________________________________________.
(3)放出气体的速度由快到慢的原因是____________________________.
(4)为什么要加入过量的NaOH溶液______________________________.
(5)在空气中加热灰绿色沉淀的化学方程式是______________________.
(6)锌在样品中的质量分数是____________________________________.
查看答案和解析>>
科目: 来源:物理教研室 题型:058
银器皿日久表面逐渐变黑色,这是由于生成了硫化银(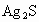 ).有人设计用原电池的原理进行“抛光”,其处理方法为:将一定浓度的食盐溶液放入一铝制容器中,再将变黑的银器浸入溶液中,放置一段时间后,黑色会褪去而银恢复光泽,且不会损失.试回答:
).有人设计用原电池的原理进行“抛光”,其处理方法为:将一定浓度的食盐溶液放入一铝制容器中,再将变黑的银器浸入溶液中,放置一段时间后,黑色会褪去而银恢复光泽,且不会损失.试回答:
(1)食盐的作用是__________________________.
(2)在此原电池反应中,负极发生的电极反应为_____________________,
正极发生的电极反应为_________________________________________.
(3)反应过程中产生臭鸡蛋气味的气体,溶液中发生的反应为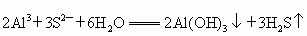 ,则原电池总反应方程式为________________________________________.
,则原电池总反应方程式为________________________________________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com