
科目: 来源: 题型:058
将一定量含![]() 和Fe的混合物投入50mL2mol/L
和Fe的混合物投入50mL2mol/L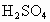 溶液中,在一定条件下固体混合恰好完全溶解,放出448mL(标准状况)下的气体,在所得溶液中加入KSCN溶液,无红色出现如果用足量的CO在高温下与相同质量的此固体混合物充分反应,能得到铁多少克?
溶液中,在一定条件下固体混合恰好完全溶解,放出448mL(标准状况)下的气体,在所得溶液中加入KSCN溶液,无红色出现如果用足量的CO在高温下与相同质量的此固体混合物充分反应,能得到铁多少克?
查看答案和解析>>
科目: 来源: 题型:058
按图所示装置连接好仪器.
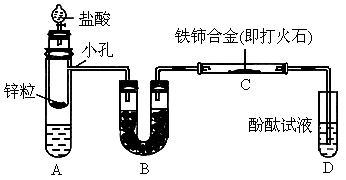
已知:A中装有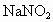 和
和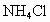 混合溶液,B中装有碱石灰,C中有铁铈合金,D中有酚酞试液.
混合溶液,B中装有碱石灰,C中有铁铈合金,D中有酚酞试液.
C中发生反应的热化学方程式为: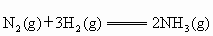 ;
;
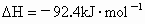
实验步骤如下:①检查装置的气密性;②用酒精灯加热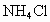 和
和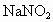 饱和溶液,待有气体生成,可停止加热,但仍有大量气体产生;③再用酒精灯给铁铈合金加热至一定温度;④从分液漏斗中滴入一定浓度盐酸,不久见酚酞试液变红.
饱和溶液,待有气体生成,可停止加热,但仍有大量气体产生;③再用酒精灯给铁铈合金加热至一定温度;④从分液漏斗中滴入一定浓度盐酸,不久见酚酞试液变红.
回答下列问题:
(1)写出A中两溶液间发生反应的化学方程式________,此反应为________热反应(填“放”或“吸”);
(2)先用酒精灯加热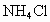 、
、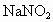 饱和溶液的目的是______________;
饱和溶液的目的是______________;
(3)C中铁铈合金的作用是______________,要先加热至一定温度的原因是______________;
(4)如果通入C中的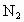 、
、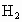 各有1 mol、3 mol,为什么反应后放出的热量比92.4 kJ少?
各有1 mol、3 mol,为什么反应后放出的热量比92.4 kJ少?
查看答案和解析>>
科目: 来源: 题型:058
在标准状况下,将1.40g氮气,1.60g氧气和4.00g氩气混合,该混合气体的体积是________L,其平均相对分子质量为________;若将该混合气体通过灼热的铜网,经充分反应后,剩余气体恢复到标准状况时,混合气体的平均相对分子质量为________________________.
查看答案和解析>>
科目: 来源: 题型:058
如图所示装置可用来制取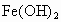 和观察
和观察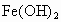 在空气中被氧化时的颜色变化.实验时必须使用铁屑、6mol/L硫酸溶液,其他试剂任选.填写下列空白:
在空气中被氧化时的颜色变化.实验时必须使用铁屑、6mol/L硫酸溶液,其他试剂任选.填写下列空白:
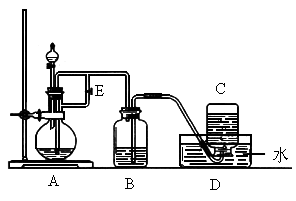
(1)B中盛有一定量的NaOH溶液,A中应预先加入的试剂是________,A中反应的化学方程式为______________________________________.
(2)实验开始时应先将活塞E__________(填“打开”或“关闭”),其目的是______________.在C中收集到的气体主要为___________________.
(3)简述生成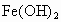 的操作过程________________________________.
的操作过程________________________________.
(4)拔去装置B中的橡皮塞,使空气进入,写出有关反应的化学方程式∶_____________________________________________________________.
查看答案和解析>>
科目: 来源: 题型:058
将70g过氧化钠和氧化钠的混合物跟98g水充分反应后,所得氢氧化钠溶液中溶质的质量分数为50%.试分别写出过氧化钠和氧化钠跟水反应的化学方程式,并计算原混合物中过氧化钠和氧化钠的质量各多少克.
查看答案和解析>>
科目: 来源: 题型:058
在一定条件下用普通铁粉和水蒸气反应,可以得到铁的氧化物,该氧化物又可以经过此反应的逆反应,生成颗粒很细的铁粉,这种粉具有很高的反应活性,在空气中受撞击或受热时会燃烧,所以俗称“引火铁”.请分别用下图中示意的两套仪器装置,制取上述铁的氧化物和“引火铁”.实验中必须使用普通铁粉、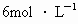 盐酸,其他试剂自选(装置中必要铁架台、铁夹、铁圈、石棉网、加热设备等在图中均已略去).填写下列白:
盐酸,其他试剂自选(装置中必要铁架台、铁夹、铁圈、石棉网、加热设备等在图中均已略去).填写下列白:
(1)①实验进行时试管A中应加入的试剂是__________;
②烧瓶B的用是_____________;
③烧瓶C的作用是___________;
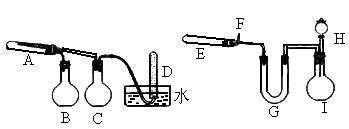
④在试管D中集得到的是_________.
(2)实验时,U型管G中应加入的试剂是_______.长颈漏斗H中应加入____________.
(3)两套装置中,在实验时需要加热的仪器是(填该仪器对应字母)____________.
(4)试管E中发生反应的化学程式是____________.
(5)为了安全,在E管中的反应发生前,在F出口处必须___________;
E管中的反应开始后,在F出口处应__________.
查看答案和解析>>
科目: 来源: 题型:058
有一块表面氧化成氧化钠的金属钠,质量是5.4g,将它投入到100g水中完全反应后,收集到0.1g气体,试计算:
(1)被氧化成氧化钠的金属钠的质量是多少克?
(2)未被氧化的金属钠的质量是多少克?
(3)反应后所得溶液的溶质的质量分数是多少?
查看答案和解析>>
科目: 来源:上海市长宁区2012届高三上学期期末质量抽测化学试题 题型:058
某工厂生产硼砂过程中产生的固体废料,主要含有MgCO3、MgSiO3、CaMg(CO3)2、Al2O3和Fe2O3等,回收其中镁的工艺流程如下:
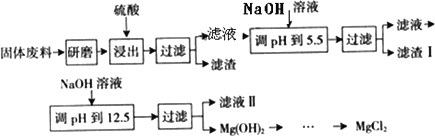
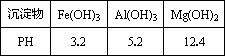
部分阳离子以氢氧化物形式完全沉淀时溶液的pH见上表,请回答下列问题:
1.“浸出”步骤中,为提高镁的浸出率,可采取的措施有________(要求写出两条).
2.滤渣Ⅰ的主要成分是________.
Mg(ClO3)2在农业上可用作脱叶剂、催熟剂,可采用复分解反应制备:
MgCl2+2NaClO3→Mg(ClO3)2+2NaCl
已知四种化合物的溶解度(S)随温度(T)变化曲线如下图所示:
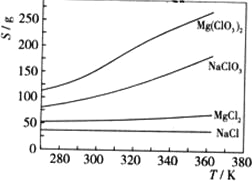
3.将反应物按化学反应方程式计量数比混合制备Mg(ClO3)2.简述可制备Mg(ClO3)2的原因:________.
4.按题44中条件进行制备实验.在冷却降温析出Mg(ClO3)2过程中,常伴有NaCl析出,原因是:________.除去产品中该杂质的方法是:________.
查看答案和解析>>
科目: 来源:江苏省仪征中学2011-2012学年高二上学期期末模拟考试化学试题(选修) 题型:058
通常用燃烧的方法测定有机物的分子式,可在燃烧室内将有机物样品与纯氧在电炉加热下充分燃烧,根据产品的的质量确定有机物的组成.下图所示的是用燃烧法确定有机物物分子式的常用装置.
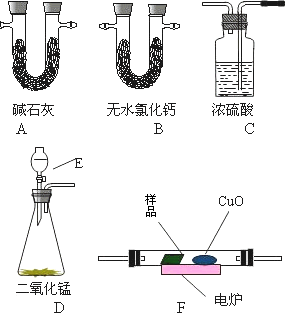
(1)现准确称取0.44 g样品(只含C、H、O三种元素中的两种或三种),经燃烧后A管增重0.88 g,B管增重0.36 g.请回答:(1)按上述所给的测量信息,装置的连接顺序应是
D![]() ________
________![]() F
F![]() ________
________![]() ________;
________;
(2)A、B管内均盛有有固态试剂,A管的作用是________;
(3)E中应盛装什么试剂:________;
(4)如果把CuO网去掉,A管重量将________;(填“增大”、“减小”、或“不变”)
(5)请改进这套装置的一个不足之处________;
(6)该有机物的实验式为________;
(7)要确定该有机物的分子式,还必须知道的数据是________.(填编号)
①消耗液体E的质量
②样品的摩尔质量
③CuO固体减少的质量
④C装置增加的质量
⑤燃烧消耗O2的物质的量
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com