
科目: 来源:物理教研室 题型:022
原子结构模型的演变共分为:公元前5世纪古希腊哲学家的观点;19世纪初英国科学家道尔顿的观点;1904年汤姆生的观点;1911年卢瑟福的观点;1913年玻尔的观点;20世纪现代科学家的观点.
简要分析上述六个阶段原子结构模型的联系及演变过程.
查看答案和解析>>
科目: 来源:非常讲解·教材全解全析 高中化学 必修1 (山东版) 山东版 题型:022
120℃、101.3 kPa条件下,有2 L H2O、2 L CO、1 L CO2、1.5 L O2和1 L H2组成的混合气体.将混合气体通过分别放足量Cu粉、C粉和CuO粉的三个灼热的反应管.假设气体通过每个反应管都能充分反应,且不记三个反应管以何种顺序排列,问:
(1)尾气是否有可能是单一气体?________(填“可能”或“不可能”).若可能,该气体是________.
(2)原气体中是否有几种(或一种)不可能再存在于尾气之中?________(填“有”或“没有”).若有,它们(或它)是________.
(3)原气体中是否有几种(或一种)一定存在于尾气中?________(填“有”或“没有”).若有,它们(或它)是________.
查看答案和解析>>
科目: 来源: 题型:022
用铜、银和硝酸银设计一个原电池,此电池负极是 ,负极的电极反应是 。将锌片、铜片连接后浸入稀硫酸溶液中,构成了原电池,工作一段时间,锌片质量减少了3.25g,铜表面析出氢气________L(标准状况下),导线中通过了 mol电子。
查看答案和解析>>
科目: 来源: 题型:022
取少量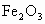 粉末(红棕色)加入适量盐酸,所发生反应的化学方程式为______________________,反应后得到的溶液呈_______色。用此溶液进行以下实验:
粉末(红棕色)加入适量盐酸,所发生反应的化学方程式为______________________,反应后得到的溶液呈_______色。用此溶液进行以下实验:
(1)取少量溶液置于试管中,滴入NaOH溶液,可观察到有红褐色沉淀生成,反应的化学方程式为____________________,此反应属于___________(填反应类型)。
(2)在小烧杯中加入20mL蒸馏水,加热至沸腾后,向沸水中滴入几滴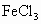 浓溶液,继续煮沸直至溶液呈______色,即可制得
浓溶液,继续煮沸直至溶液呈______色,即可制得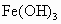 胶体。
胶体。
(3)取另一小烧杯也加入20mL蒸馏水,向烧杯中加入1mL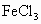 溶液,振荡均匀后,将此烧杯(编号甲)与盛有
溶液,振荡均匀后,将此烧杯(编号甲)与盛有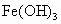 胶体的烧杯(编号乙)一起放置于暗处,分别用激光笔照射烧杯中的液体,可以看到___________烧杯中的液体产生了丁达尔效应。这个实验可以用来区别_______。
胶体的烧杯(编号乙)一起放置于暗处,分别用激光笔照射烧杯中的液体,可以看到___________烧杯中的液体产生了丁达尔效应。这个实验可以用来区别_______。
(4)取乙烧杯中少量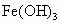 胶体置于试管中,向试管中滴加一定量稀盐酸,边滴边振荡,会出现一系列变化。
胶体置于试管中,向试管中滴加一定量稀盐酸,边滴边振荡,会出现一系列变化。
①先出现红褐色沉淀,原因是____________________________。
②随后沉淀溶解,溶液呈棕黄色,写出此反应的化学方程式:_____________________________________。
(5)已知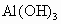 胶体能够净水,则
胶体能够净水,则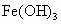 胶体_______(填“能”或“不能”)净水。
胶体_______(填“能”或“不能”)净水。
查看答案和解析>>
科目: 来源: 题型:022
我国有着悠久的“玉文化”,古代精美绝伦的玉器,其工艺之精湛,至今为人们所叹服。据研究,古代是以精选的河砂作为磨料对玉石进行加工的。请你对玉石可以用河砂作磨料进行琢磨的原因进行推测,并查阅相关资料予以证实或修正。
查看答案和解析>>
科目: 来源: 题型:022
化学电池在通讯、交通及日常生活中有着广泛的应用.
(1)目前常用的镍(Ni)镉(Cd)电池,其电池总反应可以表示为:


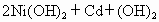
已知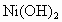 和
和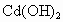 均难溶于水但能溶于酸,以下说法中正确的是[ ]
均难溶于水但能溶于酸,以下说法中正确的是[ ]
①以上反应是可逆反应 ②以上反应不是可逆反应 ③充电时化学能转变为电能 ④放电时化学能转变为电能
(2)废弃的镍镉电池已成为重要的环境污染物,有资料表明一节废镍镉电池可以使一平方米面积的耕地失去使用价值.在酸性土壤中这种污染尤为严重.这是因为_______________________________.
(3)另一种常用的电池是锂电池(锂是一种碱金属元素,其相对原子质量为7),由于它的比容量(单位质量电极材料所能转换的电量)特别大而广泛应用于心脏起搏器,一般使用时间可长达十年,它的负极用金属锂制成,电池总反应可表示为:
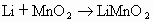
试回答:锂电池比容量特别大的原因是____________________________.锂电池中的电解质溶液需用非水溶剂配制,为什么这种电池不能使用电解质的水溶液?请用化学方程式表示其原因______________________________.
查看答案和解析>>
科目: 来源: 题型:022
市场上出售的“热敷袋”,其主要成分是铁屑、炭粉、木屑与少量氯化钠、水等.它在使用之前需用塑料袋与空气隔绝.使用时启开塑料袋上的气孔,轻轻揉搓就会放出热量来.当使用完后还会发现有铁锈生成,依上述现象回答:
(1)“热敷袋”放出的热量是利用铁发生了_________反应放出的热量.
(2)炭粉的主要作用是_____________________.
(3)加入氯化钠的作用是________________________.
(4)试用有关的电极反应式、离子方程式和化学方程式来表明上述变化过程:
①负极:______________;正极______________.
②离子方程式:____________________________.
③有关化学方程式:__________________________.
查看答案和解析>>
科目: 来源: 题型:022
有A、B、C、D四种金属,将A与B用导线连接起来,浸入电解质溶液中,B不易腐蚀.将A、D分别投入等物质的量浓度的盐酸中,D比A反应剧烈.将铜浸入B的盐溶液里,无明显变化,如果把铜浸入C的盐溶液里,有金属C析出.据此判断它们的活动性由强到弱的顺序是__________.
查看答案和解析>>
科目: 来源: 题型:022
我国首创以铝椏掌鴹海水电池作为能源的新型海水标志灯,它以海水为电解质溶液,靠空气中的氧气使铝不断氧化而产生电流.只要把灯放入海水中数分钟,就会发出耀眼的白光.则该电源负极材料为________,正极材料为___________,正、负极反应分别为______________________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com