
科目: 来源:广东省2009届高三化学各地名校月考试题汇编-实验基础(3) 题型:013
|
下表是食用碘盐包装上的部分说明,下列说法正确的是
| |
| [ ] | |
A. |
高温会导致碘的损失 |
B. |
碘酸钾可氧化氯化钾 |
C. |
可用淀粉检验碘盐中的碘酸钾 |
D. |
该碘盐中碘酸钾含量为20~50 mg/kg |
查看答案和解析>>
科目: 来源:广东省2009届高三化学各地名校月考试题汇编-实验基础(2) 题型:013
|
在K2CO3样品中含Na2CO3、KNO3、Ba(NO3)2中的一或二种杂质.将13.8 g该样品溶于足量水中得到澄清溶液,再加入过量CaCl2溶液,可得9.0 g沉淀,则原样品中含有的杂质会是 | |
| [ ] | |
A. |
肯定有Na2CO3,没有Ba(NO3)2 |
B. |
肯定有KNO3,没有Ba(NO3)2,可能还有Na2CO3 |
C. |
肯定没有Na2CO3,Ba(NO3)2 |
D. |
无法判断何种为肯定或否定的杂质 |
查看答案和解析>>
科目: 来源:广东省2009届高三化学各地名校月考试题汇编-实验基础(2) 题型:013
下图所示为实验室中完成不同的化学实验所选用的装置或进行的操作,其中没有明显错误的是________
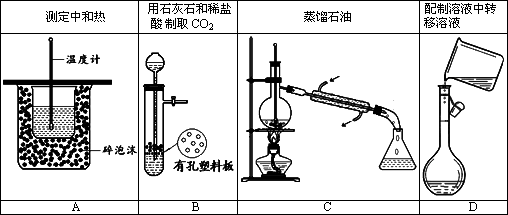
查看答案和解析>>
科目: 来源:广东省2009届高三化学各地名校月考试题汇编-实验基础(2) 题型:013
|
设计下列实验方案鉴别Na2CO3和NaHCO3两种白色粉末,不能达到预期目的的是 | |
| [ ] | |
A. |
分别向等量的白色粉末中加等体积、等浓度的稀盐酸,比较生成气体的快慢 |
B. |
分别向等量的白色粉末中加等体积适量的水,比较固体溶解量的多少 |
C. |
分别将等量的白色粉末配成溶液,然后加入澄清石灰水,比较是否有沉淀生成 |
D. |
分别将等量的白色粉末加热,将产生的气体分别通入澄清石灰水,比较澄清石灰水是否变混浊 |
查看答案和解析>>
科目: 来源:广东省2009届高三化学各地名校月考试题汇编-实验基础(1) 题型:013
|
某同学拟用“甲醛法”测定工业产品中氯化铵的纯度(假定杂质不与甲醛反应)反应为:4NH4Cl+6HCHO→(CH2)6N4+4HCl+6H2O,称取1.5 g该样品溶于水,加入足量的甲醛并加水配成100 mL溶液.从中取出10 mL,滴入酚酞再用0.1 mol/L的NaOH溶液滴定,到滴定终点时消耗NaOH溶液25.00 mL,该样品中氯化铵的质量分数为: | |
| [ ] | |
A. |
8.92% |
B. |
89.2% |
C. |
85.6% |
D. |
92.3% |
查看答案和解析>>
科目: 来源:广东省2009届高三化学各地名校月考试题汇编-实验基础(1) 题型:013
|
下列各溶液中的离子可能大量共存的是 | |
| [ ] | |
A. |
滴加无色酚酞后仍为无色的溶液:Na+、CO32-、K+、ClO-、SO42- |
B. |
由水电离的c(OH-)=10-14 mol·L-1的溶液:CH3COO-、SO42-、Na+、K+ |
C. |
含有大量NO3-的溶液:SO42-、Fe2+、H+、Cl- |
D. |
加入铝粉后产生大量氢气的溶液:NH4+、Na+、NO3-、Cl-、SO42- |
查看答案和解析>>
科目: 来源:广东省2009届高三化学各地名校月考试题汇编-实验基础(1) 题型:013
|
“绿色化学实验”进课堂,某化学教师为“氯气与金属钠反应”设计了如下装置与操作以替代相关的课本实验.实验操作:钠与氯气反应的装置可作如下图改进,将一根玻璃管与氯气发生器相连,玻璃管内放一块黄豆粒大的金属钠(已吸净煤油),玻璃管尾部塞一团浸有NaOH溶液的棉花球.先给钠预热,到钠熔融成圆球时,撤火,通入氯气,即可见钠着火燃烧,生成大量白烟.以下叙述错误的是
| |
| [ ] | |
A. |
反应生成的大量白烟是氯化钠晶体 |
B. |
玻璃管尾部塞一团浸有NaOH溶液的棉球是用于吸收过量的氯气,以免其污染空气 |
C. |
钠着火燃烧产生苍白色火焰 |
D. |
若在棉球外沿滴一滴淀粉碘化钾溶液,可据其颜色变化判断氯气是否被碱液完全吸收 |
查看答案和解析>>
科目: 来源:广东省2009届高三化学各地名校月考试题汇编-溶解平衡与溶解度 题型:013
|
已知25℃时,电离常数Ka(HF)=3.6×10-4 mol·L-1,溶度积常数KSP(CaF2)=1.46×10-10 mol3·L-3.现向1 L 0.2 mol·L-1HF溶液中加入1 L 0.2 mol·L-1CaCl2溶液,则下列说法中,正确的是 | |
| [ ] | |
A. |
25℃时,0.1 mol·L-1HF溶液中pH=1 |
B. |
KSP(CaF2)随温度和浓度的变化而变化 |
C. |
该体系中KSP(CaF2)= |
D. |
该体系中有CaF2沉淀产生 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com