
科目: 来源:湖南省长郡中学2009届高三第五次月考化学试题湘教版 湘教版 题型:013
|
在恒压密闭容器M(如图Ⅰ)和恒容密闭容器N(如图Ⅱ)中,分别加入a molA和a molB,起始时两容器体积均为L,发生如下反应并达到化学平衡状态:2A(?)+B(?)
| |
| [ ] | |
A. |
x=5 |
B. |
若N中气体的密度如图Ⅲ所示,则A、B都是气态 |
C. |
若A为气体,B为非气体,则平衡时M、N中C的物质的量相等 |
D. |
若A、B均为气体,平衡时M中A的转化率小于N中A的转化率 |
查看答案和解析>>
科目: 来源:湖南省长郡中学2009届高三第五次月考化学试题湘教版 湘教版 题型:013
|
某稀溶液中含有Fe(NO3)3.Cu(NO3)2.HNO3,向其中逐渐加入铁粉,溶液中Fe2+的浓度(纵坐标)和加入铁粉的物质的量(横坐标)之间的关系入下图所示,则溶液中Fe(NO3)3.Cu(NO3)2.HNO3物质的量浓度之比为
| |
| [ ] | |
A. |
2∶1∶4 |
B. |
1∶3∶1 |
C. |
3∶3∶8 |
D. |
1∶1∶4 |
查看答案和解析>>
科目: 来源:湖南省长郡中学2009届高三第五次月考化学试题湘教版 湘教版 题型:013
|
按图甲装置进行实验,实验结果如图乙所示.乙中横坐标x表示电路中通过电子的物质的量,纵坐标y表示反应物或生成物的物质的量,下列叙述不正确的是
| |
| [ ] | |
A. |
E表示反应生成铜的物质的量与电路中通过电子的物质的量的关系 |
B. |
E表示反应消耗水的物质的量与电路中通过电子的物质的量的关系 |
C. |
F表示反应生成氧气的物质的量与电路中通过电子的物质的量的关系 |
D. |
F表示反应生成硫酸的物质的量与电路中通过电子的物质的量的关系 |
查看答案和解析>>
科目: 来源:湖北省武汉市武昌区2009届高三元月调研考试化学试题 题型:013
|
向含有1 mol HCl和1 mol MgSO4的混合溶液中加入1 mol/L Ba(OH)2溶液.下列图象能正确表示产生沉淀的物质的量(n)与加入溶液的体积(V)之间关系的是 | |
| [ ] | |
A. |
|
B. |
|
C. |
|
D. |
|
查看答案和解析>>
科目: 来源:湖北省武汉市武昌区2009届高三元月调研考试化学试题 题型:013
|
常温下,0.1 mol/L KCl溶液和0.1 mol/L CH3COOK溶液各100 mL,两溶液中所含离子总数 | |
| [ ] | |
A. |
一样多 |
B. |
KCl溶液中多 |
C. |
CH3COOK溶液中多 |
D. |
无法比较 |
查看答案和解析>>
科目: 来源:黑龙江哈尔滨九中2009届高三上学期第五次月考化学试题 题型:013
|
今有一混合物的水溶液,只可能含有以下离子中的若干种:K+、NH4+、Cl-、Mg2+、Ba2+、CO32-、SO42-,分别取三份各100 mL溶液进行如下实验: (1)第一份加入AgNO3溶液有沉淀产生 (2)第二份加足量NaOH溶液加热后,收集到气体0.04 mol (3)第三份加足量BaCl2溶液后,得干燥沉淀6.27 g,经足量盐酸洗涤、干燥后,沉淀质量为2.33 g.根据上述实验,以下推测正确的是: | |
| [ ] | |
A. |
K+一定存在 |
B. |
Cl-一定存在 |
C. |
100 mL溶液中含0.01 mol CO32- |
D. |
Ba2+一定不存在,Mg2+可能存在 |
查看答案和解析>>
科目: 来源:黑龙江哈尔滨九中2009届高三上学期第五次月考化学试题 题型:013
向一定量的K2CO3溶液中缓慢滴加稀盐酸,并不断搅拌.随着盐酸的加入,溶液中离子数目也相应地发生变化.如图所示,四条曲线与溶液中的离子的对应关系,完全正确的是________.
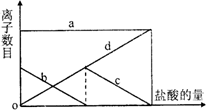
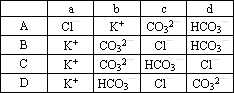
查看答案和解析>>
科目: 来源:黑龙江哈尔滨九中2009届高三上学期第五次月考化学试题 题型:013
|
图中,两电极上发生的电极反应为:a极:Cu2++2e-=Cu b极:Fe-2e-=Fe2+,下列说法中不正确的是
| |
| [ ] | |
A. |
该装置可能是电解池 |
B. |
a极上一定发生还原反应 |
C. |
a、b可能是同种电极材料 |
D. |
该过程中能量的转换一定是化学能转化为电能 |
查看答案和解析>>
科目: 来源:广东省2009届高三化学各地名校月考试题汇编-碳硅及其化合物 题型:013
|
往含0.2 mol KOH和0.1 mol Ca(OH)2的溶液中持续地通入CO2气体,当通入气体的体积为6.72 L(标准状况)时立即停止,则在这一过程中,溶液中离子的物质的量n和通入CO2的体积V的关系示意图正确的是(气体的溶解忽略不计): | |
| [ ] | |
A. |
|
B. |
|
C. |
|
D. |
|
查看答案和解析>>
科目: 来源:广东省2009届高三化学各地名校月考试题汇编-实验探究(1) 题型:013
|
时钟反应或振荡反应提供了迷人课堂演示实验,也是一个活跃的研究领域.测定含I-浓度很小的碘化物溶液时,利用振荡反应进行化学放大,以求出原溶液中碘离子的浓度.主要步骤如是: ①在中性溶液中,用溴将试样中I-氧化成IO3-,将过量的溴除去. ②再加入过量的KI,在酸性条件下,使IO3-完全转化成I2. ③将②中生成的碘完全萃取后,用肼将其还原成I-,方程式为:N2H4+2I2=4I-+N2+4H+ ④将生成的I-萃取到水层后用①法处理. ⑤将④得到的溶液加入适量的KI溶液,并用硫酸酸化. ⑥将⑤反应后的溶液以淀粉作指示剂,用Na2S2O3标准溶液滴定,方程式为:2Na2S2O3+I2=Na2S4O6+2NaI 经过上述放大后,溶液中I-浓度放大为原溶液中I-浓度的(设前后溶液体积相等) | |
| [ ] | |
A. |
2倍 |
B. |
4倍 |
C. |
36倍 |
D. |
6倍 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com