
科目: 来源:江西省南昌三中2011届高三第六次月考化学试题 题型:013
|
今有两种正盐的稀溶液,分别是a mol/L NaX溶液和b mol/L NaY溶液,下列说法不正确的是 | |
| [ ] | |
A. |
若a=b,pH(NaX)>pH(NaY),则相同浓度时,酸性HX<HY |
B. |
若a=b,并测得c(X-)=c(Y-)+c(HY),则相同浓度时,酸性HX>HY |
C. |
若a>b,测得c(X-)=c(Y-),则可推出溶液中c(HX)>c(HY),且相同浓度时,酸性HX<HY |
D. |
若两溶液等体积混合,测得c(X-)+c(Y-)+c(HX)+c(HY)=0.1 mol/L,则可推出a=b=0.1 mol/L |
查看答案和解析>>
科目: 来源:江西省南昌三中2011届高三第六次月考化学试题 题型:013
|
化合物A、B、C、D各由两种元素组成,甲、乙、丙是三种单质.这些常见的化合物与单质之间存在如下关系(已知化合物C是一种有机物),
以下结论不正确的是 | |
| [ ] | |
A. |
甲、乙、丙三种单质全是非金属 |
B. |
上述转化关系所涉及的化合物中有一种是电解质 |
C. |
上图所示的五个转化关系中,有三个是化合反应 |
D. |
上图所示的五个转化关系中,均为放热反应 |
查看答案和解析>>
科目: 来源:江西省南昌三中2011届高三第六次月考化学试题 题型:013
|
一定温度下可逆反应:A(s)+2B(g)
| |
| [ ] | |
A. |
保持温度和活塞位置不变,在甲中再加入1 mol A和2 mol B,达到新的平衡后,甲中C的浓度是乙中C的浓度的2倍 |
B. |
保持活塞位置不变,升高温度,达到新的平衡后,甲中B的体积分数均增大,乙则减小 |
C. |
保持温度不变,移动活塞P,使乙的容积和甲相等,达到新的平衡后,乙中C的体积分数是甲中C的体积分数的2倍 |
D. |
保持温度和乙中的压强不变,t2时分别向甲、乙中加入等质量的氦气后,甲、乙中反应速率变化情况分别如图1和图2所示(t1前的反应速率变化已省略)
|
查看答案和解析>>
科目: 来源:江西省南昌三中2011届高三第六次月考化学试题 题型:013
|
下列叙述中完全正确的一组是 ① 常温常压下,1 mol甲基(-CH3)所含的电子数为10NA②由Cu、Zn和稀硫酸组成的原电池工作时,若Cu极生成0.2 g H2,则电路通过电子0.2NA ③在标准状况下,11.2 L NO与11.2 L O2混合后气体分子数为0.75NA ④常温常压下,16 g O3所含的原子数为NA ⑤1 mol C10H22分子中共价键总数为31NA ⑥1 mol Cl2发生反应时,转移的电子数一定是2 NA ⑦标准状况下,22.4 L水中含分子数为NA | |
| [ ] | |
A. |
①②③④⑤ |
B. |
②③④⑤⑥ |
C. |
②④⑤ |
D. |
②③④⑤ |
查看答案和解析>>
科目: 来源:江西省南昌三中2011届高三第六次月考化学试题 题型:013
|
下列反应的离子方程式中正确的是 | |
| [ ] | |
A. |
甲醇、氧气和氢氧化钾溶液组成的燃料电池的负极反应 CH3OH+H2O-6e- |
B. |
在NaHSO4溶液中加Ba(OH)2至中性 H++SO42-+Ba2++OH- |
C. |
苯酚钠的水溶液中通入少量的CO2 2C6H5Oˉ+CO2+H2O→2C6H5OH+CO32- |
D. |
用 侯氏制碱法制得NaHCO3Na++NH3+CO2+H2O |
查看答案和解析>>
科目: 来源:江西省南昌三中2011届高三第六次月考化学试题 题型:013
|
已知热化学方程式 2SO2(g)+O2(g)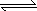 2SO3(g) ΔH=-Q kJ/mol(Q>0),则下列说法正确的是 2SO3(g) ΔH=-Q kJ/mol(Q>0),则下列说法正确的是
| |
| [ ] | |
A. |
2 mol SO2(g) 和1 mol O2(g)所具有的能量小于2 mol SO3(g)所具有的能量 |
B. |
将 2 mol SO2(g)和1 mol O2(g)置于一密闭容器中充分反应后放出QKJ的热量 |
C. |
升高温度,平衡向逆反应移动,上述热化学方程式中的Q值将减小 |
D. |
如将一定量SO2(g)和O2(g)置于某密闭容器中充分反应后放热QKJ,则此过程中有2 mol SO2(g)被氧化 |
查看答案和解析>>
科目: 来源:江西省南昌三中2011届高三第六次月考化学试题 题型:013
|
Na2O2、CaC2、CaH2、Mg3N2都能与水反应,且反应中均有气体放出.下列说法中正确的是 | |
| [ ] | |
A. |
都属于氧化还原反应 |
B. |
Na2O2与水反应时水作氧化剂 |
C. |
CaC2、Mg3N2、CaH2与水反应属复分解反应 |
D. |
CaH2与水反应时产生H2,它既是氧化产物又是还原产物 |
查看答案和解析>>
科目: 来源:江西省南昌三中2011届高三第六次月考化学试题 题型:013
|
绿色化学己成为当前化学研究的热点和前沿,旨在从源头上消除污染,实现经济和社会可持续发展.而常温离子液体(ionic liquid)(也有称常温熔融盐)以其优异的理化特性最有可能使上述理想变为现实.1914年报道的第一种离子液体硝酸乙基铵[(C2H5NH3)NO3]离子液体其熔点为12℃.已知C2H5NH2结合质子的能力比NH3略强,下列有关硝酸乙基铵的说法正确的是 | |
| [ ] | |
A. |
离子液体可以作为电池的电解质 |
B. |
硝酸乙基铵水溶液呈碱性 |
C. |
硝酸乙基铵水解的离子方程式或表示为:C2H5NH3++H2O |
D. |
同温度下相同物质的量浓度的硝酸乙基铵溶液和硝酸铵溶液前者的pH值小 |
查看答案和解析>>
科目: 来源:福建省泉州一中2011届高三上学期期末考试化学试题 题型:013
|
25℃时,有关弱酸的电离平衡常数如下:
下列有关说法正确的是 | |
| [ ] | |
A. |
等物质的量浓度的各溶液pH关系为:CH3COONa>Na2CO3>NaCN |
B. |
a mol/L NaOH溶液与b mol/L HCN溶液等体积混合后,所得溶液中c(Na+)>c(CN-),则a一定大于b |
C. |
在冰醋酸中逐滴加水,则溶液的导电性和醋酸的电离程度均先增大后减小 |
D. |
NaHCO3和Na2CO3混合溶液中,一定存在c(Na+)+c(H+)=c(OH-)+c(HCO |
查看答案和解析>>
科目: 来源:福建省泉州一中2011届高三上学期期末考试化学试题 题型:013
|
下列叙述正确的是 | |
| [ ] | |
A. |
0.1 mol·L-1 NH4Cl溶液:c(NH |
B. |
pH=4的盐酸与pH=10的氨水溶液等体积混合后pH>7 |
C. |
0.1 mol·L-1与0.2 mol·L-1氨水溶液中c(OH-)之比为1∶2 |
D. |
中和pH与体积都相同的氨水和Ba(OH)2溶液,消耗HCl的物质的量之比是1∶2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com