相关习题
0 95353 95361 95367 95371 95377 95379 95383 95389 95391 95397 95403 95407 95409 95413 95419 95421 95427 95431 95433 95437 95439 95443 95445 95447 95448 95449 95451 95452 95453 95455 95457 95461 95463 95467 95469 95473 95479 95481 95487 95491 95493 95497 95503 95509 95511 95517 95521 95523 95529 95533 95539 95547 203614
科目:
来源:2007届电海中学高三第一次月考测试卷、化学(人教) 人教
题型:022
|
|
已知 可简写为 可简写为
降冰片烯的分子结构可表示为: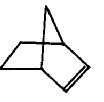
| (1) |
|
降冰片烯属于________.
a.环烃
b.不饱和烃
c.烷烃
d.芳香烃
|
|
(2) |
|
(3) |
|
降冰片烯的一种同分异构体(含有一个六元环的单环化合物)的结构简式为________.
|
|
(4) |
|
降冰片烯不具有的性质________.
a.能溶于水
b.能发生氧化反应
c.能发生加成反应
d.常温常压下为气体
|
|
|
查看答案和解析>>
科目:
来源:2007届电海中学高三第一次月考测试卷、化学(人教) 人教
题型:022
|
|
稀薄燃烧是指汽油在较大空/燃比(空气与燃油气的体积比)条件下的燃烧.随着全球能源危机的加剧,稀薄燃烧技术的研究受到了人们的重视,但稀薄燃烧时,常用的汽车尾气净化装置不能有效地将NOx转化为N2.不同空/燃比时汽车尾气中主要污染物的含量变化如右图所示.

| (1) |
|
稀薄燃烧技术除能节约能源外,还具有的优点是________(填一项).排放到大气中的NOx会导致酸雨、________等环境问题(填一项).
|
|
(2) |
|
某校化学研究性学习小组的同学在技术人员的指导下,按下列流程探究不同催化剂对NH3还原NO反应的催化性能.
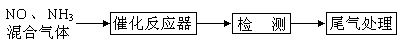
若控制其他实验条件均相同,在催化反应器中装载不同的催化剂,将经催化反应后的混合气体通过滴有酚酞的稀硫酸溶液(溶液的体积、浓度均相同).为比较不同催化剂的催化性能,需要测量并记录的数据是________.
|
|
(3) |
|
若某一催化剂能同时催化NH3等还原性气体与的反应NOx的反应.将该催化剂分别用于催化还原含等物质的量NOx的两种气体:①纯NO气体,②汽车尾气.消耗的物质的量较多的可能是________(填字母),原因是________
|
|
|
查看答案和解析>>
科目:
来源:2007届电海中学高三第一次月考测试卷、化学(人教) 人教
题型:022
(1)化学平衡常数K表示可逆反应的进行程度,K值越大,表示________,K值大小与温度的关系是:温度升高,K值________(填一定增大、一定减小、或可能增大也可能减小).
(2)在一体积为10L的容器中,通人一定量的CO和H2O,在850℃时发生如下反应:CO(g)十H2O(g) CO2(g)十H2(g)十Q(Q>0)
CO和H2O浓度变化如下图,则0-4min的平均反应速率v(CO)=________mol/(L·min)

(3)t℃(高于850℃)时,在相同容器中发生上述反应,容器内各物质的浓度变化如上表.
①表中3min-4min之间反应处于________状态;C1数值________0.08mol/L(填大于、小于或等于).
②反应在4min-5min问,平衡向逆方向移动,可能的原因是________(单选),
表中5min-6min之间数值发生变化,可能的原因是________(单选).
a.增加水蒸气
b.降低温度
c.使用催化剂
d.增加氢气浓度
查看答案和解析>>
科目:
来源:2007届电海中学高三第一次月考测试卷、化学(人教) 人教
题型:022
|
|
下表中的实线表示元素周期表的部分边界.①-⑤分别表示元素周期表中对应位置的元素.

| (1) |
|
(2) |
|
元素⑤的原子核外p电子数比s电子总数多________个.元素③氢化物的电子式为________.
|
|
(3) |
|
元素④—般在化合物中显________价,但与________形成化合物时,所显示的价态则恰好相反.
|
|
(4) |
|
在元素①的单质、元素②的单质和元素①②形成的合金这三种物质中,熔点最低的是________.
a.元素①的单质b.元素②的单质c.元素①②形成的合金d.无法判断
|
|
|
查看答案和解析>>
科目:
来源:2007届电海中学高三第一次月考测试卷、化学(人教) 人教
题型:022
|
(1) |
|
蛇纹石矿可以看作由MgO、Fe2O3、Al2O3、SiO2组成.由蛇纹石制取碱式碳酸镁的实验步骤如下

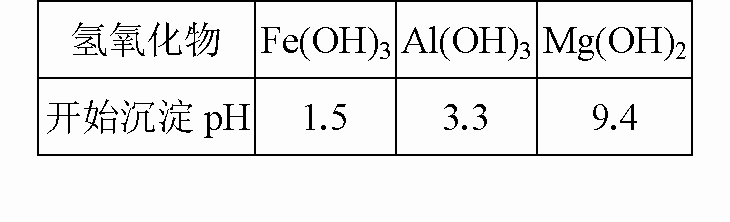
|
|
(2) |
|
进行Ⅰ操作时,控制溶液pH=7-8(有关氢氧化物沉淀的pH见右表)Ca(OH)2不能过量,若Ca(OH)2过量可能会导致________溶解、________沉淀.
|
|
(3) |
|
从沉淀混合物A中提取红色氧化物作颜料,先向沉淀物A中加入________(填入物质的化学式),然后________(依次填写实验操作名称).
|
|
(4) |
|
物质循环使用,能节约资源.上述实验中,可以循环使用的物质是________(填写物质化学式).
|
|
(5) |
|
现设计一个实验,确定产品aMgCO3·bMg(OH)2·cH2O中a、b、c的值,请完善下列实验步骤(可用试剂:浓硫酸、碱石灰):
①样品称量;②高温分解;③________;④________;⑤MgO称量
|
|
(6) |
|
18.2g产品完全分解后,产生6.6gCO2和8.0gMgO,由此可知,产品的化学式中:a=________b=________C=________
|
|
|
查看答案和解析>>
科目:
来源:2007届道县高考文化补习学校第四次周考试题、化学
题型:022
|
|
已知A、B、C、D均为短周期元素,它们的原子序数依次递增.A单质是自然界中密度最小的气体,C原子的最外层电子数是次外层的3倍;C和D可形成两种固态化合物,其中一种为淡黄色固体;B和C可形成多种气态化合物.A、B、C三种元素可以形成离子晶体,该晶体可以和氢氧化钠反应放出无色刺激性气味气体E.请回答下列问题:
| (1) |
|
写出B单质的电子式________;C和D形成淡黄色固体化合物电子式________.
|
|
(2) |
|
元素原子的物质的量之比为A∶B∶C=4∶2∶3的晶体名称为________其水溶液显________性,用离子方程式说明________.
|
|
(3) |
|
E分子的空间构型是________,属于________分子(填极性或非极性)
|
|
(4) |
|
A、B、C三种元素还可以形成另一种化合物,其热的浓溶液可以溶解铝和铁,但常情况下它的浓溶液又可盛放在铝或铁制的容器中,原因是________.
|
|
|
查看答案和解析>>
科目:
来源:2007届道县高考文化补习学校第四次周考试题、化学
题型:022
|
|
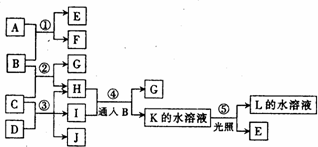
根据下列反应框图填空.已知B、D、E、L常温下为密度比空气大的气体,D、E为单质,其它为化合物.A是一种淡黄色固体,C在水中的溶解度随温度的升高而减小,F、G均能与L的水溶液反应放出B.
| (1) |
|
F的俗名是________,工业上利用反应③生产________.
|
|
(2) |
|
反应①棦葜校?粲谘趸?乖?从Φ氖—________.
|
|
(3) |
|
(4) |
|
有一种单质能与H反应生成E,该反应的化学方程式为________.
|
|
(5) |
|
某气体M具有漂白性,既有氧化性,又有还原性,请写出同时有B、H和M生成的化学方程式________.
|
|
|
查看答案和解析>>
科目:
来源:2007届道县高考文化补习学校第四次周考试题、化学
题型:022
|
|
二氧化氯(ClO2)作为替代传统多氯漂白工艺的最佳漂白剂、消毒杀菌剂和水处理剂,其生产和应用有着广阔的前景.ClO2在常温下是一种黄绿色气体;在酸性溶液中比较稳定;在碱性溶液中迅速生成ClO2-和ClO3-混合物.
| (1) |
|
ClO2起消毒杀菌作用是利用了它具有________的化学性质,生成物中氯元素呈________价.
|
|
(2) |
|
写出ClO2与NaOH溶液反应的化学方程式________.若有0.1molClO2参加反应,则转移的电子的物质的量为________mol
|
|
(3) |
|
国际上关ClO2生产工艺和制备方法的研究一直很活跃,仅成型的生产工艺就有十几种之多,其中有一种是用NaClO3和NaCl为原料,反应必须在酸性溶液中进行.现仍用NaClO3为原料,只需加入另一种原料即可,请完成这一化学反应方程式:
□NaClO3+□ →□ClO2↑+□Cl2↑+□NaCl+□ →□ClO2↑+□Cl2↑+□NaCl+□
|
|
|
查看答案和解析>>
科目:
来源:2007届道县高考文化补习学校第四次周考试题、化学
题型:022
|
|
我们知道自然界中的蜘蛛丝和细菌纤维素纤维是典型的纳米纤维.较细的蜘蛛丝直径还不足100纳米,是真正的天然纳米纤维.美国与加拿大的科学家合作,采用蜘蛛基因,利用仿生结构,成功地纺制出人造蜘蛛丝,其强韧性能优于钢材.
| (1) |
|
纳米纺织材料凭借其内部所特有的小尺寸效应、表面效应等日益受到广大消费者的
喜爱.许多纳米材料的粒子直径都在1~100nm之间,从分散系的角度看应该属于________
|
|
(2) |
|
纳米是长度单位,物质的颗粒达到纳米级时,具有不同的性质,如果单质铜制成“纳米铜”时,具有非常强的化学活性,在空气中可以燃烧,下列对“纳米铜”的说法正确的是:________(填序号)
|
| [ ] |
A. |
“纳米铜”与铜片还原性相同
|
B. |
“纳米铜”比铜片更易失电子
|
C. |
“纳米铜”比铜片的氧化性强
|
|
(3) |
|
钢铁在人们生活中应用非常广泛,但是钢铁因腐蚀造成的损失全球每年高达7000亿美元,目前钢铁被腐蚀的主要形式是吸氧腐蚀,其正极发生________反应,负极发生的电极反应式为________.为了减少这种腐蚀生产生活中常见的有哪些防腐措施:________.(至少填两种措施)
|
|
|
查看答案和解析>>
科目:
来源:2007届道县高考文化补习学校第四次周考试题、化学
题型:022
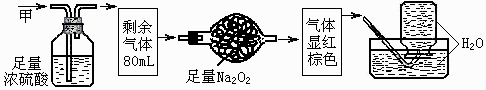
无色的混合气体甲,可能含NO、CO2、NO2、NH3、N2中的几种,将100mL甲气体经过下图实验的处理,结果得到酸性溶液,而几乎无气体剩余,则甲气体的组成为________
查看答案和解析>>


