相关习题
0 95418 95426 95432 95436 95442 95444 95448 95454 95456 95462 95468 95472 95474 95478 95484 95486 95492 95496 95498 95502 95504 95508 95510 95512 95513 95514 95516 95517 95518 95520 95522 95526 95528 95532 95534 95538 95544 95546 95552 95556 95558 95562 95568 95574 95576 95582 95586 95588 95594 95598 95604 95612 203614
科目:
来源:浙江省杭州第二中学2006-2007学年度高三化学11月月考试卷
题型:022
向50mL0.018mol/L的AgNO3溶液中加入50mL0.02mol/L的盐酸生成沉淀,如果溶液中[Ag+][Cl-]的乘积是一个常数,且[Ag+][Cl-]=1.0×10-10(mol/L)2,则沉淀生成后溶液中[Ag+]=________;溶液的PH值=________.
查看答案和解析>>
科目:
来源:浙江省杭州第二中学2006-2007学年度高三化学11月月考试卷
题型:022
|
|
下表列出了前20号元素中的某些元素性质的有关数据:
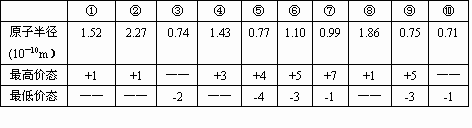
试回答下列问题:
| (1) |
|
以上10种元素的原子中,失去核外第一个电子所需能量最少的是________(填写编号).
|
|
(2) |
|
上述⑤、⑥、⑦三种元素中的某两种元素形成的化合物中,每个原子都满足最外层为8电子稳定结构的物质可能是________(写分子式).某元素R的原子半径为1.02×10—10m,该元素在周期表中的位置是________;若物质Na2R2是一种含有非极性共价键的离子化合物,请你写出该化合物的电子式________.
|
|
(3) |
|
元素⑤的某种单质具有平面层状结构,同一层中的原子构成许许多多的正六边形,此单质与熔融的②单质相互作用,形成某种青铜色的物质(其中的元素②用“●”表示),原子分布如图所示,该物质的化学式为________.

|
|
|
查看答案和解析>>
科目:
来源:浙江省杭州第二中学2006-2007学年度高三化学11月月考试卷
题型:022
|
|
铝和氢氧化钾都是重要的工业产品.请回答:
| (1) |
|
(2) |
|
铝与氢氧化钾溶液反应的离子方程式是________.
|
|
(3) |
|
工业品氢氧化钾的溶液中含有某些含氧酸根杂质,可用离子交换膜法电解提纯.电解槽内装有阳离子交换膜(只允许阳离子通过),其工作原理如图所示.
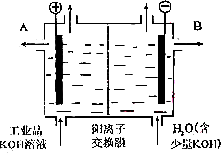
①该电解槽的阳极反应式是________.
②通电开始后,阴极附近溶液pH会增大,请简述原因________
③除去杂质后的氢氧化钾溶液从液体出口________(填写“A”或“B”)导出.
|
|
|
查看答案和解析>>
科目:
来源:浙江省杭州第二中学2006-2007学年度高三化学11月月考试卷
题型:022
|
|
铅蓄电池是典型的可充型电池,它的正负极格板是惰性材料,电池总反应式为:Pb+PbO2+4H++2SO2-4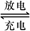 2PbSO4+2H2O请回答下列问题(不考虑氢、氧的氧化还原): 2PbSO4+2H2O请回答下列问题(不考虑氢、氧的氧化还原):
| (1) |
|
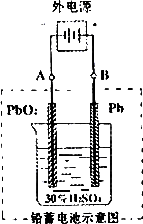
放电时:正极的电极反应式是________;电解液中H2SO4的浓度将变________;当外电路通过1mol电子时,理论上负极板的质量增加________g.
|
|
(2) |
|
在完全放电耗尽PbO2和Pb时,若按右图连接,电解一段时间后,则在A电极上生成________、B电极上生成________,此时铅蓄电池的正负极的极性将________.
|
|
|
查看答案和解析>>
科目:
来源:浙江省东阳中学、义乌中学、兰溪一中2007届高三期中联考试卷、化学试题
题型:022
|
|
已知C12和NO2在一定条件下可以化合成一种气态化合物A.为了测定A的组成进行如下实验:(不考虑2NO2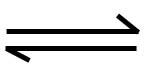 N2O4的平衡) N2O4的平衡)
| (1) |
|
当C12与NO2混合气体以不同比例混合时,测得其平均式量分别为51和6l,分别求出C12在上述混合气体中的体积分数.
|
|
(2) |
|
取上述不同比例的混合气体各5L,在一定条件下充分反应后,气体体积均为4L,由此写出C12和NO2反应的化学方程式.
|
|
(3) |
|
设C12的体积分数为x(0<x<1),试讨论当x的取值范围不同时(C12与NO2的总体积为5L),反应后的总体积V随x变化的函数关系,将结果填入下表.

|
|
|
查看答案和解析>>
科目:
来源:浙江省东阳中学、义乌中学、兰溪一中2007届高三期中联考试卷、化学试题
题型:022
|
|
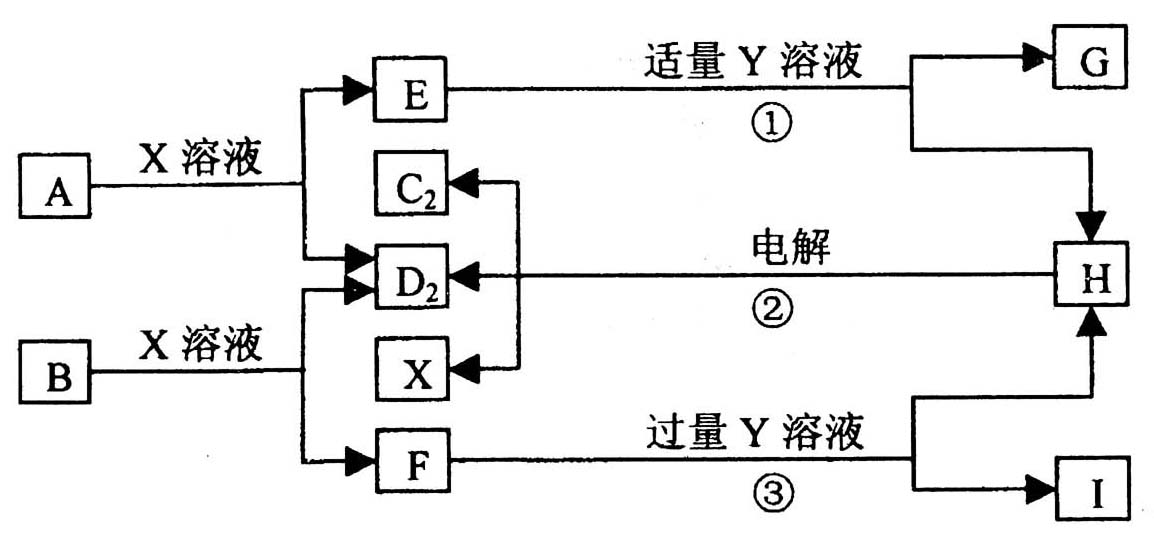
位于短周期的原子序数依次增大的D、A、B、C四种元素(其中一种是金属),它们的单质在通常情况下,A、B是固体.C2、D2是常见的双原子气体单质,另有X溶液和Y溶液.这些物质相互转化的关系如下图所示,图中G、I均为白色胶状沉淀,F是含B元素的盐.电解H的水溶液生成C2、D2和X溶液,这是一种重要的化工生产原理.
| (1) |
|
X、Y的化学式分别为________、________.
|
|
(2) |
|
(3) |
|
(4) |
|
写出反应①、③的离子方程式:
反应①:________.
反应③:________.
|
|
|
查看答案和解析>>
科目:
来源:浙江省东阳中学、义乌中学、兰溪一中2007届高三期中联考试卷、化学试题
题型:022
|
|
A、B、C、D均为常见的短周期元素,常温下A、B可形成两种常见的液态化合物,其最简式分别为BA和B2A、B与D可形成分子X,也可形成阳离子Y,X和Y在水溶液中酸碱性正好相反,C 的焰色反应呈黄色. 的焰色反应呈黄色.
| (1) |
|
C元素在周期表中的位置是________,液态X类似B2A也能微弱电离产生电子数相同的两种离子,则液态x的电离方程式:________.
|
|
(2) |
|
M、N是由A、B、C、D四种元素中任意三种元素组成的不同类型的强电解质,M的水溶液呈碱性,N的水溶液呈酸性,且M溶液中水的电离程度小于N溶液中水的电离程度.则M、N分别为________(填化学式).若将0.1m01.L 1M和0.2mol.L 1M和0.2mol.L 1N两溶液等体积混和所得溶液中离子浓度的大小顺序________. 1N两溶液等体积混和所得溶液中离子浓度的大小顺序________.
|
|
|
查看答案和解析>>
科目:
来源:浙江省东阳中学、义乌中学、兰溪一中2007届高三期中联考试卷、化学试题
题型:022
|
|
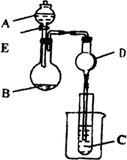
用下图装置进行实验,将A逐滴加入B中:
| (1) |
|
若A为浓H2SO4,B为第三周期金属元素的片状单质,其在常温下难与水反应;C为品红溶液,实验中观察到C中溶液褪色,则B是________(填化学式),B与浓H2SO4反应的化学方程式为________.反应后往烧杯中加入沸水,又可观察到试管C中的现象为________.
|
|
(2) |
|
若B为KMnO4晶体,C为品红溶液,实验中观察到C中溶液褪色,则B中发生反应的化学方程式是________.然后往烧杯中加入沸水,试管C中的现象是________.
|
|
(3) |
|
若B是生石灰,实验中观察到C溶液从无色变红色,则A是________,C是________仪器D在此实验中的作用是________.
|
|
|
查看答案和解析>>
科目:
来源:浙江省东阳中学、义乌中学、兰溪一中2007届高三期中联考试卷、化学试题
题型:022
|
|
请按要求填空:
| (1) |
|
指出下列实验用品或仪器(已经洗涤干净)使用时的第一步操作:
①石蕊试纸(检验气体性质)________;
②容量瓶________.
|
|
(2) |
|
当NaHCO3溶液中混有Na2CO3,为除去Na2CO3可以通入________,化学方程式为________.
|
|
(3) |
|
BaSO4中混有AgCl可通过加入________使AgCl转化为可溶的________除去.
|
|
|
查看答案和解析>>
科目:
来源:浙江省东阳中学、义乌中学、兰溪一中2007届高三期中联考试卷、化学试题
题型:022
查看答案和解析>>

![]() 、SO2
、SO2![]() -4、Fe3+、H+、M,其物质的量之比为:n(NO
-4、Fe3+、H+、M,其物质的量之比为:n(NO![]() ):n(SO2
):n(SO2![]() 4):n(Fe3+):n(H
4):n(Fe3+):n(H![]() ):n(M)=2︰3︰1︰3︰1,则M可能是
):n(M)=2︰3︰1︰3︰1,则M可能是