
科目: 来源:江苏省高淳高级中学2008届高三质量检测化学试卷 题型:022
下图是元素周期表中的一部分,表中所列字母分别代表一种化学元素,请回答下列问题:

(1)上述所列元素的原子中,最外层电子层上只有两个电子的是________(填“元素符号”);
(2)下列叙述正确的是________(填字母序号);
a.K的最高价氧化物对应的水化物是一种强碱
b.硒化氢的稳定性强于H的氢化物的热稳定性
c.F与H形成化合物水溶液的pH大于F与I形成化合物水溶液的pH,说明相同浓度氢化物水溶液的酸性H弱于I
d.MA2E分子中M原子采取SP2杂化方式
e.N的电子排布式:ls22s22p63s23p63d44s2
(3)根据VSEPR理论预测DA4+离子的空间构型________,ME2的空间构型________;
(4)元素F和元素I形成的化合物是________晶体(填晶体类型),下图为该晶体的结构示意图,请在图中用实心球(●)和空心球(○)分别表示元素F和元素I所在位置.

(5)已知Ti3+可形成配位数为6的配合物.现有含钛的两种颜色的晶体,一种为紫色,另一为绿色,相关实验证明,两种晶体的组成皆为TiCl3·6H2O.为测定这两种晶体的化学式,设计了如下实验:
a.分别取等质量的两种配合物晶体的样品配成待测溶液;
b.分别往待测溶液中滴入AgNO3溶液,均产生白色沉淀;
c.沉淀完全后分别过滤得两份沉淀,经洗涤干燥后称量,发现原绿色晶体的水溶液与AgNO3溶液反应得到的白色沉淀质量为紫色晶体的水溶液反应得到沉淀质量的2/3.
则绿色晶体的化学式为________,该配合物中的配位体为________.
查看答案和解析>>
科目: 来源:江苏省高淳高级中学2008届高三质量检测化学试卷 题型:022
根据下列框图关系填空,已知反应①、③是我国工业生产中的重要反应,X常温下为无色无味透明液体;C焰色反应火焰呈黄色,J为红褐色沉淀;D、E常温下为气体,且E能使品红溶液褪色;A固体中仅含两种元素,其中金属元素的质量分数约为46.7%.
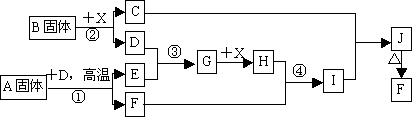
(1)G的化学式为________;
(2)固体A中所包含的化学键与固体B类似,则A的电子式为________;
(3)反应②的离子方程式:________________________________________;
(4)反应④的离子方程式:________________________________________;
(5)已知每生成16 g E,放出106.5 kJ热量,则反应①的热化学方程式为:
___________________________________________________.
查看答案和解析>>
科目: 来源:江苏海门市2008届高三第一次诊断性考试试卷、化学 题型:022
含氮废水进入水体,对环境造成的污染越来越严重.环保专家认为,可以用金属铝将水体中的NO3-还原为N2而消除污染,Al则转变为Al(OH)3.发生的反应为:
6NO3-+10Al+18H2O![]() 3N2↑+10Al(OH)3↓+6OH-
3N2↑+10Al(OH)3↓+6OH-
(1)某水库水的实际容量大约为1×1010 m3,1 m3水体中含N元素4.2 g,假设水中N元素全部以NO3-的形式存在,则转化该水库中的N元素,大约需要多少kg金属铝?
(2)事实证明,金属镁比金属铝能更快的消除水体中N污染,反应原理和金属铝相同.金属镁可由下述方法制得:
![]()
如果用金属镁除去该水库中的N元素,大约需要含MgCl2 0.5%(质量分数)的海水多少kg?
查看答案和解析>>
科目: 来源:江苏海门市2008届高三第一次诊断性考试试卷、化学 题型:022
某种含有少量氧化钠的过氧化钠试样质量为1.56 g,为测定各成分的质量分数,按如图所示,原锥形瓶和水的总质量为190.72,将1.56 g上述样品投入锥形瓶中,充分反应后,电子天平最终的读数为192.12 g.求:
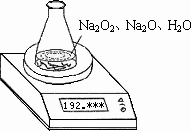
(1)反应中产生的氧气在标准状态下的体积为多少mL?
(2)样品中Na2O和Na2O2的物质的量比为多少?
查看答案和解析>>
科目: 来源:江苏海门市2008届高三第一次诊断性考试试卷、化学 题型:022
已知甲、乙、丙为常见单质,A、B、C、D、E、F、G、X均为常见的化合物;B和X的摩尔质量相同,E的相对分子质量比D的相对分子质量大16,在一定条件下,各物质相互转化关系如下图所示:
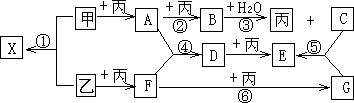
(1)写出X的电子式________;以上物质中具有漂白作用的有(填写化学式)________、________;
(2)以上①②③④⑤⑥的六个转化中,属于化合反应,但不属于氧化还原反应的是(填写编号)________;
(3)写出D→E的化学方程式:________;
(4)同类物质的化学性质具有相似性,也有特殊性.请写出物质B与F反应的可能的化学方程式:________,你这样书写的理由是:_________________________.
查看答案和解析>>
科目: 来源:江苏海门市2008届高三第一次诊断性考试试卷、化学 题型:022
硝酸盐受热分解的产物与硝酸盐的组成以及受热的温度等因素有关.
(1)一定条件下硝酸铵受热分解的化学反应方程式为:
NH4NO3-HNO3+N2+H2O(未配平)
反应中生成的氧化产物是__________;
在反应中被氧化与被还原的氮原子数之比为__________;
反应中若产生0.2 mol N2气体,则转移电子的物质的量是________mol.
(2)某硝酸盐受热分解的产物为不含氮元素的固体物质和NO2、O2气体,若产生NO2和O2的物质的量之比为8∶1,则金属元素的价态在反应过程中________(填“升高”、“降低”、“不变”).
查看答案和解析>>
科目: 来源:江苏海门市2008届高三第一次诊断性考试试卷、化学 题型:022
| |||||||||||||||||||||||||||||||
查看答案和解析>>
科目: 来源:江苏海门市2008届高三第一次诊断性考试试卷、化学 题型:022
铁是人体必须的微量元素,治疗缺铁性贫血的常见方法是服用补铁药物.“速力菲”(主要成分:琥珀酸亚铁,呈暗黄色)是市场上一种常见的补铁药物.该药品不溶于水但能溶于人体中的胃酸.
某同学为了检测“速力菲”药片中Fe2+的存在,设计并进行了如下实验:
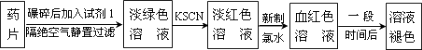
(1)试剂1是________,加入新制氯水后溶液中发生的离子反应方程式是:
____________________,__________________________;
(2)加入KSCN溶液后,在未加新制氯水的情况下,溶液中也产生了红色,其可能的原因是______________________;
(3)在实验中发现放置一段时间,溶液的颜色会逐渐褪去.为了进一步探究溶液褪色的原因,甲、乙、丙三位同学首先进行了猜想:

基于乙同学的猜想,请设计实验方案,验证乙同学的猜想是否正确.写出有关的实验操作、预期现象和结论.(不一定填满,也可以补充)

查看答案和解析>>
科目: 来源:湖南省示范性高级中学衡南一中2008届高三第一次月考、化学 题型:022
(1)肼(N2H4)又称联氨,是一种可燃性的液体,可用作火箭燃料.已知在101 kPa时,32.0 g N2H4在氧气中完全燃烧生成氮气,放出热量624 kJ(25℃时),N2H4完全燃烧反应的热化学方程式是__________________________.
(2)如图是一个电化学过程示意图.
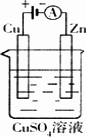
①锌片上发生的电极反应是_________________________
②假设使用肼-空气燃料电池作为本过程中的电源,铜片的质量变化128 g,则肼一空气燃料电池理论上消耗标标准状况下的空气________L(假设空气中氧气体积含量为20%)
(3)传统制备肼的方法,是以NaClO氧化NH3,制得肼的稀溶液.该反应的离子方程式是______________________________________.
(4)1998年希腊亚里斯多德大学的Marnellos和Stoukides采用高质子导电性的SCY陶瓷(能传递H+),实现了高温常压下高转化率的电化学合成氨.其实验装置如图.
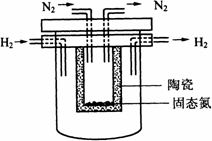
阴极的电极反应式为__________________________________.
查看答案和解析>>
科目: 来源:湖南省示范性高级中学衡南一中2008届高三第一次月考、化学 题型:022
A、B、C、D、E、F、G是由短周期元素组成的七种物质,其中B、C、F是单质;常温下B、C、E为气体;A物质的焰色反应呈黄色.(下图中反应②的部分产物未表示出来.)
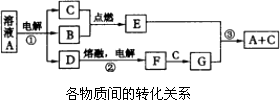
根据上图所示转化关系回答:
(1)经测定G属于离子化合物,其电子式为________.
(2)写反应②的电极反应式:
阳极___________________;阴极_________________________.
(3)反应③的化学方程式为____________________.
(4)这七种物质中含有共价键的有__________________(用化学式回答).
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com