
科目: 来源:湖南省浏阳一中2010届高三第四次月考、化学试卷 题型:022
单质铁溶于一定浓度的硝酸中反应的化学方程式如下:
aFe+bNO3-+cH
+请你用已掌握的知识研究出下列规律.
(1)b、g、h的关系式是________.
(2)b、c、d、f的关系式是________.
(3)d、f、g、h的关系式是________.
查看答案和解析>>
科目: 来源:湖南省衡阳八中2010届高三第四次月考、化学试卷 题型:022
1986年,化学家Karl Christe首次用化学方法制得了F![]() 2.他提出的三步反应如下(反应①、②里氟元素化合价不变):
2.他提出的三步反应如下(反应①、②里氟元素化合价不变):
①KMnO4+KF+H2O2+HF→K2MnF6+________+H2O
②SbCl5+HF→SbF5+________
③2K2MnF6+4SbF5=4KSbF6+2MnF3+F2↑
请根据以上反应回答问题:
(1)反应①中空格上应填物质的化学式为________;
(2)反应③中的氧化剂为________;被氧化的元素为________.
查看答案和解析>>
科目: 来源:湖南省长沙市一中2010届高三第四次月考、化学试卷 题型:022
有①~⑧八种短周期元素,其原子序数依次增大,其中②、⑦、⑧三种元素在周期表中的相对位置如下,且元素②所处主族的位置为所有主族的正中间.
(1)元素②在周期表中的位置为________;②、⑦、⑧三种元素最高价氧化物对应水化物的酸性由强到弱的顺序是________(用化学式表示).
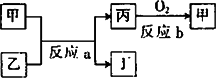
(2)如图所示,甲、乙、丙、丁均为①~⑧中某些元素形成的单质或化合物,反应a为置换反应,反应b为化合反应.单质乙与单质丙所含元素位于同一主族,试写出符合条件的反应a的两个化学方程式:________、________.
查看答案和解析>>
科目: 来源:湖南省长沙市一中2010届高三第四次月考、化学试卷 题型:022
蛋白质是一类复杂的含氮化合物,每种蛋白质都有其恒定的含氮量,食品中蛋白质的含量测定常用凯氏定氮法.其测定原理是:
Ⅰ.蛋白质中的氮(用氨基表示)在强热和CuSO4、浓H2SO4作用下,生成一种无机含氮化合物,反应式为:2(-NH2)+H2SO4+2H+![]() ________
________
Ⅱ.该无机化合物在凯氏定氮器中与碱作用,通过蒸馏释放出NH3,收集于H3BO3溶液中,生成(NH4)2B4O7.
Ⅲ.用已知浓度的盐酸标准溶液滴定,根据盐酸消耗的量计算出氮的含量,然后乘以相应的换算系数,即得蛋白质的含量.
(1)上述原理第Ⅰ步生成的无机含氮化合物化学式为________.
(2)上述原理第Ⅱ步有关反应的离子方程式(或化学方程式)为:________,________
查看答案和解析>>
科目: 来源:河南省沁阳一中2010届高三第四次月考、化学试卷 题型:022
已知某溶液中只含有4种离子:A+、B-、H+、OH-,对这4种离子浓度的大小比较,有以下3种说法.请判断离子浓度的大小顺序是否正确,你认为正确的请在相应的空格内填上符合这种情况的A+和B-组成物质的化学式(只写一种情况,可以是一种溶质或两种溶质);你认为一定不正确的,请在相应的空格内填上你选择“不正确”的理由.供选择的离子有:Na+、Ag+、NH4+、Cl-、NO3-、CH3COO-、H+、OH-
(1)c(B-)>c(A+)>c(H+)>c(OH-):________
(2)c(A+)>c(B-)>c(OH-)>c(H+):________
(3)c(H+)>c(B-)>c(A+)>c(OH-):________
查看答案和解析>>
科目: 来源:河南省沁阳一中2010届高三第四次月考、化学试卷 题型:022
下列三组试剂已失去标签,分别用一种试剂可以鉴别.
A、AlCl3、NaCl、Na2CO3三种溶液
B、Na2CO3、Na2SO4、K2S、Na2SO3、BaCl2、NaAlO2六种溶液;
C、CaC2、NaCl、CuSO4、CaCO3、Al2S3五种固体;
A组可选用________(填名称,下同);
B组可选用________;
C组可选用________.
查看答案和解析>>
科目: 来源:山东省淄博市2010届高三上学期期末考试化学试卷 题型:022
三峡大坝使万里长江变成黄金水道,但三峡船闸的防腐蚀是现实而又紧迫的任务,请你分析:
(1)船闸主要发生的是________腐蚀,并请写出腐蚀的电极反应式:
负极:____________________;
正极:____________________.
(2)请你对三峡船闸的防腐蚀提出一项合理化建议:________________.
查看答案和解析>>
科目: 来源:山东省淄博市2010届高三上学期期末考试化学试卷 题型:022
已知:Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g) △H=-24.8 kJ/mol
3Fe2O3(s)+CO(g)=2Fe3O4(s)+CO2(g) △H=-47.2 kJ/mol
Fe3O4(s)+CO(g)=3FeO(s)+CO2(g) △H=+640.5 kJ/mol
请运用盖斯定律写出CO气体还原FeO固体得到Fe固体和CO2气体的热化学反应方程式:________
查看答案和解析>>
科目: 来源:甘肃省兰州五十五中2009-2010学年度第一学期期末试卷高三化学 题型:022
A、B、C、D为原子序数依次增大的短周期主族元素.已知:A、C同主族,B、C、D同周期,A原子的最外层电子数是次外层电子数的3倍,B是短周期元素中原子半径最大的主族元素.回答下列问题:
①A的元素符号________;D的原子结构示意图________;A2B2的电子式________.
②A、B、C三种元素形成的简单离子的半径由人到小的顺序是________.
③CA2与D元素的单质在水溶液中反应的化学方程式是______________.
查看答案和解析>>
科目: 来源:甘肃省兰州五十五中2009-2010学年度第一学期期末试卷高三化学 题型:022
物质A~K的转化关系如下图所示,已知A是由两种元素组成的化合物;B是非金属单质;J是金属单质.H的相对分子质量比D大16(部分反应物、生成物术列出).
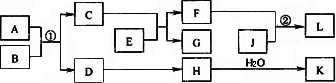
依据上述信息,回答下列问题:
Ⅰ.若A为固体,F是盐,反应①是上业上制取K的重要反应,反应②为化合反应.
(1)G的电子式是_____________________.
(2)工业上反应①在________(填工业设备名称)中进行.
(3)反应①的化学方样式为____________.
Ⅱ.若A为气体,E为活泼金属单质,且K与“I”中的K不同.
(4)物质A的分子式是________________.
(5)反应②的离子方程式为____________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com