
科目: 来源:河南省卢氏二高2010届高三上学期期末模拟高三化学试题 题型:022
对于密闭容器中的反应:
N2(g)+3H2(g)![]() 2NH3(g);ΔH<0,在
2NH3(g);ΔH<0,在
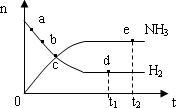
(1)正反应速率点a处的比点b处的________.(填“大、小或相等”)
(2)点c处的正反应速率比逆反应速率________.(填“大、小或相等”)
(3)点d(t1时刻)的n(N2)______(填“大于、小于或等于”)点e(t2时刻)处的n(N2).
(4)其他条件不变,773K下反应至t1时刻,此时画出的两根平行线间的距离将要变________.(填“大、小或相等”)
查看答案和解析>>
科目: 来源:贵州省云峰中学2010届高三下学期3月月考化学试题 题型:022
有机物A(C10H20O2)具有香味,可用作香皂、洗发香波等.已知:
①B分子中没有支链.
②D能与碳酸氢钠溶液反应放出二氧化碳.
③D、E互为具有相同官能团的同分异构体.E分子烃基上的氢若被Cl取代,其一氯代物只有一种.
④F可以使溴的四氯化碳溶液褪色.
(1)B可以发生的反应类型有________(选填序号)
①取代反应
②消去反应
③加聚反应
④氧化反应
(2)C、F分子所含的官能团的名称依次是:________、________.
(3)写出与D、E具有相同官能团的同分异构体的可能结构简式:________________.
(4)写出由B生成F的化学方程式_______________.
(5)E可用于生产氨苄青霉素等.已知E的制备方法不同于其常见的同系物,据报道可由2-甲基-1-丙醇和甲酸在一定条件下制取E.该反应的化学方程式是_________________.
查看答案和解析>>
科目: 来源:贵州省云峰中学2010届高三下学期3月月考化学试题 题型:022
工业制硫酸生产流程如下图:

(1)早期生产用黄铁矿为原料,但现在工厂生产硫酸用硫磺为原料,理由是________________.
(2)在催化反应室,使用常压的原因是:________________.
(3)在气体进入催化反应室前,需净化的原因是:_____________.
(4)已知2SO2(g)+O2(g)![]() 2SO3(g),ΔH=-196 kJ·mol-1.在450℃、常压和钒催化条件下向一密闭容器中充入2 mol SO2和1 mol O2,充分反应后,放出的热量________(填“<”“>”“=”)196 kJ.
2SO3(g),ΔH=-196 kJ·mol-1.在450℃、常压和钒催化条件下向一密闭容器中充入2 mol SO2和1 mol O2,充分反应后,放出的热量________(填“<”“>”“=”)196 kJ.
(5)经检测生产硫酸的原料气成分(体积分数)为SO27%、O211%、N282%.在500℃,0.1 MPa条件下达到平衡时,各种气体的体积比为V(SO2)∶V(SO3)∶V(O2)∶V(N2)=0.46∶6.54∶7.73∶82,则SO2的利用率为________.
(6)在450℃、常压和钒催化条件下,在容积为VL的容器中加入2n mol SO2和n mol O2,反应达平衡后测得平衡常数为K,此时O2的转化率为x.则K和x的关系满足K=________.
查看答案和解析>>
科目: 来源:贵州省云峰中学2010届高三下学期3月月考化学试题 题型:022
物质A中只含有C、H、O三种元素,能发生银镜反应.物质C的相对分子质量为104.A与其他物质之间的转化关系如下图所示:
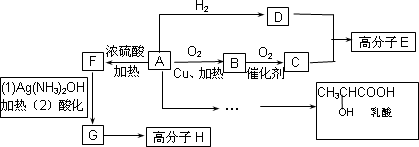
已知:(1)有机物之间的转化关系以及转化过程相对分子质量变化如下:
物质转化关系:RCH2OH RCHO RCOOH
相对分子质量:M M-2 M+14
(2)RCH![]() CH2+HBr
CH2+HBr![]() RCH(Br)CH3
RCH(Br)CH3
回答下列问题:
(1)H结构简式_______________.
(2)一定条件下B发生银镜反应的化学方程式为:_______________.
(3)C、D在一定条件下反应还能生成八元环状物,其化学反应方程式为_______________.
(4)在有机合成中,很多复杂的有机物都是从碳原子数小于或等于4有机物合成的.其中有机物F可以从甲烷合成得到,他的第一步反应是甲烷与氯气的取代反应,若此反应理论上欲获得最多的氯化氢,设V(Cl2)/V(CH4)=x,则x的取值范围是________.
(5)请设计合理方案从A合成乳酸(用反应流程图表示,并注明反应条件).
例:由乙醇合成聚乙烯的反应流程图可表示为:
CH3CH2OH![]() CH2
CH2![]() CH2
CH2![]()
![]()
查看答案和解析>>
科目: 来源:贵州省云峰中学2010届高三下学期3月月考化学试题 题型:022
在元素周期表中,锌(30Zn)、镉(48Cd)、汞(80Hg)同属于锌族,锌和汞在自然界中常共生,镉的金属活动性介于锌和汞之间.湿法炼锌过程中产生的铜镉渣中含有Cu、Cd、Zn等多种金属,可用于生产金属镉.镉的主要用途可以用作镍-镉电池,以及用于颜料生产,镉化合物还在PVC稳定剂、发光材料、半导体材料、杀菌剂等方面有广泛的应用.镉的生产流程如图示意如下:
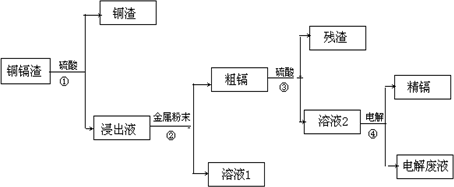
请回答下列问题:
(1)镉元素位于周期表中第________周期,第________族,其原子结构示意图为________;
(2)写出步骤①反应的离子方程式_______________.
(3)步骤②所加入的金属是________.
(4)步骤④用“溶液2”作电解液,镉在________极析出,该电极材料是________.
(5)“电解废液”中含有镉,不能直接作为污水排放.目前含镉的废水处理的方式有两种,一种是在含镉污水中加入硫化钠,沉淀镉离子,另一种是加入聚合硫酸铁和聚合氯化铝,沉淀镉离子.写出硫化钠沉淀镉离子的离子方程式_______________.
查看答案和解析>>
科目: 来源:河北省衡水中学2010届高三上学期第三次调研考试化学试题 题型:022
混合物A由碳酸钠和碳酸氢钠组成.现有两包质量相等的混合物A:
(1)若向其中一包加入100 mL 3 mol/L的Ba(OH)2溶液(过量),使HCO3-、CO32-全部变为沉淀,过滤后,再向滤液中加入200 mL 2 mol/L的稀盐酸,溶液恰好呈中性.
①写出下列反应的离子方程式
碳酸氢钠与过量氢氧化钡的反应:________;
②混合物A中NaHCO3的质量为________g.
(2)若向另一包中先加50 mL 8 mol/L的HCl溶液,使HCO3-、CO32-全部变为CO2后,再加50 mL 2 mol/L的Ba(OH)2溶液,混合后的溶液pH=14(混合后溶液体积变化忽略不计、在常温下).混合物A中Na2CO3的质量为________g.
查看答案和解析>>
科目: 来源:河北省衡水中学2010届高三上学期第三次调研考试化学试题 题型:022
某同学设计实验将Fe3O4和CuO组成的混合物X进行如图所示的转化(每一步均反应完全):
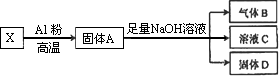
(1)生成气体B的化学方程式是________.
(2)将固体D投入过量稀硫酸并充分反应后,过滤,再向滤液加入双氧水,得黄色溶液.写出当加入双氧水时溶液中发生反应的离子方程式:________.
(3)若已知固体X的质量为7.2 g反应中Al粉的质量是2.7 g,气体B在标准状况下的体积为672 mL,则固体D的质量是________g.
查看答案和解析>>
科目: 来源:河北省衡水中学2010届高三上学期第三次调研考试化学试题 题型:022
已知W、D、E、X、Y、Z是六种短周期主族元素.元素W与元素Y位于同一主族.X、W、E三元素位于同一周期,且原子序数依次增大.D、W在周期表中的位置如下图.
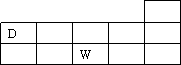
请回答下列问题.
(1)请在上图中用元素符号标明E的位置.
![]() (2)化合物DY2和DW2的分子空间构型相似,DW2的结构式为________.
(2)化合物DY2和DW2的分子空间构型相似,DW2的结构式为________.
(3)已知元素W和E的最外层电子数之和与Y和X的最外层电子数之和相差6;又知aX、bY、cZ三种元素,a+b+c=26.化合物XZ3是合成抗禽流感药物“达菲”的中间活性物质,XZ3受撞击会生成一种非金属单质和一种离子化合物X3Z,请写出该反应的化学方程式________.若反应生成标准状况下11.2 L气体单质,则电子转移的物质的量为________mol.
查看答案和解析>>
科目: 来源:河北省衡水中学2010届高三上学期第三次调研考试化学试题 题型:022
现有四种短周期元素X、Y、Z、W,其中:
①X、W原子的电子层数与最外层电子数之比分别为3∶1和1∶3
②Y元素的某原子核内无中子
③Z元素原子的最外层电子数是其内层电子总数的2倍.
回答下列问题:
(1)X元素在周期表中的位置是________.
(2)上述四种元素中,只由一种元素的原子构成的常见离子是________(填离子符号).
(3)化合物X2W2的电子式是________.
(4)向含1 mol Na2SiO3的溶液中缓慢通入2 mol的ZO2,反应的离子方程式是________.
(5)由Y、Z、W元素中的两种或三种可以组成多种分子,其中含有18个电子的分子是________(填化学式).
(6)用KMnO4溶液可以通过滴定来测定Y2Z2W4溶液的物质的量浓度.向25.00 mL的Y2Z2W4溶液中加入5.00 mL 0.50 mol/L酸性KMnO4溶液恰好完全反应,得到ZO2和Mn2+,则此种Y2Z2W4溶液的物质的量浓度是________mol/L.
查看答案和解析>>
科目: 来源:河北省衡水中学2010届高三上学期第三次调研考试化学试题 题型:022
现有下列短周期元素的性质数据:
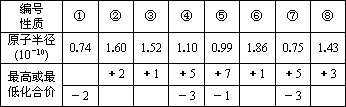
试回答下列问题:
(1)上述元素中处于第ⅤA族的有________,处于第二周期的有________(以上均用编号回答)
(2)上述元素中金属性最强的是________(用编号回答)
(3)经验表明,除氢和氦外,当元素原子的电子层数(n)多于或等于原子最外层电子数(m)即(n-m)≥0时,该元素属于金属元素;当元素原子的最外层电子数(m)多于或等于原子的电子层数(n)即(n-m)<0时,该元素属于非金属元素.试回答:
a、第n(n≥2)周期有________种非金属元素(含零族元素)
b、根据周期表中每个周期非金属元素的种数(含零族元素),预测目前的周期表若填满后还有________种非金属元素未被发现.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com