
科目: 来源:宁夏银川二中2011届高三第三次月考化学试题 题型:022
按下列要求回答
(1)除去下列不纯物质中的少量杂质(括号内为杂质),请填入适当的试剂
①NO(NO2)________
②NH3(H2O)
(2)实验室配制100 mL 0.5 mol·L-1的Na2CO3溶液,回答下列问题:
①应用托盘天平称取碳酸钠粉末________g.
②配制时应选用的仪器有500 mL容量瓶,托盘天平、烧杯、药匙、________.
③若实验时遇到下列情况,所配溶液的浓度偏大的是________.
A.加水定容时超过刻度线,又吸出少量至刻度线
B.没有将洗涤液转入容量瓶
C.容量瓶洗涤后内壁有水珠而未作干燥处理
D.定容时府视刻度线
查看答案和解析>>
科目: 来源:辽宁省沈阳四校协作体2010-2011学年高三12月阶段测试化学试题 题型:022
短周期主族元素A、B、C、D、E、F的原子序数依次增大,它们的原子核外层数之和为13;B的化合物种类繁多,数目庞大;C、D是空气中含量最多的两种元素;
D、E两单质可以生成两种不同的离子化合物;F与D具有相同的最外层电子数.
(1)A与D形成原子个数比为1∶1的化合物,则其电子式________.
(2)A、B、D、E四种元素形成的化合物的水溶液呈碱性,其原因是:(用离子方程式表示)________.
(3)A、C、D、E的原子半径由小到大的顺序________(用元素符号表示).
(4)由B的最简单气态氢化物形成的燃料电池中,用氢氧化钾溶液做电解质溶液则正极反应式:________.
(5)用惰性电极电解NaHSO3溶液来制取硫酸的装置如图所示.
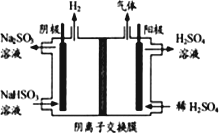
阳极区放出气体的成分________(填化学式).
查看答案和解析>>
科目: 来源:黑龙江省大庆铁人中学2011届高三上学期期中考试化学试题 题型:022
| |||||||||||||||||||||||||||||||||
查看答案和解析>>
科目: 来源:黑龙江省大庆铁人中学2011届高三上学期期中考试化学试题 题型:022
有①~⑧八种短周期元素,其原子序数依次增大,其中②、⑦、⑧三种元素在周期表中的相对位置如下,且元素②所处主族的位置为所有主族的正中间.
(1)元素②在周期表中的位置为________;②、⑦、⑧三种元素最高价氧化物对应水化物的酸性由强到弱的顺序是________(用化学式表示).
(2)如图所示,甲、乙、丙、丁均为①~⑧中某些元素形成的单质或化合物,反应a为置换反应,反应b为化合反应.单质乙与单质丙所含元素位于同一主族,试写出符合条件的反应a的两个化学方程式________、________.
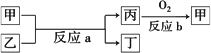
查看答案和解析>>
科目: 来源:江苏省泰州中学2011届高三质量调研测试化学试题 题型:022
近年我国汽车拥有量呈较快增长趋势,汽车尾气已成为重要的空气污染物.
(1)汽车内燃机工作时引起反应:N2(g)+O2(g)![]() 2NO(g),是导致汽车尾气中含有NO的原因之一.T℃时,向容积为2 L的密闭容器中充入10 mol N2与5 mol O2,达到平衡后NO的物质的量为2 mol,则T℃时该反应的平衡常数K=________.(计算结果保留小数点后两位数字)
2NO(g),是导致汽车尾气中含有NO的原因之一.T℃时,向容积为2 L的密闭容器中充入10 mol N2与5 mol O2,达到平衡后NO的物质的量为2 mol,则T℃时该反应的平衡常数K=________.(计算结果保留小数点后两位数字)
(2)一定量的NO发生分解的过程中,NO的转化率随时间变化的曲线如下图所示.(已知:T1<T2)
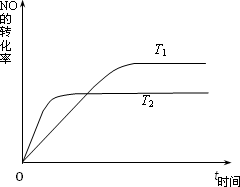
①反应2NO(g)![]() N2(g)+O2(g)为(填“吸热”或“放热”)________反应.
N2(g)+O2(g)为(填“吸热”或“放热”)________反应.
②一定温度下,能够说明反应2NO(g)![]() N2(g)+O2(g)已达到平衡的是(填序号)________.
N2(g)+O2(g)已达到平衡的是(填序号)________.
a.容器内的压强不发生变化
b.NO分解的速率和NO生成的速率相等
c.NO、N2、O2的浓度保持不变
d.单位时间内分解4 mol NO,同时生成2 mol N2
(3)①当发动机采用稀薄燃烧时,尾气中的主要污染物为NOx,可用CxHy(烃)催化还原NOx消除氮氧化物的污染.
已知:CH4(g)+4NO2(g)![]() 4NO(g)+CO2(g)+2H2O(g) ΔH1=-574 kJ·mol-1
4NO(g)+CO2(g)+2H2O(g) ΔH1=-574 kJ·mol-1
CH4(g)+4NO(g)![]() 2N2(g)+CO2(g)+2H2O(g) ΔH2
2N2(g)+CO2(g)+2H2O(g) ΔH2
CH4(g)+2NO2(g)![]() N2(g)+CO2(g)+2H2O(g) ΔH3=-867 kJ·mol-1
N2(g)+CO2(g)+2H2O(g) ΔH3=-867 kJ·mol-1
ΔH2=________.
②使用催化剂可以将汽车尾气的主要有害成分一氧化碳(CO)和氮氧化物(NOx)转化为无毒气体,该反应的化学方程式为________.
查看答案和解析>>
科目: 来源:2010年普通高等学校招生全国统一考试、化学(江苏卷) 题型:022
乙炔是有机合成工业的一种原料.工业上曾用CaC2与水反应生成乙炔.
(1)CaC2中C22-与O22+互为等电子体,O22+的电子式可表示为________;1 mol O22+中含有的![]() 键数目为________.
键数目为________.
(2)将乙炔通入[Cu(NH3)2]Cl溶液生成Cu2C2红棕色沉淀.CU+基态核外电子排布式为________.
(3)乙炔与氢氰酸反应可得丙烯腈(H2C=CH-C=N).丙烯腈分子中碳原子轨道杂化类型是________;分子中处于同一直线上的原子数目最多为________.
(4)CaC2晶体的晶胞结构与NaCl晶体的相似(如下图所示),但CaC2晶体中含有的中哑铃形C22-的存在,使晶胞沿一个方向拉长.CaC2晶体中1个Ca2+周围距离最近的C22-数目为________.
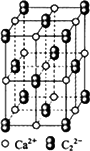
查看答案和解析>>
科目: 来源:2010年普通高等学校招生全国统一考试、化学(江苏卷) 题型:022
以水氯镁石(主要成分为MgCl2·6H2O)为原料生产碱式碳酸镁的主要流程如下:
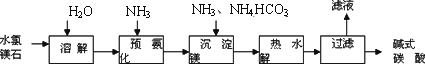
(1)预氨化过程中有Mg(OH)2沉淀生成,已知常温下Mg(OH)2的Ksp=1.8×10-11,若溶液中c(OH-)=3.0×10-6 mol·L-1,则溶液中c(Mg2+)=________.
(2)上述流程中的滤液浓缩结晶,所得主要固体物质的化学式为________.
(3)高温煅烧碱式碳酸镁得到MgO.取碱式碳酸镁4.66 g,高温煅烧至恒重,得到固体2.00 g和标准状况下CO2 0.896 L,通过计算确定碱式碳酸镁的化学式.
(4)若热水解不完全,所得碱式碳酸镁中将混有MgCO3,则产品中镁的质量分数________(填“升高”、“降低”或“不变”).
查看答案和解析>>
科目: 来源:2010年普通高等学校招生全国统一考试、化学(江苏卷) 题型:022
正极材料为LiCoO2的锂离子电池已被广泛用作便携式电源.但钴的资源匮乏限制了其进一步发展.
(1)橄榄石型LiFePO4是一种潜在的锂离子电池正极材料,它可以通过(NH4)2Fe(SO4)2、H3PO4与LiOH溶液发生共沉淀反应,所得沉淀经80℃真空干燥、高温成型而制得.
①共沉淀反应投料时,不将(NH4)2Fe(SO4)2和LiOH溶液直接混合的原因是________.
②共沉淀反应的化学方程式为________.
③高温成型前,常向LiFePO4中加入少量活性炭黑,其作用除了可以改善成型后的LiFePO4的导电性能外,还能________.
(2)废旧锂离子电池的正极材料试样(主要含有LiCoO2及少量AI、Fe等)可通过下列实验方法回收钴、锂.

①在上述溶解过程中,S2O32-被氧化成SO42-,LiCoO2在溶解过程中反应的化学方程式为________.
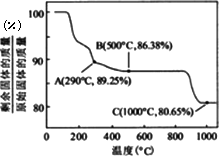
②Co(OH)2在空气中加热时,固体残留率随温度的变化
如下图所示.已知钴的氢氧化物加热至290℃时已完全
脱水,则1000℃时,剩余固体的成分为________.(填化学式);
在350~400℃范围内,剩余固体的成分为________.(填化学式).
查看答案和解析>>
科目: 来源:2010年普通高等学校招生全国统一考试、化学(江苏卷) 题型:022
下表列出了3种燃煤烟气脱硫方法的原理.
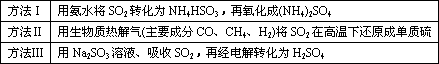
(1)方法Ⅰ中氨水吸收燃煤烟气中SO2的化学反应为:
2NH3+SO2+H2O=(NH4)2SO3
(NH4)2SO3+SO2+H2O=2NH4HSO3
能提高燃煤烟气中SO2去除率的措施有________(填字母).
A.增大氨水浓度 B.升高反应温度 C.使燃煤烟气与氨水充分接触 D.通入空气使HSO3-转化为SO42-
采用方法Ⅰ脱硫,并不需要预先除去燃煤烟气中大量的CO2,原因是________(用离子方程式表示).
(2)方法Ⅱ重要发生了下列反应:
2CO(g)+SO2(g)=S(g)+2CO2(g) ΔH=8.0 KJ·mol-1
2H2(g)+SO2(g)=S(g)+2H2O(g) ΔH=90.4 KJ·mol-1
2CO(g)+O2(g)=2CO2(g) ΔH=-566.0 KJ·mol-1
2H2(g)+O2(g)=2H2O(g) ΔH=-483.6 KJ·mol-1
S(g)与O2(g)O2(g)反应生成SO2(g)的热化学方程式为________.
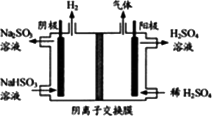
(3)方法Ⅲ中用惰性电极电解NaHSO3溶液的装置如下图所示.阳极区放出气体的成分为________.(填化学式)
查看答案和解析>>
科目: 来源:2010年普通高等学校招生全国统一考试、化学(江苏卷) 题型:022
钡盐行业生产中排出大量的钡泥[主要含有BaCO3、BaSiO3、BaSO3、Ba(FeO2)2等.某主要生产BaCl2、BaCO3、BaSO4的化工厂利用钡泥制取Ba(NO3)2,其部分工艺流程如下:
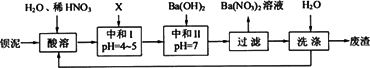
(1)酸溶后溶液中pH=1,Ba(FeO2)2与HNO3的反应化学方程式为________.
(2)酸溶时通常控制反应温度不超过70℃,且不使用浓硝酸,原因是________、________.
(3)该厂结合本厂实际,选用的X为________(填化学式);中和Ⅰ使溶液中________(填离子符号)的浓度减少(中和Ⅰ引起的溶液体积变化可忽略).
(4)上述流程中洗涤的目的是________________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com