
科目: 来源:河南省豫南九校2010-2011学年高三第二次联考化学试题 题型:022
A、B、C、X均为中学化学中常见的纯净物,它们之间有如图所示的转化关系(副产物已略去).
试回答:
(1)若X是强氧化性单质,则A可能是________.(填序号)
a、S
b、Na
c、Mg
d、Al
(2)若X为金属单质,向C的溶液中滴加AgNO3溶液,产生不溶于稀HNO3的白色沉淀,则B的化学式为________;C溶液在储存时应加入少量X,理由是(用离子方程式表示)________.
(3)若A、B、C为含同种金属元素的无机化合物,X为强酸或强碱.A和C在H2O溶液中反应生成B的离子方程式为________.
查看答案和解析>>
科目: 来源:浙江省杭州宏升高复学校2011届高三上学期第三次月考化学试题 题型:022
K2EO4(E代表某种元素)是一种不常见的含氧酸盐,但在工业上有重要的应用,以下是制备该物质的工艺流程图:
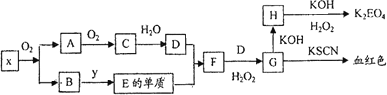
已知:A和C是由同一主族元素组成的化合物,x是工业上制D的重要原料.
请回答以下问题:
(1)x的化学式是________,H的化学式是________.
(2)写出F→G的离子反应方程式________.
(3)琴实现B→E的转化,y的化学式可能是________.
(4)H→K2EO4过程中H2O2的作用________,1 mol H转化为K2EO4时需H2O2的物质的量是________.
查看答案和解析>>
科目: 来源:浙江省杭州宏升高复学校2011届高三上学期第三次月考化学试题 题型:022
下图是一个用铂丝作电极,电解稀的MgSO4溶液的装置,电解液中加有中性红指示剂,此时溶液呈红色.(指示剂的pH变色范围:6.8~8.0,酸色-红色,减色-黄色)回答下列问题:
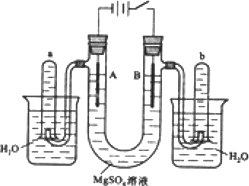
(1)下列关于电解过程中电极附近溶液颜色变化的叙述正确的是________(填编号);
①A管溶液由红变黄;
②B管溶液由红变黄;
③A管溶液不变色;
④B管溶液不变色;
(2)写出A管中发生反应的反应式:________;
(3)写出B管中发生反应的反应式:________;
(4)检验a管中气体的方法是________;
(5)检验b管中气体的方法是________
(6)电解一段时间后,切断电源,将电解液倒入烧杯内观察到的现象是________.
查看答案和解析>>
科目: 来源:浙江省杭州宏升高复学校2011届高三上学期第三次月考化学试题 题型:022
对于可逆反应N2(g)+3H2(g)![]() 2NH3(g);ΔH<0,下列研究目的和示意图相符的是________.
2NH3(g);ΔH<0,下列研究目的和示意图相符的是________.
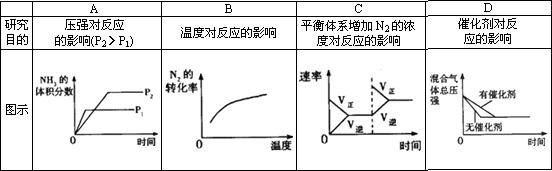
查看答案和解析>>
科目: 来源:新疆乌鲁木齐2011届高三第三次月考化学试题 题型:022
烟气中NOx是NO和NO2的混合物(不含N2O4).
(1)根据废气排放标准,1m3烟气最高允许含400 mg NOx.若NOx中NO质量分数为0.85,则1m3烟气中最高允许含NO________L(标准状况,保留2位小数).
(2)工业上通常用溶质质量分数为0.150的Na2CO3水溶液(密度1.16 g/mL)作为NOx吸收剂,该碳酸钠溶液物质的量浓度为________mol/L(保留2位小数).
(3)已知:NO+NO2+Na2CO3→2NaNO2+CO2①
2NO2+Na2CO3→NaNO3+CO2②
1m3含2000mg NOx的烟气用质量分数为0.150的碳酸钠溶液吸收.若吸收率为80%,吸收后的烟气________排放标准(填“符合”或“不符合”),理由:________.
(4)加入硝酸可改变烟气中NO和NO2的比,反应为:NO+2HNO3→3NO2+H2O当烟气中n(NO)∶n(NO2)=2∶3时,吸收率最高.
1m3烟气含2000 mg NOx,其中n(NO)∶n(NO2)=9∶1.
计算:①为了达到最高吸收率,1m3烟气需用硝酸的物质的量(保留3位小数).
②1m3烟气达到最高吸收率90%时,吸收后生成NaNO2的质量(假设上述吸收反应中,反应①比反应②迅速.计算结果保留1位小数).
查看答案和解析>>
科目: 来源:新疆乌鲁木齐2011届高三第三次月考化学试题 题型:022
2SO2(g)+O2(g)=2SO3(g)反应过程的能量变化如图所示.已知1 mol SO2(g)氧化为1 mol SO3的ΔH=-99 kJ·mol-1.请回答下列问题:

(1)图中A.C分别表示________.________,E的大小对该反应的反应热有无影响?________.该反应通常用V2O5作催化剂,加V2O5会使图中B点升高还是降低?________,理由是________;
(2)图中ΔH=________KJ·mol-1;
(3)V2O5的催化循环机理可能为:V2O5氧化SO2时,自身被还原为四价钒化合物;四价钒化合物再被氧气氧化.写出该催化循环机理的化学方程式________;
(4)已知单质硫的燃烧热为296 KJ·mol-1,计算由S(s)生成3 mol SO3(g)的ΔH(写出计算过程)
查看答案和解析>>
科目: 来源:新疆乌鲁木齐2011届高三第三次月考化学试题 题型:022
有4种化合物W(通常状况下是气态).X(通常状况下是液态).Y、Z(通常状况下是固态),它们共由5种短周期元素A、B、C、D、E组成.已知:①原子序数A<B<C<D<E,且A与D同族;C与E同族;B与C同周期.②W由A和B组成,且W分子中,A与B的原子个数比为4∶1;X由A和C组成,且X分子中A与C的原子个数比为1∶1,Y由C和D组成,属离子化合物,且测得Y固体中C与D的原子个数比为1∶1.③Z由D和E组成,属离子化合物,且其阳离子比阴离子少1个电子层,阳离子数与阴离子数之比为2∶1.试推断写出:
(1)W的化学式是________,W属于________分子(填极性或非极性).
(2)X的电子式是________,X属于________化合物.
(3)1 mol Y在干燥的空气中质量会________(填“增大”或“减小”),其变化量(Δm)为________.
(4)用电子式表示化合物Z的形成过程________.
查看答案和解析>>
科目: 来源:新疆乌鲁木齐2011届高三第三次月考化学试题 题型:022
A.B.C.D.E.F六种短周期主族元素,原子序数依次增大.其中B的单质在常温下为双原子分子,它与A的单质可形成分子X,X的水溶液呈碱性;D的简单阳离子与X具有相同电子数,且D是同周期中简单离子半径最小的元素;E元素的原子最外层比次外层少两个电子,C.F两种元素的原子最外层共有13个电子.则
(1)B的原子结构示意图________;X的分子构型________;
(2)B.C.E分别与A形成的化合物中最不稳定的是________(写化学式);
(3)C与D形成的化合物的化学式是________,它的性质决定了它在物质的分类中应属于________;请写出该化合物的水化物的电离方程式________;
(4)F的单质在反应中常作________剂,该单质的水溶液与E的低价氧化物反应的离子方程式为________.
查看答案和解析>>
科目: 来源:新疆乌鲁木齐2011届高三第三次月考化学试题 题型:022
已知A-O分别代表一种物质,它们之间的转化关系如下图所示(反应条件略去).A、B、H分别是由短周期元素组成的单质.B与冷水缓慢反应,与沸水迅速反应,放出氢气.D是一种离子化合物,其阴阳离子的个数比为2∶3,且能与水反就应得到两种碱.C为淡黄色固体化合物,O能与G的水溶液反应生成蓝色沉淀.
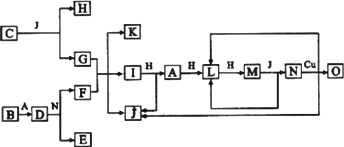
请回答下列问题:
(1)组成B单质的元素位于周期表第________周期,第________族.化合物C的电子式为________.
(2)通常情况下J为液体,用电子式表示其形成过程为________.
(3)写出I与H在点燃条件下反应生成A和J的化学方程式:________.
(4)写出D与足量的N反应生成E和F的化学方程式:________.
查看答案和解析>>
科目: 来源:上海市十三校2011届高三12月联考化学试题 题型:022
大多金属碳化物能与水剧烈反应,生成相应氢氧化物和气态烃,如:
Na4C+4H2O→4NaOH+CH4↑, MgC2+2H2O→Mg(OH)2+C2H2↑
现有CaC2与某常见金属碳化物A的混合物,与足量盐酸反应,得一澄清溶液,并有大量气体产生,将气体通过碱石灰干燥除杂后,测其体积为V1,将所得气体充分燃烧,生成的CO2的体积为V2,相同条件下,V1:V2=5:7:向澄清溶液中逐渐加入足量Na2CO3溶液后,再继续加入NaOH溶液,沉淀物质的量变化如下图所示,试回答下列问题:
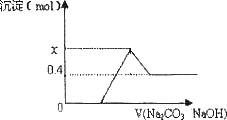
(1)已知A中的金属元素是短周期元素,则该元素是:________(写元素符号),写出CaC2与浓盐酸反应的化学方程式:________;
(2)根据Vl∶V2=5∶7,可算出混合烃中平均每Imol烃分子含有________molC,由此可知气态混合烃中含有乙炔和________,
(3)A的化学式为________;
(4)原混合物中CaC2的物质的量为________mol,A的质量为________g.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com