
科目: 来源:黑龙江省牡丹江一中2011届高三上学期期末考试化学试题 题型:022
(1)pH
=3的盐酸a L,分别与下列3种溶液混合,充分反应后溶液呈中性:①pH=11的氨水b L;
②物质的量浓度为1×10-3 mol/L氨水c L;
③c(OH-)=1×10-3 mol/L的Ba(OH)2溶液d L;
试判断a、b、c、d的大小关系正确的是________
A.a=b>c>d
B.b>a=d>c
C.c>a>d>b
D.c>a=d>b
(2)
已知室温的条件下,pH均为5的H2SO4溶液和NH4Cl溶液,两溶液中c(H+)·c(OH-)=________;各取5 mL上述溶液,分别加水稀释至50 mL,pH较大的是________溶液;各取5 mL上述溶液,分别加热到90℃,pH较小的是________溶液.(3)
同浓度的下列溶液:①NH4Al(SO4)2;②NH4Cl;③NH3·H2O;④CH3COONH4,其中c(NH查看答案和解析>>
科目: 来源:黑龙江省牡丹江一中2011届高三上学期期末考试化学试题 题型:022
化学学科中的平衡理论主要包括:化学平衡、电离平衡、水解平衡和溶解平衡四种,且均符合勒夏特列原理.请回答下列问题:
有甲、乙两个容积相等的恒容密闭容器,
发生反应3A(g)+B(g)![]() xC(g) ΔH=Q KJ/mol
xC(g) ΔH=Q KJ/mol
回答下列问题:
(1)下列各项能作为判断该反应达到化学平衡状态的依据是________(填序号)
①化学反应速率:v(A)=3v(B)
②混合气体的密度保持不变
③有3 mol A消耗的同时有1 mol B生成
④C的浓度保持不变
(2)根据试验测得的数据可知,温度越高该反应的化学平衡常数越大,则Q________0(填“大于”或“小于”)
(3)向甲中通入6 mol A和2 mol B,向乙中通入1.5 mol A、0.5 mol B和3 mol C,将两容器的温度恒定在770 K,使反应3A(g)+B(g)![]() xc(g)达到平衡,此时测得甲、乙两容器中C的体积分数均为0.2.
xc(g)达到平衡,此时测得甲、乙两容器中C的体积分数均为0.2.
①若平衡时,甲、乙两容器中A的物质的量相等,则x=________;
②平衡时甲中A的体积分数为________;
③若平衡时两容器的压强不相等,则两容器中压强之比为________.
查看答案和解析>>
科目: 来源:黑龙江省牡丹江一中2011届高三上学期期末考试化学试题 题型:022
A~I分别表示中学化学中常见的一种物质,它们之间相互关系如下图所示(部分反应物、生成物没有列出),且已知G为主族元素的固态氧化物,A、B、C、D、E、F六种物质中均含同一种元素.
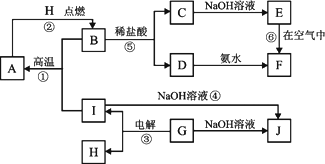
请填写下列空白:
(1)A、B、C、D、E、F六种物质中所含同一种元素的名称为________;
(2)若C→D为化合反应,则此时的化学方程式________;
(3)写出反应④的离子方程式________;
(4)写出反应③的电极方程式:阳极________;阴极________.
(5)从能量变化的角度看,①②③反应中属于ΔH>0的反应是________.(填序号)
查看答案和解析>>
科目: 来源:黑龙江省大庆铁人中学2011届高三上学期期末考试化学试题 题型:022
A、B、C、D、E五种盐,它们的阳离子可能是Na+、NH![]() 、Cu2+、Ba2+、Al3+、Ag+、Fe3+,阴离子可能是Cl-、NO
、Cu2+、Ba2+、Al3+、Ag+、Fe3+,阴离子可能是Cl-、NO![]() 、SO
、SO![]() 、CO
、CO![]() .已知:
.已知:
①五种盐均溶于水,水溶液均为无色.
②D的焰色反应呈黄色.
③A的溶液呈中性,B、C、E的溶液呈酸性,D的溶液呈碱性.
④若在这五种盐的溶液中分别加入Ba(NO3)2溶液,只有A、C的溶液不产生沉淀.
⑤若在这五种盐的溶液中,分别加入氨水,E和C的溶液中生成沉淀,继续加氨水,C中沉淀消失.
⑥把A的溶液分别加入到B、C、E的溶液中,均能生成不溶于稀硝酸的沉淀.
回答下列问题:
(1)五种盐中,一定没有的阳离子是________;所含的阴离子相同的两种盐是(用编号表示)________.
(2)D的化学式为________,推断的理由是________.
(3)A和C的溶液反应的离子方程式是:________.
(4)若要检验B中所含的阳离子,正确的实验方法是________.
查看答案和解析>>
科目: 来源:黑龙江省大庆铁人中学2011届高三上学期期末考试化学试题 题型:022
碘钨灯具有使用寿命长、节能环保等优点.一定温度下,在碘钨灯灯泡内封存的少量碘与沉积在灯泡壁上的钨可以发生如下的可逆反应:W(s)+I2(g)![]() WI2(g)为模拟上述反应,在实验室中准确称取0.508 g碘、0.736 g金属钨放置于50.0 mL密闭容器中,并加热使其反应.下图是混合气体中的WI2蒸气的物质的量随时间变化关系的图像[n(WI2)~t],其中曲线Ⅰ(0~t2时间段)的反应温度为450℃,曲线Ⅱ(从t2时刻开始)的反应温度为530℃.
WI2(g)为模拟上述反应,在实验室中准确称取0.508 g碘、0.736 g金属钨放置于50.0 mL密闭容器中,并加热使其反应.下图是混合气体中的WI2蒸气的物质的量随时间变化关系的图像[n(WI2)~t],其中曲线Ⅰ(0~t2时间段)的反应温度为450℃,曲线Ⅱ(从t2时刻开始)的反应温度为530℃.
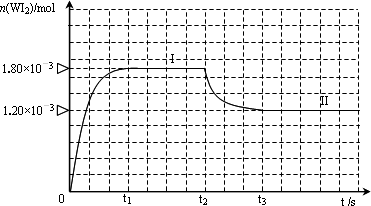
请回答下列问题:
(1)该反应的化学平衡常数表达式为:K=________
(2)该反应是________(填“放热”或“吸热”)反应.
(3)反应从开始到t1(t1=3 min)时间内的平均速率v(I2)=________.
(4)能够说明上述反应已经达到平衡状态的有________.
a.I2与WI2的浓度相等
b.单位时间内,金属钨消耗的物质的量与单质碘生成的物质的量相等
c.容器内混合气体的密度不再改变
d.容器内气体压强不发生变化
(5)在另一个体积为50.0 mL的容器里,在保持530℃温度不变的情况下加入1.0160 g碘、和2.000 g金属钨,达到平衡时WI2的物质的量为________mol.
(6)假设灯丝温度为660℃,灯泡壁温度为350℃.请根据化学平衡移动原理分析在灯泡内充入碘能够延长钨丝寿命的原因________
查看答案和解析>>
科目: 来源:安徽省合肥市2011届高三第一次教学质检化学试题 题型:022
乙基香兰素的键线式结构如下图,它是当今世界上最重要的合成香料之一.
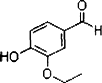
(1)以下推测正确的是________(填字母).
a.从成键方式看,所含碳氧双键中有一个σ键和一个π键
b.该物质的一个分子内含有一个碳氧双键、三个碳碳双键
c
.1 mol该物质最多能与4 mol H2发生加成反应d.该物质能使酸性高锰酸钾溶液褪色,也能与碳酸钠溶液反应产生CO2气体
(2)已知R物质是乙基香兰素的同分异构体,其性质如下:
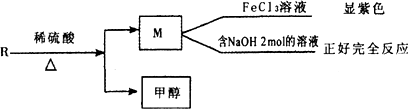
R
符合上述条件,且1 mol R与溴水发生取代反应时,消耗1 mol溴,试写出符合要求的Fl的结构简式________、________、________;(3)X
也是乙基香兰素的同兮异构体,其结构简式为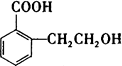
可以通过不同的反应制得下列物质.
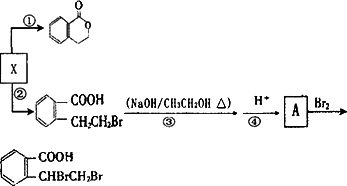
请回答下列问题:
A反应③的反应类型________;
B反应①的化学方程式________.
查看答案和解析>>
科目: 来源:安徽省合肥市2011届高三第一次教学质检化学试题 题型:022
2006年世界锂离子电池总产量超过25亿只,锂电池消耗量巨大,对不可再生的金属资源的消耗是相当大的.因此锂离子电池回收具有重要意义,其中需要重点回收的是正极材料,其主要成分为钴酸锂(LiCoO2)、导电乙炔黑(一种炭黑)、铝箔以及有机粘接剂.某回收工艺流程如下:
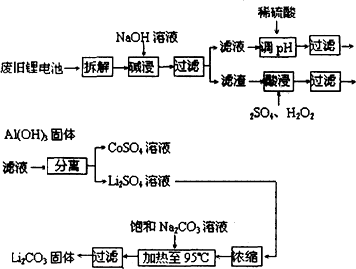
(1)上述工艺回收到的产物有________________.
(2)废旧电池可能由于放电不完全而残留有原子态的锂,为了安全对拆解环境的要求是________________.
(3)碱浸时主要反应的离子方程式为________.
(4)酸浸时反应的化学方程式为________.最后一步过滤应________.
(5)如何洗涤过滤后的Li2CO3固体________________.
查看答案和解析>>
科目: 来源:上海市闵行区2011届高三上学期质量调研考试化学试题 题型:022
将3.96 g组成为X2YZ4的盐(不是复盐)溶于水,滴加适量稀硫酸后再加入2.24 g还原铁粉,恰好完全反应生成Fe2+.向反应后的溶液中加入足量的KOH溶液至刚好将Fe2+完全沉淀;将沉淀过滤、洗涤并充分加热后得到红棕色固体4.80 g;将滤液在一定条件下蒸发可得到一种纯净的不含结晶水的含氧酸盐(不是复盐)13.92 g.
(1)红棕色固体的化学式为________,含氧酸盐的化学式为________.
(2)组成为X2YZ4的盐中是否含有铁元素和钾元素?通过计算说明.
(3)推断X2YZ4的盐的化学式,写出推断过程.
查看答案和解析>>
科目: 来源:上海市闵行区2011届高三上学期质量调研考试化学试题 题型:022
已知:![]()
(1)天然橡胶主要成分的结构为:![]()
其单体的名称为________,该单体与溴发生加成反应时,可能生成的产物有________种.
(2)天然橡胶的单体经臭氧氧化并在锌粉存在时水解生成的物质中除HCHO外,还有(写结构简式):________,产物的物质的量之比依次为:________.
(3)写出由环己醇( )合成己二醛(
)合成己二醛(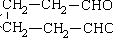 )各步反应的化学方程式:________、________.
)各步反应的化学方程式:________、________.
(4)已知某烃A,俗名为柠檬烯,化学式为C10H16,A经臭氧分解后得到1 mol HCHO和1 mol  .A经催化加氢后得到的产物B,其化学式为C10H20,分子内含有六元环.请推导A的结构简式.
.A经催化加氢后得到的产物B,其化学式为C10H20,分子内含有六元环.请推导A的结构简式.
A________.
查看答案和解析>>
科目: 来源:上海市闵行区2011届高三上学期质量调研考试化学试题 题型:022
| |||||||||||||||||||||||||||||
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com