
科目: 来源:辽宁省抚顺市六校联合体2011届高三二模理综化学试题 题型:022
物质A、E、F的焰色反应呈黄色,物质I的1个分子由4个原子组成并共含有10个电子,B、C、D、K在常温下都是气体单质,G在常温下是无色液体,反应①~⑤都是用于工业生产的反应,各有关物质之间的相互反应转化关系如下图所示(部分反应条件已略去):
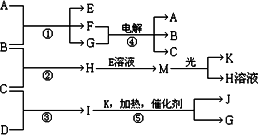
(1)写出物质的化学式:B________ M________
(2)写出A物质的电子式________
(3)0.1 mol/L E水溶液中各离子浓度由大到小的顺序为________
(4)反应④阴极电极反应式________
反应①的离子方程式________
反应⑤的化学方程式________
查看答案和解析>>
科目: 来源:江苏省南京市白下区2011届高三二模化学试题 题型:022
| |||||||||||||||||||||||||||||||||
查看答案和解析>>
科目: 来源:江苏省南京市白下区2011届高三二模化学试题 题型:022
三效催化转化器可减少汽车尾气中的主要污染物(CO、NOx等),部分反应如下:
①2NO(g)+2CO(g)=N2(g)+2CO2(g) ②CO(g)+H2O(g) H2(g)+CO2(g)
H2(g)+CO2(g)
(1)
已知:N2(g)+O2(g)=2NO(g) ΔH=+180.5 kJ·mol-12C(s)
十O2(g)=2CO(g) ΔH=-221.0 kJ·mol-1C(s)
十O2(g)=CO2(g) ΔH=-393.5 kJ·mol-1则反应①的ΔH=________.
(2)已知某温度下,反应②的平衡常数K=1.0.在该温度下向某密闭容器中充入1.0 mol CO和2.0 mol H2O,经充分反应达平衡后,CO的平衡转化率为________,H2的体积分数为________.
(3)NaBH4/H2O2燃料电池是一种有广泛前景的汽车能源,结构如图所示.电池工作时,负极发生的电极反应可表示为________.
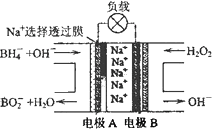
查看答案和解析>>
科目: 来源:江苏省南京市白下区2011届高三二模化学试题 题型:022
铝土矿的主要成分为Al2O3.生产铵明矾[NH4Al(SO4)2·12H2O]和H2O2的工艺流程图如下.
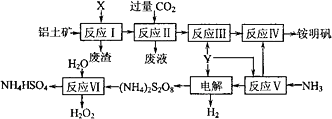
(1)流程图中X为________(填化学式)溶液.
(2)反应Ⅱ的离子方程式为________.
(3)“电解”时,用惰性材料作电极,则阴极反应可表示为________.
(4)反应Ⅵ的化学方程式为________.
(5)流程中可以循环使用的物质是________.
查看答案和解析>>
科目: 来源:广东省深圳市2011届高三二模理综化学试题 题型:022
Na2SO3是抗氧剂.向烧碱和Na2SO3混合溶液中加入少许溴水,振荡后溶液变为无色.
(1)写出碱性中Br2氧化Na2SO3的离子方程式________.
(2)反应后的溶液含有SO![]() 、SO
、SO![]() 、Br-、OH-等阴离子,请填写鉴定其中SO
、Br-、OH-等阴离子,请填写鉴定其中SO![]() 和Br-的实验报告(步骤可增减).
和Br-的实验报告(步骤可增减).
限选试剂:2 mol·L-1 HCl;1 mol·L-1 H2SO4;1 mol·L-1 BaCl2;1 mol·L-1 Ba(NO3)2;0.1 mol·L-1 AgNO3;CCl4;新制饱和氯水.

查看答案和解析>>
科目: 来源:广东省深圳市2011届高三二模理综化学试题 题型:022
有关钴和铁化合物的性质见下表
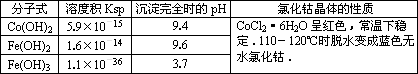
用含钴废料(含少量铁)可制备氯化钴:Co+2HCl=CoCl2+H2↑.工艺流程如下:
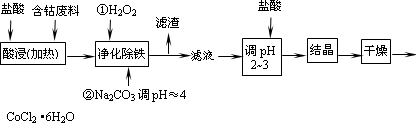
试回答:
(1)“净化除铁”中,写出加入H2O2
时反应的离子方程式________.(2)②步中用Na2CO3调pH≈4的原因是________________.
(3)“滤液”中所含主要溶质的化学式是________.
(4)为防止CoCl2·6H2O脱水,“干燥”时可采用的方法或操作是_______________.
查看答案和解析>>
科目: 来源:广东省深圳市2011届高三二模理综化学试题 题型:022
| |||||||||||||||||||||||||||
查看答案和解析>>
科目: 来源:北京市顺义区2011届高三二模理综化学试题 题型:022
X、Y、Z是中学化学常见的三种元素,其中,X、Z位于短周期.常温下,X单质为黄绿色气体;向含Y离子的溶液中滴加氢氧化钠溶液,生成白色絮状沉淀,迅速变为灰绿色,最后变为红褐色;Z的最外层电子数与核外电子总数之比为3∶13.请回答下列问题:
(1)Z在元素周期表中的位置是________,X单质分子的电子式是________.
(2)Z单质与Y的氧化物在高温条件下反应是冶炼Y单质的一种方法,该反应化学方程式是________.
(3)含上述元素的某些物质常用于处理工业废水,部分流程如下图:

①处理含铬废水时,在反应池中Cr2O![]() 变为Cr3+,当反应转移1 mol电子时,有________mol Cr2O
变为Cr3+,当反应转移1 mol电子时,有________mol Cr2O![]() 转化(计算结果保留两位小数).
转化(计算结果保留两位小数).
②含Z化合物可以使水中悬浮颗粒发生凝聚,原因是________________(用文字和化学用语表示).
③处理含氰废水时,CN-最终转化为两种无毒的气体,该反应的离子方程式是________.
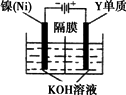
(5)利用下图方法电解可得到一种新型净水剂K2YO4,阳极的电极反应式为________.
查看答案和解析>>
科目: 来源:北京市海淀区2011届高三二模理综化学试题 题型:022
煤的气化是高效、清洁地利用煤炭的重要途径之一.
(1)
在25℃、101 kPa时,H2与O2化合生成1 mol H2O(g)放出241.8 kJ的热量,其热化学方程式为________.又知:①C(s)+O2(g) CO2(g) ΔH=-393.5 kJ/mol
CO2(g) ΔH=-393.5 kJ/mol
②CO(g)+![]() O2(g)
O2(g) CO2(g) ΔH=-283
CO2(g) ΔH=-283
焦炭与水蒸气反应是将固体煤变为气体燃料的方法
,C(s)+H2O(g) CO(g)+H2(g) ΔH=________kJ/mol.
CO(g)+H2(g) ΔH=________kJ/mol.
(2)CO
可以与H2O(g)进一步发生反应:CO(g)+H2O(g)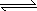 CO2(g)+H2(g) ΔH<0
CO2(g)+H2(g) ΔH<0
在甲、乙、丙三个恒容密闭容器中,起始时按照下表进行投料,在800℃时达到平衡状态,K=1.0.

①该反应的平衡常数表达式为________.
②平衡时,甲容器中CO的转化率是________;
容器中CO的转化率:乙________甲;丙________甲.(填“>”、“=”或“<”)
③丙容器中,通过改变温度,使CO的平衡转化率升高,则温度________(填“升高”或“降低”).
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com