
科目: 来源:山东省莘县实验高中2012届高三上学期期中考试化学试题 题型:022
储氢纳米碳管的研制成功体现了科技的进步.用电弧法合成的纳米碳管常伴有大量的杂质碳纳米颗粒,这种碳纳米颗粒可用氧化气化法提纯,其反应中的反应物和生成物有C、CO2、H2SO4、K2Cr2O7、Cr2(SO4)3、H2O七种物质.
(1)若将碳纳米颗粒分散到一定溶剂中,形成稳定的分散系,所具的性质有________
①丁达尔效应
②加入饱和(NH4)2SO4溶液产生聚沉
③可通过半透膜
(2)请用上述物质填空,并配平化学方程式:
________C+________+________H2SO4→________K2SO4+________+________Cr2(SO4)3+________H2O
(3)H2SO4在上述反应中表现出来的性质是(填选项编号)________.
A.氧化性
B.氧化性和酸性
C.酸性
D.还原性和酸性
(4)若反应中电子转移了0.8 mol,则产生的气体在标准状况下的体积为________.
(5)若将一定量的上述气体通入含0.1 mol NaOH的溶液中,小心加热蒸干,可得7.16 g固体,则在加热前溶液中离子浓度的大小关系是________.
查看答案和解析>>
科目: 来源:山东省济宁市汶上一中2012届高三11月月考化学试题 题型:022
X、Y、Z、W是元素周期表中前四周期的常见元素,其相关信息如下表;

(1)X位于元素周期表第________族.X的一种单质熔点很高,硬度很大,则这种单质的晶体属于________晶体.
(2)X与Y中电负性较强的是(填元素符号)________;XY2的电子式是________,分子中存在________个σ键.
(3)Z2Y2中含有的化学键类型有________.阴、阳离子的个数比为________.
(4)W的基态原子核外电子排布式是________.
(5)废旧印刷电路板上有W的单质A.用H2O2和H2SO4的混合溶液可溶出印刷电路板上的A.已知:
A(s)+H2SO4(aq)![]() ASO4(aq)+H2(g) ΔH=+64.4 kJ·mol-1
ASO4(aq)+H2(g) ΔH=+64.4 kJ·mol-1
2H2O2(l)![]() 2H2O(l)+O2(g) ΔH=-196.4 kJ·mol-1
2H2O(l)+O2(g) ΔH=-196.4 kJ·mol-1
H2(g)+![]() O2(g)
O2(g)![]() H2O(l) ΔH= -285.8 kJ·mol-1
H2O(l) ΔH= -285.8 kJ·mol-1
请写出A与H2SO4、H2O2反应生成ASO4(aq)和H2O(l)的热化学方程式(A用化学式表示):________.
查看答案和解析>>
科目: 来源:山东省济宁市汶上一中2012届高三11月月考化学试题 题型:022
现有浓度各为2 mol/L的FeCl3、FeCl2、CuCl2混合溶液100 mL,加入一定量的铁粉,按下列情况填空.
(1)充分反应后,无固体存在,则溶液中一定含有的金属阳离子是________.
(2)反应完毕后,铁粉有剩余,过滤所得的固体物质为________,溶液中一定含有的金属离子的物质的量为________mol.
(3)反应完毕,有固体剩余,则反应后的溶液中一定有的金属阳离子为________,其物质的量取值范围是________.
查看答案和解析>>
科目: 来源:山东省济宁市汶上一中2012届高三11月月考化学试题 题型:022
纯净物A、B、C、D、E均是中学常见的物质.其转化关系如下图所示(图中某些生成物已略去),物质A与物质B之间的反应不在溶液中进行,通常状况下D为气体请回答下列问题:
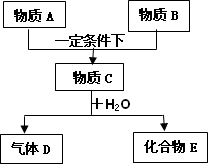
(1)若A、B、D均为短周期元素的单质,C为化合物且气体D就是物质B,又知D气体不可燃,则B的分子式是________,化合物E的化学式为________.
(2)若A、C、D均为短周期元素的单质,B、E为氧化物,且化合物E通常状况下为气体,在一定条件下E还可以和氧气发生反应.则A位于在周期表中的________周期________族.A和B反应生成C的化学方程式是________.
查看答案和解析>>
科目: 来源:山东省济宁市汶上一中2012届高三11月月考化学试题 题型:022
工业盐中含有NaNO2,外观和食盐相似,有咸味,人若误食会引起中毒,致死量为0.3 g-0.5 g.已知NaNO2能发生如下反应:aNO![]() +xI-+yH+=bNO↑+cI2+zH2O,
+xI-+yH+=bNO↑+cI2+zH2O,
请回答下列问题:
(1)上述反应中,x、y、z的数值分别是________(全对才给分).
(2)根据上述反应,可用化学试纸和生活中常见物质进行实验来鉴别工业盐和食盐,现有碘化钾淀粉试纸,则还需选用的生活中常见物质的名称为________.
(3)某工厂废切削液中含有2%-5%的NaNO2,直接排放会造成水污染,但加
入下列物质中的某一种就能使NaNO2转化为不引起污的N2,该物质是________,
a.NaCl
b.H2O2
c.NH4Cl
d.浓H2SO4
所发生反应的离子方程式为:________.
查看答案和解析>>
科目: 来源:安徽省省城名校2012届高三第三次联考试题化学试题 题型:022
2011年9月29日21时16分许,中国首个目标飞行器“天宫一号”搭乘着“长征二号F”T1运载火箭在酒泉卫星发射中心载人航天发射场成功发射升空,这标志着中国在探索太空的征程上又迈出了一大步,是中华民族太空计划的一重大里程碑事件.在这之前的火箭推进剂的主要成分是有毒的四氧化二氮和偏二甲肼,现在改用了液氧、煤油.
试回答下列问题:
(1)在之前的火箭助推器中是以液态的四氧化二氮(N2O4)和液态的偏二甲肼(C2H8N2)为推进剂的.已知10 g液态偏二甲肼与足量N2O4完全反应放出425 kJ的热量,生成对环境无害的N2、CO2、水蒸气.写出该反应的热化学方程式:________.在该反应中,氧化剂为________,转移的电子数为________.
(2)火箭推进剂采用煤油和液氧,解决了接触推进剂的工作人员的安全问题,是目前各国常用的燃料.已知煤油(以十二烷C12H26为例)的燃烧热为8075 kJ·mol-1,试计算同等条件下,C12H26和原燃料(偏二甲肼与N2O4)分别燃烧时,放出同等热量时的C12H26与C2H8N2的质量比________.
(3)目前,各国致力发展高效新型燃料,即液氢和液氧,燃烧时生成气态水.已知lg氢气完全燃烧生成液态水时放出142.9 kJ的热量,又知1 mol液态水变成水蒸气时需要吸收44.0 kJ的热量,写出火箭发射时H2(g)燃烧的热化学方程式:________.
查看答案和解析>>
科目: 来源:安徽省省城名校2012届高三第三次联考试题化学试题 题型:022
我省合肥市大力发展清洁能源产业,以太阳能为代表的新能源产业规模占全省的一半以上.试完成下列问题:
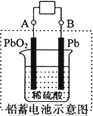
(1)现在电瓶车所用电池一般为铅蓄电池,如图所示,这是一种典型的可充电电池,电池总反应式为:Pb+PbO2+4H++2SO![]()
![]() 2PbSO4+2H2O.则电池放电时,溶液的pH会________(填“增大”或“减小”),写出负极反应式为________充电时,铅蓄电池的负极应与充电器电源的________极相连.
2PbSO4+2H2O.则电池放电时,溶液的pH会________(填“增大”或“减小”),写出负极反应式为________充电时,铅蓄电池的负极应与充电器电源的________极相连.
(2)为体现节能减排的理念,中国研制出了新型燃料电池汽车,该车装有“绿色心脏”——质子交换膜燃料电池.下图是某种质子交换膜燃料电池原理示意图.该电池的正极是________(填“a”或“b”,下同)极,工作过程中,质子(H+)透过质子交换膜移动到________极.写出该电池的负极反应式为:________.

(3)最近,合肥开工建设大型太阳能电池板材料生产基地,这种材料主要是高纯度的硅,下面关于硅的叙述中,正确的是________.
A.硅的非金属性比碳弱,只有在高温下才能跟氢气起化合反应
B.SiO2与碳酸钠固体高温条件下反应,说明硅酸的酸性强于碳酸
C.SiO2是酸性氧化物,它不溶于任何酸
D.虽然硅的化学性质不活泼,但在自然界中以化合态存在
E.硅是构成矿物和岩石的主要元素,硅在地壳中的含量在所有的元素中居第一位
查看答案和解析>>
科目: 来源:吉林省长春市十一中2012届高三上学期期中考试化学试题 题型:022
将镁粉和铝粉混合均匀后,取不同质量的混合物分别加入到100 mL某浓度的稀硫酸中,产生气体的体积(已折合成标准状况)与加入混合物的质量关系如下表:
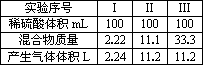
(1)实验中,硫酸过量的实验为________(填序号).
(2)稀硫酸的物质的量浓度为________.
(3)固体粉末中Mg和Al的物质的量之比为________.
(4)当稀硫酸体积为350 mL时,加入33.3克该固体粉末,充分反应后产生的气体体积(标准状况下)为________L.
查看答案和解析>>
科目: 来源:吉林省长春市十一中2012届高三上学期期中考试化学试题 题型:022
(1)某温度(t℃)时,水的Kw=1.0×10-13,则该温度(填“大于”“小于”或“等于”)________25℃,其理由是________.将此温度下PH=11的NaOH溶液a L与PH=1 H2SO4 b L混合,若所得浊合液为中性,则a∶b=________
(2)已知25℃,时0.1 mol/L醋酸溶液达到平衡时的PH值约为3,如果在此溶液中加入等体积的PH值为5的盐酸,则电离平衡________(填“向左”“向右”“不移动”).若向原醋酸溶液中加入少量醋酸钠晶体,待晶体溶解后溶液的PH________(填“增大”“减小”或“不变”)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com