
科目: 来源:河北省正定中学2012届高三第二次综合考试化学试题 题型:022
黄血盐[亚铁氰化钾,K4Fe(CN)6]目前广泛用做食盐添加剂(抗结剂),我国卫生部规定食盐中黄血盐的最大使用量为10 mg·kgˉ1.黄血盐易溶于水,在水溶液中会电离出K+和[Fe(CN)6]4ˉ,其中CNˉ的电子式为![]() .它与硫酸反应的化学方程式为K4Fe(CN)6+6H2SO4+6H2O
.它与硫酸反应的化学方程式为K4Fe(CN)6+6H2SO4+6H2O![]() 2K2SO4+FeSO4+3(NH4)2SO46CO↑
2K2SO4+FeSO4+3(NH4)2SO46CO↑
(1)上述反应是否为氧化还原反应?________(填“是”或“不是”).
(2)食盐经长时间火炒,“亚铁氰化钾”名称前的“亚铁”就去掉了,变成了剧毒物质氰化钾,这是因为黄血盐在超过400℃时会分解,试配平该反应的化学方程式:
(3)黄血盐可与高锰酸钾溶液反应,其化学方程式为
K4Fe(CN)6+KMnO4+H2SO4→KHSO4+Fe2(SO4)3+MnSO4+HNO3+CO2↑+H2O(未配平)
①该反应的氧化产物有________(填化学式).
②若有1 mol K4Fe(CN)6被高锰酸钾氧化,则消耗高锰酸钾的物质的量________mol.
查看答案和解析>>
科目: 来源:河北省正定中学2012届高三第二次综合考试化学试题 题型:022
水是生命之源,也是化学反应中的主角.请回答下列问题:(下列问题
所涉及的答案可能有多种,只需答出一种情况即可)
1.水是一种电解质,发生电离会产生电子总数相同的两种微粒,其电离的方程式为________.
2.有以下五组离子
①K+、Cl-、NO3-、S2-;
②K+、Fe2+、I-、SO42-;
③Na+、Cl-、NO3-、SO42-;
④Na+、Ca2+、Cl-、HCO3-;
⑤K+、Ba2+、Cl-、NO3-.在由水电离产生的c(OHˉ)=1×10ˉ13 mol/L溶液中,一定不能大量共存的离子组是________(填序号)
3.在许多反应中H2O扮演不同的“角色”.请结合所学完成下列反应
(1)H2O参与的置换反应:
符合X+W→Y+V,已知X和Y分别是短周期同主族两种元素形成的单质,W、V是化合物
①W是水,离子方程式为________;
②V是水,化学方程式为________.
(2)水既不是氧化剂也不是还原剂的氧化还原反应:
A、B是中学化学常见的两种由短周期元素组成的有色气体,它们均能与水发生氧化还原反应,但水既不是氧化剂也不是还原剂,写出A、B与水反应的化学方程式:
①A+H2O________;
②B+H2O________;
查看答案和解析>>
科目: 来源:河南省卫辉市第一中学2012届高三4月考试化学试题 题型:022
肼(N2H4)又称联氨,是一种可燃性的液体,可用作火箭燃料.
(1)肼的结构式为:________.
(2)下图是一个电化学过程示意图.
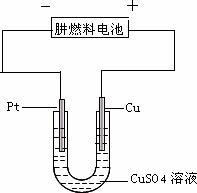
①铂片上发生的电极反应是________.
②假设使用肼一空气燃料电池作为本过程中的电源,铜片的质量变化128 g,则肼一空气燃料电池理论上消耗标准状况下的空气________L(假设空气中氧气体积含量为20%).
(3)肼——空气燃料电池是一种碱性燃料电池,生成无污染的物质.电解质溶液是20%-30%的KOH溶液.肼——空气燃料电池放电时:负极的电极反应式是________.
查看答案和解析>>
科目: 来源:辽宁省大连市2012届高三双基测试化学试题 题型:022
室安卡因(G)是一种抗心律失常药物,可由下列路线合成;
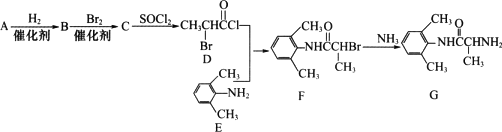
(1)已知C的核磁共振氢谱有3种不同的峰,其峰面积比为3:1:1,B能发生酯化反应.则A中含有的官能团是________(写名称).C的结构简式是________.
(2)写出由,B-C的化学方程式________.
(3)D+E→F的反应中,还有一种小分子生成,该小分子为________.(写化学式)
(4)F→G的反应类型是________,G的分子式为________.
(5)下列关于室安卡因(G)的说法正确的是________.
a.能发生加成反应
b.能发生酯化反应
c.不存在同分异构体
d.属于芳香烃
查看答案和解析>>
科目: 来源:辽宁省大连市2012届高三双基测试化学试题 题型:022
硅在材料王国中具有举足轻重的位置.请解答下列试题:
(1)硅的制备方法是制约太阳能发展的瓶颈,硅的制备原料是石英砂,石英与焦炭在高温电炉中反应可以制得硅.该反应的化学方程式是________,该反应的气体产物是一氧化碳,不是二氧化碳,其原因是________.
(2)氮化硅Si3N4是一种高温结构材料,粉末状态的Si3N4可以由SiCl4的蒸气和NH3反应制取.粉末状Si3N4对空气和水都不稳定.但将粉末状的Si3N4和适量氧化镁在230×1.01×105 Pa和185℃的密闭容器中热处理,可以制得结构十分紧密、对空气和水都相当稳定的固体材料,同时还得到对水不稳定的Mg3N2.
①写出由SiCl4和NH3反应制取Si3N4的化学反应方程式________;
②现用四氯化硅和氮气在氢气气氛保护下,加强热发生反应,使生成的Si3N4沉积在石墨表面可得较高纯度的氮化硅,该制造方法称为:________;反应的化学方程式为________;该法还可制造金刚石薄膜,反应的化学方程式为________.
③在Si3N4和适量氧化镁在230×1.01×105 Pa和185℃的密闭容器中热处理的过程中,除生成Mg3N2外,还可能生成________物质.热处理后除去MgO和Mg3N2的方法是________.
查看答案和解析>>
科目: 来源:辽宁省大连市2012届高三双基测试化学试题 题型:022
在0.5升密闭容器中,一定量的氮气与氢气进行如下反应:N2(g)+3H2(g)![]() 2NH3(g) ΔH=a kJ·mol-1,其化学平衡常数K与温度的关系如下:
2NH3(g) ΔH=a kJ·mol-1,其化学平衡常数K与温度的关系如下:
请回答下列问题:
(1)写出该反应的化学平衡常数的表达式:________,a________0(填“大于”、“小于”或”等于”).
(2)400℃时,2NH3(g)![]() N2(g)+3H2(g)的化学平衡常数为________,测得氨气、氮气、氢气的物质的量分别为3 mo1、2 mol、1 mol时,该反应的v正(N2)________v逆(N2)(填“大于”、“小于’或”等于”).
N2(g)+3H2(g)的化学平衡常数为________,测得氨气、氮气、氢气的物质的量分别为3 mo1、2 mol、1 mol时,该反应的v正(N2)________v逆(N2)(填“大于”、“小于’或”等于”).
查看答案和解析>>
科目: 来源:辽宁省大连市2012届高三双基测试化学试题 题型:022
已知A、B、C为中学化学中常见的单质.室温下,A为固体,B和C均为气体.在适宜的条件下,它们可以按下面框图进行反应.
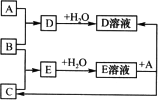
回答下列问题:
(1)A、B、C三种元素中的任意两种元素形成的化合物所属物质类别一定不是________.
①氢化物
②酸
③碱
④盐
⑤氧化物
理由是________.
(2)A、B、C三种元素中有一种是金属,则三种元素中可能是金属的是________,理由是________.
(3)如果E溶液是一种强酸,写出E作为还原剂参加反应的离子方程式________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com