
科目: 来源:上海市浦东新区2012届高三4月(二模)质量抽测化学试题 题型:022
酒后驾车已成为一个社会问题.检测驾驶人员呼气中酒精浓度(BrAC)的方法有多种.
1.早期是利用检测试剂颜色变化定性判断BrAC,曾用如下反应检测BrAC:3CH3CH2OH+2KMnO4→3CH3CHO+2MnO2+2KOH+2H2O.上述反应中发生还原反应的过程是________→________.
2.已知KMnO4在酸性条件下氧化性增强,能得到更多的电子,若在稀硫酸中反应的氧化产物为乙酸,则还原产物为________;若反应产生了12.0 mg乙酸,则转移的电子数目是________.
3.受上述方法启发,后来用五氧化二碘的淀粉溶液检测BrAC,乙醇被氧化为乙醛,该反应的化学方程式为________.
4.1994年美国首次批准使用唾液酒精含量检测方法,成为血液、呼气之后的第三种检测手段.其原理是在乙醇氧化酶作用下,乙醇与氧气反应生成乙醛和过氧化氢,判断该条件下乙醇、氧气、乙醛和过氧化氢四种物质中氧化性最强的物质是________(填写化学式).
查看答案和解析>>
科目: 来源:陕西省西安市八校2012届高三联考化学试题 题型:022
(1)常温下,用0.1000 mol/L NaOH浴液分别滴定20.00 mL 0.1000 mol/L HCl溶液和20.00 mL 0.1000 mol/L CH3COOH溶液,得到2条滴定曲线,如下图所示.
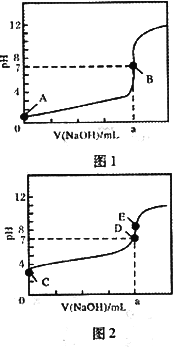
①由A、C点判断,滴定HC1溶液的曲线是________(填“图1”或“图2”);
②a=________mL;
③c(Na+)=c(CH3COO-)的点是________(填B、D或E);
④E点对应离子浓度由大到小的顺序为________.
(2)Cr(OH)3在溶液中存在以下沉淀溶解平衡:Cr(OH)3(s)![]() Cr3+(aq)+3OH-(aq)常温下,Cr(OH)3的溶度积Kap=c(Cr3+)·c3(OH-)=10-32,要使c(Cr3+)(aq)常温下,Cr(OH)3的溶度积Kap=c(Cr3+)·c3(OH-)=10-32,要使c(Cr3+)10-5 mol/L,溶液的pH应调至________.
Cr3+(aq)+3OH-(aq)常温下,Cr(OH)3的溶度积Kap=c(Cr3+)·c3(OH-)=10-32,要使c(Cr3+)(aq)常温下,Cr(OH)3的溶度积Kap=c(Cr3+)·c3(OH-)=10-32,要使c(Cr3+)10-5 mol/L,溶液的pH应调至________.
查看答案和解析>>
科目: 来源:陕西省西安市八校2012届高三联考化学试题 题型:022
现有部分短周期元素的性质或原子结构如下表:

(1)元素X的一种同位素可测定文物年代,这种同位素的符号是________.
(2)元素Y与氢元素形成一种离子YH+4,写出该微粒的电子式________(用元素符号表示)
(3)元素Z与元素T相比,非金属性较强的是________(用元素符号表示),下列表述中能证明这一事实的是________.
a.常温下Z的单质和T的单质状态不同
b.Z的氢化物比T的氢化物稳定
c.一定条件下Z和T的单质都能与氢氧化钠溶液反应
(4)探寻物质的性质差异性是学习的重要方法之一.T、X、Y、Z四种元素的最高价氧化物的水化物中化学性质明显不同于其他三种酸的是________,理由是________.
查看答案和解析>>
科目: 来源:陕西省西安市八校2012届高三联考化学试题 题型:022
白磷(P4)是一种常见的晶体,可用于制备较纯的磷酸.
(1)31 g白磷与足量的氧气完全燃烧释放出745.5 kJ的热量,请写出白磷燃烧的热化学反应方程式:________
(2)已知白磷和氯酸溶液可发生如下反应:
配平并完成上述反应方程式.
(3)白磷有毒,在实验室可采用CuSO4溶液迸行处理,其反应为:11 P4+60CuSO4+96H2O![]() 20Cu3P+24H3PO4+60H2SO4该反应的氧化产物是________,若有1.1 mol P4反应,则有________mol电子转移.
20Cu3P+24H3PO4+60H2SO4该反应的氧化产物是________,若有1.1 mol P4反应,则有________mol电子转移.
查看答案和解析>>
科目: 来源:天津市天津一中2012届高三摸底检测化学试题 题型:022
某有机物A由C.H.O.N四种元素组成,质量分数分别为C:54.8%,H:5.58%,N:7.11%,其余为O,A的相对分子质量不超过300.A是-氨基酸,并且分子中-NH2和-COOH连在同一个碳原子上,分子中不存在甲基(-CH3),能与FeCl3溶液发生显色反应,1 mol A的溶液能与3 mol NaOH完全反应.请回答:
(1)有机物A的相对分子质量为________,其分子式为________.
(2)符合上述条件的有机物A的结构有________种,写出其中的三种结构简式:________.________.________.
查看答案和解析>>
科目: 来源:天津市天津一中2012届高三摸底检测化学试题 题型:022
“立方烷”是新合成的一种烃,其分子为正立方体结构,其结构如图所示:
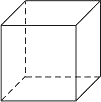
(1)立方烷的分子式为________.
(2)其二氯代物共有________种同分异构体.
(3)与立方烷互为同分异构体的芳香烃的结构简式为________.这种芳香烃异构体与单体________(写结构式)可合成具有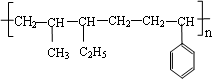 结构的橡胶.
结构的橡胶.
(4)苯乙炔可用这种芳香烃异构体为起始物质,通过加成.消去反应制得.写出制取苯乙炔的化学方程式(所需的无机试剂自选).
________,________.
查看答案和解析>>
科目: 来源:上海市虹口区2013年高考一模化学试题 题型:022
1200℃时可用反应2BBr3(g)+3H2(g)![]() 2B(s)+6HBr(g)来制取晶体硼.完成下列填空∶
2B(s)+6HBr(g)来制取晶体硼.完成下列填空∶
1.下列说法能说明该反应达到平衡的是________(选填序号,下同).
a.v正(BBr3)=3v逆(HBr)
b.2c(H2)=c(HBr)
c.密闭容器内压强不再变化
d.容器内气体平均摩尔质量不再变化
2.若密闭容器体积不变,升高温度,晶体硼的质量增加,下列说法正确的是________.
a.在平衡移动时正反应速率先增大后减小
b.在平衡移动时逆反应速率始终增大
c.正反应为放热反应
d.达到新平衡后反应物不再转化为生成物
3.若上述反应在10 L的密闭容器内反应,5 min后,气体总质量减少1.1 g,则该时间段内氢气的平均反应速率为________.
4.往容器中充入0.2 mol BBr3和一定量H2,充分反应达到平衡后,混合气体中HBr百分含量与起始通入H2的物质的量有如图关系.
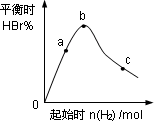
在a、b、c三点中,H2的转化率最高的是________(选填字母).
b点达到平衡后,再充入H2使平衡到达c点,此过程中平衡移动的方向为________(填“正向”、“逆向”或“不移动”).
查看答案和解析>>
科目: 来源:上海市虹口区2013年高考一模化学试题 题型:022
下表中所列的字母分别代表某一化学元素.完成下列填空∶
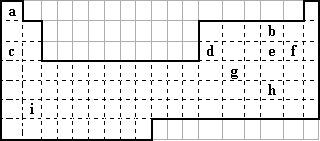
1.h的最外层有________种运动状态的电子.a、b、c三种元素形成的化合物电子式为________.
2.d单质溶于i的最高价氧化物对应水化物的溶液时发生反应的离子方程式为________.
3.元素e与f元素相比,非金属性较强的是________(写元素符号),下列表述中能证明这一事实的是________(选填序号).
a.e的阴离子还原性强于f的阴离子
b.f的氢化物酸性强于e的氢化物
c.e单质的熔点高于f单质
d.e和f形成的化合物中,e显正价,f显负价
4.元素X(非a~i元素)是所在周期原子半径最大的非金属元素,它的气态氢化物为三角锥形极性分子,写出X在周期表中的位置________.
查看答案和解析>>
科目: 来源:上海市长宁区2013年高考一模化学试题 题型:022
碳与硅是十分重要的两种元素,金刚石、SiC具有耐磨、耐腐蚀特性,应用广泛.
1.碳元素在周期表中的位置是________,其原子核外通常未成对电子数为________个.
2.已知2Ca3(PO4)2(s)+10C(s)→P4(g)+6CaO(s)+10CO(g)反应中,被破坏的化学键有________.
a.离子键
b.极性共价键
c.非极性共价键
3.一定条件下,Na还原CCl4可制备金刚石,反应结束冷却至室温后,除去粗产品中少量钠的试剂为________.
4.下列叙述正确的有________(填序号),
①Na还原CCl4的反应、Cl2与H2O的反应均是置换反应
②水晶、干冰熔化时克服粒子间作用力的类型相同
③Na2SiO3溶液与SO3的反应可用于推断Si与S的非金属性强弱
④Si在一定条件下可与FeO发生置换反应
查看答案和解析>>
科目: 来源:上海市长宁区2013年高考一模化学试题 题型:022
|
常温下,在100 mL 1 mol/L的NaHCO3溶液中,加入Xmol的Ba(OH)2固体(假设溶液体积和温度保持不变).以下关于溶液中c(CO | |
A. |
当X=0.025时,溶液中有HCO3-和CO32-,且2C(CO32-)=C(HCO3-) |
B. |
当X=0.05时,溶液中有HCO3-和CO32-,且C(CO32-)>C(HCO3-) |
C. |
当X=0.06时,溶液中HCO3-、CO32-浓度都减小了 |
D. |
当X=0.1时,溶液PH增大,沉淀达到最大值 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com