
科目: 来源:江苏省通州市石港中学2008届高三化学科预测卷 题型:022
物质结构与性质:
Mn、Fe均为第四周期过渡元素,两元素的部分电离能数据列于下表:

回答下列问题:
(1)Mn元素价电子层的电子排布式为________,比较两元素的l2、l3可知,气态Mn2+再失去一个电子比气态Fe2+再失去一个电子难.对此,你的解释是________;
(2)Fe原子或离子外围有较多能量相近的空轨道而能与一些分子或离子形成配合物.
①与Fe原子或离子形成配合物的分子或离子应具备的结构特征是________;
②六氰合亚铁离子(Fe(CN)64-)中的配体CN-中C原子的杂化轨道类型是________,写出一种与CN-互为等电子体的单质分子的路易斯结构式_________;
(3)三氯化铁常温下为固体,熔点282℃,沸点315℃,在300℃以上易升华.易溶于水,也易溶于乙醚、丙酮等有机溶剂.据此判断三氯化铁晶体为________;
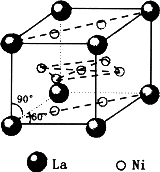
(4)金属铁的晶体在不同温度下有两种堆积方式,晶胞分别如图所示.面心立方晶胞和体心立方晶胞中实际含有的Fe原子个数之比为________.

查看答案和解析>>
科目: 来源:江苏省通州市石港中学2008届高三化学科预测卷 题型:022
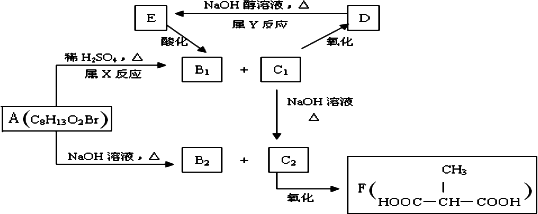
Ⅰ.某化合物A在一定条件下能发生如下图所示的转变:
其中只有B1既能使溴水褪色,又能与Na2CO3溶液反应放出CO2,回答下列问题:
(1)指出反应类型:X________反应,Y________反应.
(2)物质A的结构简式为________.
(3)写出C1![]() C2的化学方程式________.
C2的化学方程式________.
(4)与F互为同分异构体且核磁共振氢谱只有一种峰的有机物的结构简式有________.
Ⅱ.已知,卤代烃之间能发生反应:
C4H9Cl![]() (C4H9)2CuLi
(C4H9)2CuLi![]() C4H9-C2H5
C4H9-C2H5
聚苯乙烯是一种生活中常见的塑料,试以碳化钙、苯为基本有机原料,无机原料自选,在下列方框中用合成反应流程图合成聚苯乙烯
流程图示例:A![]() ……
……![]() B
B
查看答案和解析>>
科目: 来源:湖南省重点中学洞口一中2008年高考模拟训练理科综合化学部分 题型:022
硫酸铜是一种应用极其广泛的化工原料.制备硫酸铜是无机化学实验教学中一个重要的实验.由于铜不能与稀硫酸直接反应,实验中将浓硝酸分次加入到铜粉与稀硫酸中,加热使之反应完全,通过蒸发、结晶得到硫酸铜晶体(装置如图1、2所示).

(1)图2是图1的改进装置,改进的目的是________.
(2)为符合绿色化学的要求,某研究性学习小组进行如下设计:
第一组:空气为氧化剂法
方案1:以空气为氧化剂.将铜粉在仪器B中反复灼烧,使铜与空气充分反应生成氧化铜,再将氧化铜与稀硫酸反应.
方案2:将空气或氧气直接通入到铜粉与稀硫酸的混合物中,发现在常温下几乎不反应.向反应液中加FeSO4或Fe2(SO4)3,反应完全后,向其中加物质甲调节pH到3~4,产生Fe(OH)3沉淀,过滤、蒸发、结晶,滤渣作催化剂循环使用.
(已知Fe(OH)3和Cu(OH)2完全沉淀时的pH分别为3.7、6.4.)
请回答下列问题:
①方案1中的B仪器名称是________.
②方案2中甲物质是________(填字母序号).
a、CaO b、CuCO3 c、CaCO3
第二组:过氧化氢为氧化剂法
将3.2 g铜丝放到45 mL 1.5 mol/L的稀硫酸中,控温在50℃.加入18 mL 10%的H2O2,反应0.5 h后,升温到60℃,持续反应1 h后,过滤、蒸发结晶、减压抽滤等,用少量95%的酒精淋洗后晾干,得CuSO4·5H2O 10.6 g.请回答下列问题:
③该反应的离子反应方程式为________.
④控制温度在50℃和60℃加热的原因为________,晶体采用酒精淋洗的优点是________.
⑤上述两种氧化法中,更符合绿色化学理念的是________(填“第一组”或“第二组”),理由是________.
查看答案和解析>>
科目: 来源:湖南省重点中学洞口一中2008年高考模拟训练理科综合化学部分 题型:022
茚是碳氢化合物,其结构为![]() ,茚有一种同分异构体A,A分子中含有一个苯环且只有一个侧链,A有如下转化关系:
,茚有一种同分异构体A,A分子中含有一个苯环且只有一个侧链,A有如下转化关系:
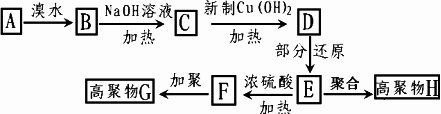
已知:①一个碳原子上同时连2个羟基不稳定,会失水形成羰基;
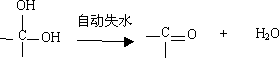
②B、C、D、E的分子结构中均有一个苯环.
根据转化关系和已知条件,试回答:
(1)A中所含官能团的名称________.
(2)A→B的反应类型是________反应.
(3)①写出C→D的化学反应方程式:________
②写出E生成高聚物H的化学方程式________
③写出F与乙醇反应的化学方程式________
(4)①A分子有多种同分异构体,试写出与A同类别且只有一个侧链的同分异构体的结构简式________
②写出符合下列3个条件的E的所有同分异构体的结构简式:a.遇氯化铁显紫色 b.含有邻二取代苯环结构 c.能发生水解反应但不能发生银镜反应.
________________________________________
查看答案和解析>>
科目: 来源:湖南省重点中学洞口一中2008年高考模拟训练理科综合化学部分 题型:022
下图为中学化学中几种常见物质的转化关系.已知:A、C、D是常见的气体单质,H为无色液体化合物,F气体极易溶于水,且液态常做制冷剂.
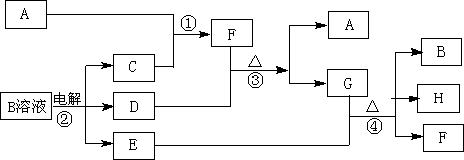
(1)写出化学式A________,写出电子式G________;
(2)鉴定G中阳离子的实验方法和现象________;
(3)D单质和E溶液反应,生成一种常见的消毒剂和漂白剂的有效成分,写出D+E溶液反应的离子方程式________.
(4)反应③的化学方程式________.
(5)将等物质的量的F与G溶于水,所得溶液呈碱性,则该溶液中各种离子浓度大小顺序为:________.
查看答案和解析>>
科目: 来源:湖南省重点中学洞口一中2008年高考模拟训练理科综合化学部分 题型:022
下表是短周期中部分元素的原子半径及主要化合价.
请回答:
(1)Y在元素周期表中的位置是________,镁条在盛有YW2气体的集气瓶中燃烧的现象为________.
(2)V、W、Z三种元素的离子具有相同的电子层结构,三者的离子半径由大到小顺序是________(用元素符号表示).
并用离子方程式表示出Z离子可作净水剂的原因________.
(3)W、X、Y分别与U可形成10电子共价化合物,三者均可形成________晶体,其中沸点最高的是(写化学式)________;1 g YU4气体完全燃烧生成液态水时,放出a kJ的热量,则该反应的热化学方程式为________.
(4)现有Z与V2W2的固体混合物样品,加入稀盐酸至混合物完全溶解,所得的混合液中c(Z3+)∶c(H+)∶c(Cl-)=1∶2∶8,则原固体混合物中,Z元素与V元素的质量比为________(最简整数比).
查看答案和解析>>
科目: 来源:广东省惠州市第八中学2008届高三化学模拟试题(8) 题型:022
有机化学基础:已知:
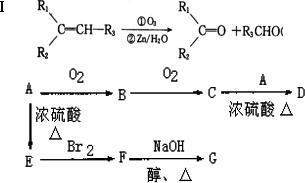
(R1R2R3代表烷烃基)
Ⅱ.烯醇式结构,即碳碳双键连接羟基(如CH2=CH-OH)不能稳定存在.
某有机物![]() 有如下转化关系:
有如下转化关系:
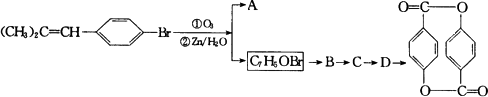
(1)C7C5OBr中官能团名称为________
(2)C7H5OBr与银氨溶液在加热时反应的化学方程式是(有机物写结构简式,下同):________;
(3)从C7H5OBr合成D通常要经过几步有机反应,其中最佳顺序瘦是________(填序号).
a.水解、酸化、氧化 b.氧化、水解、酸化
c.水解、酸化、还原 d.氧化、水解、酯化
(4)A有一种同分异构体,能与Na反应放出H2,该有机物在一定条件下能发生加聚反应,其化学方程式为:________
查看答案和解析>>
科目: 来源:广东省惠州市第八中学2008届高三化学模拟试题(8) 题型:022
A、B、C、D、E五种短周期元素,原子序数依次增大,A、E同主族,A元素的原子半径最小,B元素的原子的最外层电子数是内层电子数的2倍,C元素的最高价氧化物的水化物ACD3与其氢化物CA3反应生成一种盐X,A、B、C、E四种元素都能与D元素形成原子个数比不相同的常见化合物.
请回答下列问题:
(1)由A、B、D、E四种元素组成的某无机化合物Y受热易分解.写出少量Y溶液与足量Ba(OH)2溶液反应的离子方程式________.
(2)将铝片和镁片用导线连接,插入由A、D、E三种元素组成的稀溶液中构成原电池,则负极的电极反应式为________.
(3)常温下,ACD3的稀溶液与CA3的水溶液混合,可能出现的结果是________.
①pH<7,c(H+)>c(CD![]() )>c(OH-)>c(CA
)>c(OH-)>c(CA![]() )
)
②pH<7,c(CD![]() )>c(OH-)=c(H+)>c(CA
)>c(OH-)=c(H+)>c(CA![]() )
)
③①pH>7,c(CA![]() )>c(OH-)>c(CD
)>c(OH-)>c(CD![]() )>c(H+)
)>c(H+)
④①pH<=7,c(CA![]() )>c(CD
)>c(CD![]() )>c(H+)>c(OH-)
)>c(H+)>c(OH-)
(4)对可逆反应3A2(g)+C2(g)![]() 2CA3(g),当反应达到平衡时,不断改变条件(不改变A2、C2、CA3的量),下图表示反应速率与反应过程的关系,其中表示平衡混合物中CA3的含量最高的一段时间是________.
2CA3(g),当反应达到平衡时,不断改变条件(不改变A2、C2、CA3的量),下图表示反应速率与反应过程的关系,其中表示平衡混合物中CA3的含量最高的一段时间是________.
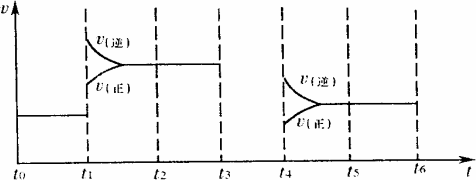
(5)温度为T℃时,将4 amol A2和2 amol C2放入1 L密闭容器中,充分反应后测得C2的转化率为50%,则该反应的平衡常数为________.
查看答案和解析>>
科目: 来源:广东华附2008届高三5月月考化学试卷 题型:022
已知:HCN的结构为H-C≡N,R-CN![]() RCOOH,
RCOOH,
R-Cl+CN-→R-CN+Cl-
(R为烃基).玉米芯、甘蔗渣等废物水解发酵后可制得糠醛![]() ,它是重要的化工原料,它在一定条件下可发生以下变化:
,它是重要的化工原料,它在一定条件下可发生以下变化:
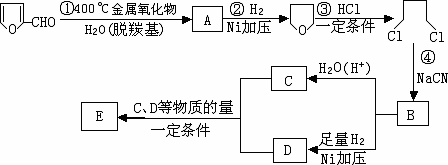
(1)写出反应类型:②________,④________.
(2)写出反应③的化学方程式:________;
写出能证明糠醛中含有醛基的一个化学反应方程式________.
(3)若E为环状化合物,则其结构简式________.
查看答案和解析>>
科目: 来源:广东华附2008届高三5月月考化学试卷 题型:022
下图是部分元素的单质及其化合物的转化关系图(有关反应的条件及部分反应物或生成物已略去);
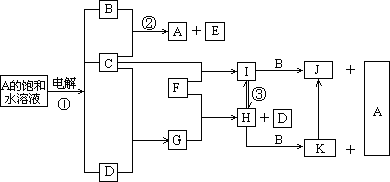
已知:C、D、F均为单质,其中C、D在常温、常压下是气体;反应②是化工生产中的重要反应,生成物E具有漂白性;J、K均为不溶于水的沉淀,其中J为红褐色.
请回答下列问题:
(1)A的电子式:________;
(2)反应②的离子方程式是________;
(3)反应③的化学方程式是________;
(4)实验室由H制备少量K的方法:是用胶头滴管吸取B溶液,将滴管尖端插入盛有新制H溶液试管底部,慢慢挤出B溶液即可,观察到的现象为:
________________________________________________;
(5)当有1.12 L(标准状况)D生成时,反应①中转移的电子数为________;
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com