
科目: 来源:重庆南开中学高2008级高三月考(5月)理科综合能力测试试卷(化学部分) 题型:022
(1)已知pH=2的高碘酸(H5IO6)溶液与pH=12的NaOH溶液等体积混合,所得混合液显酸性;0.0l mol/L的碘酸(HIO3)或高锰酸(HMnO4溶液与pH=12的NaOH溶液等体积混合,所得混合液显中性.请回答:
①高碘酸是______(填“强酸”或“弱酸”,以下同),高锰酸是________
②已知高碘酸和硫酸锰(MnSO4)在溶液中反应生成高锰酸、碘酸和硫酸,反应的离子方程式为_______________________________________________.
(2)在恒温恒容的密闭容器中通入l mol N2和X mol H2发生如下反应;![]() .
.
达到平衡后,测得反应放出的热量为18.4 kJ,混合气体的物质的量为3.6 mol,容器内的压强变为原来的90%.
①起始时充入H2物质的量为________mol;
②该反应的热化学方程式为________;
③若起始时加入N2、H2、NH3的物质的量分别为a、b、c,达到平衡时各组分物质的量与上述平衡相同.
若维持反应向正方向进行,则起始时c的取值范围是________
若c=2 mol,在相同条件下达到平衡时,该反应吸收的热量为________kJ
查看答案和解析>>
科目: 来源:重庆南开中学高2008级高三月考(5月)理科综合能力测试试卷(化学部分) 题型:022
某有机物X(C12H13O6Br)分子中含有多种官能团,其结构简式为:![]()
(其中Ⅰ、Ⅱ为未知部分的结构允为推测X的分子结构,进行如下图的转化:
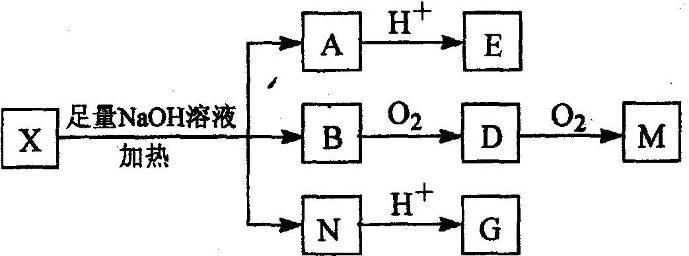
已知向E的水溶液中滴入FeCl3溶液发生显色反应;M(C2H2O4)能使蓝墨水褪色;G、M都能与NaHCO3溶液反应.请回答:
(1)E的结构简式为________
(2)M可以发生的反应有(选填序号)________
①分解反应 ②消去反应 ③氧化反应 ④取代反应
(3)由B转化成D的化学方程式是:________________________
(4)F与G互为同分异构体,F的分子中只含有羧基、羟基和醛基三种官能团,且同一个碳原子上不能同时连有两个羟基.则F的分子结构有________种.
(5)已知在X分子结构中,里含有能与FeCl3溶液发生显色反应的官能团,且E分子中苯环上的一氯代物只有一种,则X的结构简式是________.
查看答案和解析>>
科目: 来源:重庆南开中学高2008级高三月考(5月)理科综合能力测试试卷(化学部分) 题型:022
短周期元素形成的物质A、B、C、D、E,它们的转化关系如下图所示,物质A与物质B之间的反应不在溶液中进行(E可能与A、B两种物质中的某种相同).
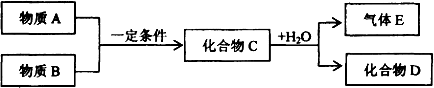
请回答下列问题:
(1)若C是离子化合物,D是一种强碱,写出C的电子式:________
(2)若E具有臭鸡蛋气味,D是既能溶于强酸,又能溶于强碱的化合物.
用电离方程式解释D既能溶于强酸,又能溶于强碱的原因:
_____________________________________________________
用等式表示E与NaOH溶液反应后生成正盐的溶液中所有离子浓度之间的关系:
_____________________________________________________
(3)若C是一种气体,D是一种强酸,且E与A相同,则C与水反应的化学方程式为(请标出电子转移方向和数目):
______________________________________________________
查看答案和解析>>
科目: 来源:山东海阳一中2008年高考模拟考试理科综合化学部分 题型:022
已知:A、H为常见的金属单质,D、F在常温下为气态单质,B为淡黄色固体,J为红褐色沉淀.请按要求填空:
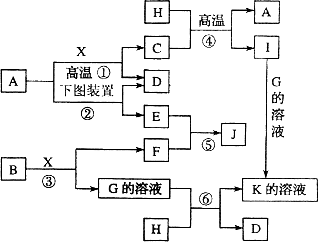
(1)写出B的电子式:____________________________.
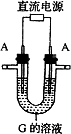
(2)写出用A作电极电解G溶液(如图),在电极上生成E的反
应式________________________.
(3)反应①的化学方程式是___________________________.
反应④在生产中有重要应用,被称为________反应.
(4)反应⑥的离子方程式是________.
查看答案和解析>>
科目: 来源:山东海阳一中2008年高考模拟考试理科综合化学部分 题型:022
化有①0.2 mol/L NaOH溶液和②0.2 mol/L HX溶液,两溶液等体积混合后,测得溶液中c(Na+)>c(X-).则:
(1)①中由水电离出的c(OH)-_______②中由水电离出的c(H+).(填“>”、“=”或“<”)
(2)上述混合液中共存在________种粒子.且:
c(HX)________c(X-).(填“>”、“=”或“<”,下同)
c(HX)+c(X-)________0.1 mol/L(忽略体积变化)
请根据电荷守恒写出一个用离子浓度表示的等式:
____________________________.
(3)上述混合液显________性(填“酸”、“碱”或“中”),其原因用离子方程式表示_____________________________.
查看答案和解析>>
科目: 来源:江苏省通州市石港中学2008届高三化学科押宝卷 题型:022
《物质的结构与性质》
(1)下面是几种物质的溶解度数据:


上述数据可以说明,结构相似的一类固体,在液体中的溶解度的规律是__________________________________;
结构相似的一类气体,在液体中的溶解度的规律是___________________________.
固体和气体在液体中的溶解度呈现上述规律的原因是__________________________________.
(2)①第四周期元素电子排布的能级能量由低到高依次为4s、3d、4p,第六周期元素电子排布的能级能量由低到高依次为:__________________.
②若某元素价电子为3d74s2,则该元素位于元素周期表的第________周期,________族,原子序数为________,其原子的核外电子中成单电子有________个.
查看答案和解析>>
科目: 来源:江苏省通州市石港中学2008届高三化学科押宝卷 题型:022
某种优质燃料油由甲、乙两种有机物混合而成,甲、乙两种物质含有C、H、O三种元素中的两种或三种.已知甲、乙及CO、H2的燃烧热如下:

取甲、乙按不同比例混合的燃油23 g,在足量的氧气中燃烧时,放出的热量Q与混合物中乙的质量分数x的关系如下图所示.试求:
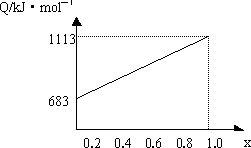
(1)乙的相对分子质量Mr=________.
(2)160 g由甲、乙以等物质的量混合而成的燃油在347.2 L O2中恰好完全燃烧,得492.8 L气体,冷却至室温时,还剩余224 L(气体体积均在标准状态下测定)气体.由此可求得混合物中C、H、O的原子个数比为________;甲、乙的分子式为:甲________;乙________.
(3)1 mol由甲、乙以等物质的量混合而成的燃油在一定量的氧气中燃烧,放出热量2876 kJ/mol,则反应中生成CO________mol.
查看答案和解析>>
科目: 来源:江苏省通州市石港中学2008届高三化学科押宝卷 题型:022
以下由A→G的合成路线叫做“Krohnke反应”:
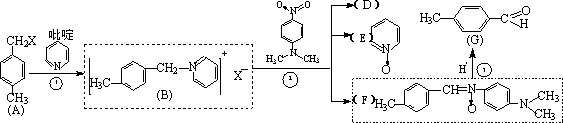
A物质中与苯环相连的“-CH2X”叫做“苄基”.请回答下列问题:
(1)物质A在酸性KMnO4溶液中两个侧链均可被氧化,其有机产物的名称叫做________;把A与NaOH水溶液共热,所得到的有机产物的结构简式为________.
(2)反应②产物中D物质的化学式为________;用足量的H2还原吡啶,所得的产物的结构简式为________.
(3)物质G与银氨溶液反应的化学方程式为:________.
(4)物质A与烧碱溶液共热的反应类型属于________反应,产物B的水溶性为________(填:可溶于水、或不溶于水).
(5)对比问题(1)的两个反应,“Krohnke反应”在有机合成中的作用是:
_______________________________.
查看答案和解析>>
科目: 来源:江苏省通州市石港中学2008届高三化学科押宝卷 题型:022
反应Fe(s)+CO2(g)![]() FeO(s)+CO(g)的平衡常数为K1;反应Fe(s)+H2O(g)
FeO(s)+CO(g)的平衡常数为K1;反应Fe(s)+H2O(g) ![]() FeO(s)+H2(g)的平衡常数为K2.在不同温度时的K1、K2的值如下表:
FeO(s)+H2(g)的平衡常数为K2.在不同温度时的K1、K2的值如下表:

(1)推导反应COz(g)+Hz(g)![]() CO(G)+HzO(g)的平衡常数K与K1、K2的的关系式:________.
CO(G)+HzO(g)的平衡常数K与K1、K2的的关系式:________.
(2)计算K值:温度为973 K时:K=________;温度为1173K时:K=________.通过K值的计算可知,反应COz(g)+Hz(g)![]() CO(g)+H2O(g)是________反应(填“吸热”或“放热”).
CO(g)+H2O(g)是________反应(填“吸热”或“放热”).
(3)在一体积为10 L的密闭容器中,加入一定量的CO2和H2O(g),在1173 K时发生反应并记录前5 min的浓度,第6 min时改变了反应条件.各物质浓度变化(mol/L)见下表:

①前2 min,用CO表示的该化学反应速率是________.
②在3 min~4 min之间,反应处于________状态(填“平衡”或“非平衡”).
③第6 min时,平衡向________方向移动,可能的原因是________.
查看答案和解析>>
科目: 来源:江苏省通州市石港中学2008届高三化学科押宝卷 题型:022
| |||||||||||||||||||||||||||
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com