
科目: 来源:江苏省扬中高级中学2007-2008届高三化学第二次月考化学试卷 题型:022
有机粘合剂的粘合过程一般是液态的小分子粘合剂经化学反应转化为大分子或高分子而固化.
(1)“502胶”是一种快干胶,其主要成分为α-氰基丙烯酸乙酯(![]() ),请写出“502胶”发生粘合作用的化学方程式:
),请写出“502胶”发生粘合作用的化学方程式:
________________________________________________
(2)厌氧胶(![]() )也是一种粘合剂,工业上用丙烯酸和某物质在一定条件下反应可制得这种粘合剂.这一制取过程的化学方程式为
)也是一种粘合剂,工业上用丙烯酸和某物质在一定条件下反应可制得这种粘合剂.这一制取过程的化学方程式为
________________________________________________
(3)白乳胶是常用的粘合剂,其主要成分为醋酸乙烯酯(CH3COOCH=CH2),它有多种同分异构体,如![]() .已知含有
.已知含有![]() 结构的物质不能稳定存在.请另外任写其3种含-CH=CH-结构的链状同分异构体的结构简式:________________、____________________、_________________________;
结构的物质不能稳定存在.请另外任写其3种含-CH=CH-结构的链状同分异构体的结构简式:________________、____________________、_________________________;
(4)已知醇和醛可以发生反应:![]() ,聚乙烯醇
,聚乙烯醇![]() 可用做普通胶水,它的羟基可全部与丁醛(CH3CH2CH2CHO)缩合脱水,得到含六原子环的强力粘合剂聚乙烯缩丁醛.请写出制取聚乙烯缩丁醛的化学方程式:
可用做普通胶水,它的羟基可全部与丁醛(CH3CH2CH2CHO)缩合脱水,得到含六原子环的强力粘合剂聚乙烯缩丁醛.请写出制取聚乙烯缩丁醛的化学方程式:
_________________________________________________________
查看答案和解析>>
科目: 来源:江苏省扬中高级中学2007-2008届高三化学第二次月考化学试卷 题型:022
(1)下表列有四种物质的沸点
①从表中的数据,结合学过的化学知识,你能得到的规律是________________.
②以上四种物质中,属于共价化合物的是________________________.
③若你得到的规律具有普遍性,则以下两种物质的沸点高低是:LiCl________BCl3(填“>”、“=”、“<”).
(2)在密闭容器中,将1.0mol CO与1.0mol H2O混合加热到800℃,发生下列反应:
CO(g)+H2O(g)![]() CO2(g)+H2(g)
CO2(g)+H2(g)
一段时间后该反应达到平衡,测得CO的物质的量为0.5 mol.
回答下列问题:
①平衡时CO的转化率为________,该反应的化学平衡常数为________.
②如果继续向该平衡体系中通入1.0 mol的H2O(g),相同条件下反应达到新的平衡状态,则CO的转化率将________(填“增大”、“减小”、“不变”),预计CO的转化率为________.
③427℃时该反应的平衡常数为9.4,请结合①中的计算结果判断该反应的ΔH________0(填“>”、“=”、“<”).
查看答案和解析>>
科目: 来源:高三化学期中试卷 题型:022
位于短周期的四种主族元素A、B、C、D,原子序数依次增大,已知A、C位于同一主族,A在周期表中原子半径最小.B、D的最外层电子数相等,且B、D的原子序数之和为A、C原子序数之和的两倍.E是自然界中含量最高的金属.根据你的推断回答下列问题:( )
(1)B元素的名称为________E的元素符号:________
(2)由A、B两种元素形成的原子个数比为1∶1的化合物的电子式________
(3)写出由上述元素形成的具有漂白作用的四种物质的化学式________、________、________
(4)用电子式表示C与D形成化合物的过程________
(5)写出E的最高价氧化物与强碱反应的离子方程式________
(6)仅由B、C、D三种元素形成的一种盐,溶于从后呈碱性,请用一个离子方程式表示其呈碱性的原因:________
查看答案和解析>>
科目: 来源:江苏省启东市中学2008届高考化学一轮复习周周测 题型:022
某待测溶液中可能含有Fe2+、Fe3+、Ag+、Al3+、Ba2+、Ca2+、NH4+等离子,进行如下实验(所加酸、碱、氨水、溴水CO2都是过量的).
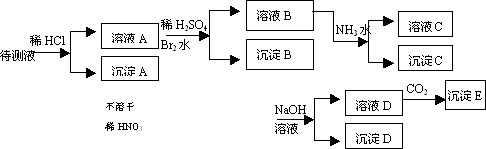
根据实验结果:
(1)判定待测液中有无Ba2+、Ca2+离子:________________________________.
理由是:___________________________________________________.
(2)写出沉淀D的分子式:__________________________.
(3)写出从溶液D生成沉淀E的反应的离子方程式:______________________.
(4)写出从溶液B生成沉淀C的反应的离子方程式:________________________.
查看答案和解析>>
科目: 来源:江苏省启东市中学2008届高考化学一轮复习周周测 题型:022
工业上制取CuCl2的生产流程如下:

请结合下表数据,回答下列问题:

(1)溶液A中加入NaClO的目的是__________________________;
(2)在溶液B中加入CuO的作用是__________________________;
(3)操作a的目的是_______________________________________;
(4)在Cu(OH)2加入盐酸使Cu(OH)2转变为CuCl2.采用多量盐酸和低温蒸干的目的是_______________________________________.
查看答案和解析>>
科目: 来源:江苏省高淳高级中学2008届高三质量检测化学试卷 题型:022
我国化工专家侯德榜的“侯氏制碱法”曾为世界制碱工业做出了突出贡献.他以NaCl、NH3、CO2等为原料先制得NaHCO3,进而生产出纯碱.有关反应的化学方程式为:NH3+CO2+H2O![]() NH4HCO3;NH4HCO3+NaCl
NH4HCO3;NH4HCO3+NaCl![]() NaHCO3↓+NH4Cl;2NaHCO3
NaHCO3↓+NH4Cl;2NaHCO3![]() Na2CO3+CO2↑+H2O
Na2CO3+CO2↑+H2O
(1)碳酸氢铵与饱和食盐水反应,能析出碳酸氢钠晶体的原因是________(填字母标号).
a.碳酸氢钠难溶于水
b.碳酸氢钠受热易分解
c.碳酸氢钠的溶解度相对较小,所以在溶液中首先结晶析出
(2)某探究活动小组根据上述制碱原理,进行碳酸氢钠的制备实验,同学们按各自设计的方案实验.
①一位同学将二氧化碳气体通入含氨的饱和食盐水中制备碳酸氢钠,实验装置如下图所示(图中夹持、固定用的仪器未画出).

试回答下列有关问题:
(Ⅰ)乙装置中的试剂是________;
(Ⅱ)丁装置中稀硫酸的作用是________;
(Ⅲ)实验结束后,分离出NaHCO3晶体的操作是________(填分离操作的名称).
②另一位同学用图中戊装置(其它装置未画出)进行实验.
(Ⅰ)实验时,须先从________管通入________气体,再从________管中通入________气体;
(Ⅱ)有同学建议在戊装置的b管下端连接己装置,理由是_____________;
(3)请你再写出一种实验室制取少量碳酸氢钠的方法:__________________.
查看答案和解析>>
科目: 来源:湖北省武汉市部分学校2007-2008高三起点调研测试化学试卷 题型:022
已知:a、苯的同系物与卤素单质混合,在光照条件下,侧链上的氢原子易被卤素原子取代;在催化剂作用下,苯环上的氢原子易被卤素原子取代.
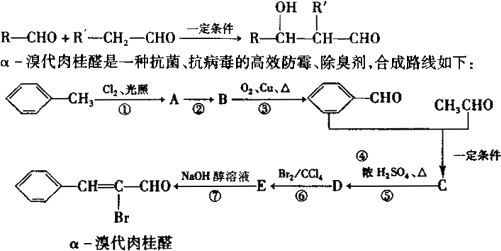
请回答:
(1)写出下列反应类型:
反应②________,反应⑤________.
(2)C的结构简式为___________________________.
(3)反应③的化学方程式为_____________________.
(4)经反应⑦得到的有机产物除α-溴代肉桂醛外,还有可能得到的有机物结构简式为(写出一种即可)____________________.
(5)C的同分异构体中,苯环上只有一个取代基,且属于酯类的有6种

查看答案和解析>>
科目: 来源:黑龙江重点中学鸡西一中2008高考化学模拟题一 题型:022
如图中A至L分别表示反应中的一种常见物质,E、F、I在通常情况下是气体单质,其中E有刺激性气体,X、Y是常见的金属单质.W是由甲、乙两种元素按1∶1组成,其中甲元素的原子M层电子数是K层的一半.乙元素的原子最外层电子数是次外层电子数的3倍,参加反应的水和生成的水已从图中略去.
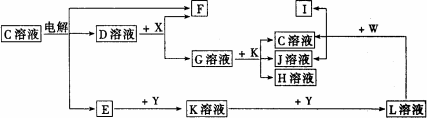
填写下列空白:
(1)E是________(化学式),Y元素在周期表中的位置是____________________.
(2)用电子式表示W的形成过程__________________________.
(3)写出K+G→H+J+C的离子方程式____________________________.
(4)设计实验分离H和J(写出加入试剂和操作方法):_______________.
查看答案和解析>>
科目: 来源:黑龙江重点中学鸡西一中2008高考化学模拟题一 题型:022
氨基钠(NaNH2)是碱性很强的离子化合物,在液氨中,氯苯与氨基钠作用生成苯胺(![]() ),反应经历了中间体苯炔(
),反应经历了中间体苯炔(![]() )这一步
)这一步
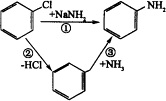
(1)如果将反应按加成、取代、消去分类,则反应①属________反应,反应②属________反应,反应③属________反应.
(2)如果用14C标识与氯原子相连的碳原子(其余的碳原子均为12C),那么,这种氯苯与氨基钠在液氨中反应,支持反应必定经历中间体苯炔这一步的事实是(从下列选出)____________________________.
A.产物苯胺只有一种,氨基全部连在14C上
B.产物苯胺有两种,氨基连在14C上比连在相邻的12C上的多
C.产物苯胺有两种,氨基连在14C上和连在相邻的12C的一样多
(3)苯胺可以由硝基苯与铁、稀盐酸反应得到,写出反应的化学方程式:________________.
查看答案和解析>>
科目: 来源:黑龙江重点中学鸡西一中2008高考化学模拟题一 题型:022
下面是某研制人员为合成药物苯氟布洛芬所设计的线路:
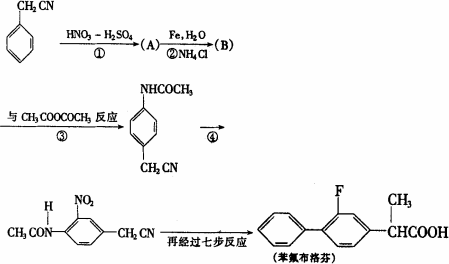
回答下列问题:
(1)苯氟布洛芬的分子式为________;该分子最多有________个碳原子共平面.
(2)物质A、B的结构简式分别为:________,________.
(3)反应①~④中属于取代反应的是_______________________(填反应代号).
(4)写出反应③的化学方程式(有机物写结构简式):____________________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com