
科目: 来源:贵州省凯里一中2009届第二轮限时训练理综化学(4) 题型:022
铝、铁和氯是三种运用广泛的元素.
(1)写出FeCl3溶液腐蚀印刷电路铜板的离子方程式________,若将此反应设计成原电池,写出电极反应式:正极反应________,负极反应________.
(2)工业上用电解饱和食盐水的方法制取氯气,制得的氯气与另一电解产物在一定条件下反应生成两种盐A和B,其物质的量比为5∶1,则盐A和B的化学式依次为________,盐B在酸性条件下可与草酸(H2C2O4)反应制得气体ClO2,写出该反应的离子方程式:________,ClO2是当前对饮用水进行消毒的一种高效消毒剂,物质的量相等的ClO2和Cl2相比较,ClO2的消毒杀菌能力是Cl2的________倍.
(3)生产中常用铝热反应焊接钢轨,反应的化学方程式为________;同温同压下,在浓度均为2 mol/L,体积均为100 mL的盐酸和NaOH溶液中分别加入等质量的铝,产生气体的体积比为5∶6,则加入铝的质量为________g.
查看答案和解析>>
科目: 来源:贵州省凯里一中2009届第二轮限时训练理综化学(4) 题型:022
A、B、C、D、E、F六种物质的相互转化关系如图所示:

(1)若A是常见的金属单质,能与B的水溶液反应生成C和D,D、F是气体单质.则A元素在元素周期表中的位置为________,反应②的离子方程式为________.
(2)若A、D、F都是非金属单质,且A、D所含元素同主族,A、F所含元素同周期,则物质B的化学式为________,物质E的电子式为________,B和E在固态时分别属于________晶体和________晶体.
(3)若A为Mg,D为一种常见非金属单质,且③④两个反应都有红棕色气体产生,则反应①和④的化学方程式分别为:
①________________________________________;
④________________________________________.
查看答案和解析>>
科目: 来源:贵州省凯里一中2009届第二轮限时训练理综化学(3) 题型:022
已知一个碳原子上连有两个羟基时,易发生下列转化:
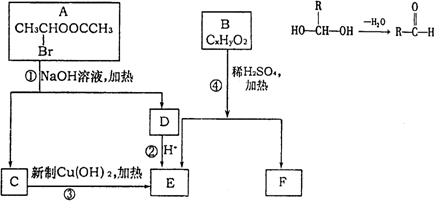
请根据上图回答:
(1)E中含有的官能团的名称是:________;反应③的化学方程式为:________.
(2)已知B的相对分子质量为162,其完全燃烧的产物中n(CO2)∶n(H2O)=2∶1,则B的分子式为________.
(3)F是高分子光阻剂生产中的主要原料.F具有如下特点:①能跟FeCl3溶液发生显色反应;②能发生加聚反应;③苯环上的一氯代物只有两种.F在一定条件下发一加聚反应的化学方程式为________.
(4)化合物G是F的同分异构体,属于芳香族化合物,能发生银镜反应.G有多种结构,写出其中两种苯环上取代基个数不同的同分异构体的结构简式________、________.
查看答案和解析>>
科目: 来源:贵州省凯里一中2009届第二轮限时训练理综化学(3) 题型:022
B是一种人体不可缺少的无色无味的液体;C是一种有磁性的化合物;E是一种无色、无味的有毒气体,是常用的还原剂,根据下列关系图,完成本题:
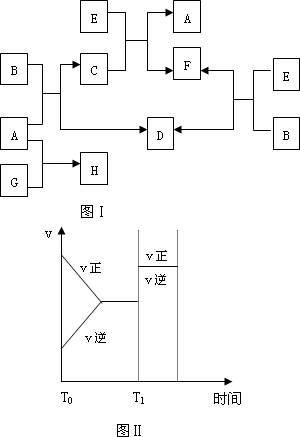
(1)写出B、C的化学式:B________,C________
(2)E和N2结构相似,请写出E的化学式:E________
(3)在101千帕和150℃时,可逆反应E+B![]() F+D反应速率和时间的关系如图Ⅱ所示,那么在T1时速率发生改变的原因可能是:________(填选项)
F+D反应速率和时间的关系如图Ⅱ所示,那么在T1时速率发生改变的原因可能是:________(填选项)
A.升高温度 B.增大压强 C.加入催化剂
(4)若G是一种淡黄色固体单质,16克的G和足量的A反应放出的热量为QkJ(Q>0),写出这个反应的热化学方程式:________若G是一种气态单质,H的水溶液可以和有机物I反应使溶液呈紫色,请写出G、I的分子式:________,________;H的水溶液呈酸性,请用化学方程式表示呈酸性的原因:________________
查看答案和解析>>
科目: 来源:贵州省凯里一中2009届第二轮限时训练理综化学(2) 题型:022
苯乙烯(![]() )与A、B、C、D、E、F、G、H、I等有机化合物之间存在如下图所示转化关系.
)与A、B、C、D、E、F、G、H、I等有机化合物之间存在如下图所示转化关系.
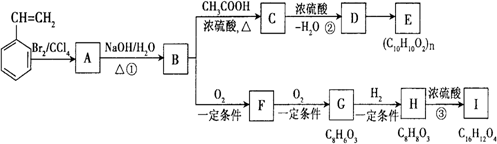
请回答下列问题:
(1)反应①、②的反应类型分别是________、________.
(2)C可能的结构简式有________.
(3)H有多种同分异构体.符合下列条件的同分异构体共有________种.
①与FeCl3溶液发生显色反应;
②1 mol H最多能与3 mol NaOH反应;
③苯环上只有两个取代基.
其中,任意一种同分异构体的结构简式为________.
(4)反应③的化学方程式是________.
(5)聚苯乙烯可用于制备高频绝缘材料.由苯乙烯合成这种高聚物的化学方程式为______________________________________.
查看答案和解析>>
科目: 来源:贵州省凯里一中2009届第二轮限时训练理综化学(2) 题型:022
中学常见物质A、B、D、E、G、M、Q之间有如下图所示变化关系(反应条件已省略):
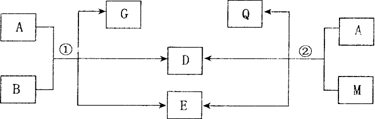
(1)若A是黑色非金属固体单质,G、Q、D是气体,E是水,D的化学式为________.
(2)若A是红色金属,B、M是同种溶质不同浓度的溶液,G、Q是气体,且G可通过化合反应生成Q.反应①的离子方程式是________.
(3)若A是Ca(OH)2,D是极易溶于水的气体.
①工业上合成D使用铁触媒作催化剂,采用500℃左右、20MPa-50MPa为生产条件的原因有________(填标号).
a.化学反应速率最大
b.催化剂的活性最大
c.反应物转化率最大
d.综合经济效益较好
上述反应中,每生成l mol D时放出热量46.2 kJ,该反应的热化学方程式是:
____________________________________
②当l mol Ca(OH)2分别与B、M完全反应时,反应①、②生成的D的物质的量之比为2∶1,B、M的化学式分别为________、________.
查看答案和解析>>
科目: 来源:贵州省凯里一中2009届第二轮限时训练理综化学(2) 题型:022
短周期元素A、B、C、D、E的原子序数依次增大,A与C、B与D分别同主族.A与E能形成化学式为AE型的共价化合物,C与D能形成化学式为C2D型的离子化合物.
(1)AE的电子式为________.
(2)C的单质在B的单质中燃烧,生成物中含有的化学键为________.
(3)用惰性电极电解C2DB4的水溶液时,阳极反应式为________.
(4)与C同周期的某金属元素单质,溶于由A、B、C三种元素组成的化合物的水溶液时,反应的离子方程式为________.
(5)由B、C.D三种元素组成的某化合物,与稀硫酸反应并生成沉淀的化学方程式为_______________________________.
查看答案和解析>>
科目: 来源:贵州省凯里一中2009届第二轮限时训练理综化学(1) 题型:022
D、E、X、Y、Z是周期表中的前20号元素,且原子序数逐渐增大.它们的最简氢化物分子的空间构型依次是正四面体、三角锥形、正四面体、角形(V形)、直线形.回答下列问题:
(1)Y的最高价氧化物的化学式为________;
(2)上述5种元素中,能形成酸性最强的含氧酸的元素是________,写出该元素的任意3种含氧酸的化学式:________;
(3)D和Y形成的化合物,其分子的空间构型为________;
(4)D和X形成的化合物,其化学键类型属________,其晶体类型属________;
(5)金属镁和E的单质在高温下反应得到的产物是________,此产物与水反应生成两种碱,该反应的化学方程式是________;
(6)试比较D和X的最高价氧化物熔点的高低并说明理由:
______________________________________________
查看答案和解析>>
科目: 来源:贵州省白云二中2009年化学综合测试卷两套 题型:022
V、W、X、Y、Z是由周期表中1~20号部分元素组成的5种化合物,其中V、W、X、Z均为两种元素组成.上述5中化合物涉及的所有元素的原子序数之和等于35.它们之间的反应关系如下图:
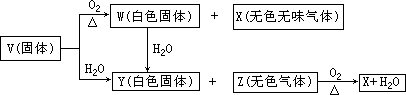
(1)5种化合物分别是V________、W________、X________、Y________、Z________;(填化学式)
(2)由上述5中化合物中的某2种化合物反应可生成一种新化合物,它包含了5种化合物中的所有元素,生成该化合物的化学方程式是________;
(3)V的电子式是________.
查看答案和解析>>
科目: 来源:贵州省白云二中2009年化学综合测试卷两套 题型:022
在2008年初我国南方遭遇的冰雪灾害中,使用了一种融雪剂,其主要成分的化学式为XY2,X、Y均为周期表前20号元素,其阳离子和阴离子的电子层结构相同,且1 mol XY2含有54 mol电子.
(1)该融雪剂的化学式是________;X与氢元素形成的化合物的电子式是________.
(2)元素D、E原子的最外层电子数是其电子层数的2倍,D与Y相邻,则D的离子结构示意图是________;D与E能形成一种非极性分子,该分子的结构式为________;D所在族元素的氢化物中,沸点最低的是________.
(3)元素W与Y同周期,其单质是原子晶体;元素Z的单质分子Z2中有3个共价健;W与Z能形成一种新型无机非金属材料,其化学式是________.
(4)元素R与Y同主族,其氢化物能用于刻蚀玻璃,R2与NaOH溶液反应的产物之一是OR2,该反应的离子方程式为________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com