
科目: 来源:2008-2009学年度济宁市育才中学高三阶段性测试、化学试卷 题型:022
物质A-H有如下图所示转化关系(部分反应物、生成物没有列出).其中,B的浓溶液与单质X在加热时才能发生反应①,B的稀溶液与足量X发生反应②,向C溶液中滴入KSCN溶液呈红色.试填写下列空白:
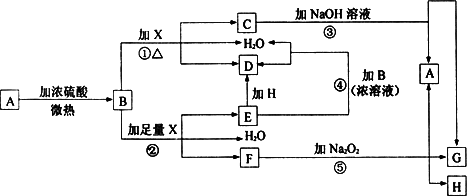
(1)晶体A的化学式_________________
(2)反应②的离子反应方程式为________
(3)根据图示信息判断,足量B的浓溶液与单质X共热时能否产生E,说明理由(用化学方程式回答)____________________
(4)在反应⑤中,若生成物G与H的物质的量之比为4∶1,写出F溶液与Na2O2反应的化学方程式___________________
查看答案和解析>>
科目: 来源:2008-2009学年度济宁市育才中学高三阶段性测试、化学试卷 题型:022
使一定量Zn与100 ml 18.5 mol·L-1浓H2SO4充分反应,Zn完全溶解,同时生成标准状况下气体33.6 L.将反应后溶液稀释,测得其PH=1.0.求:
(1)生成气体的成分及体积(假设浓H2SO4与Zn反应还原产物只生成SO2)________;
(2)参加反应的Zn的质量________;
(3)开始生成H2时H2SO4的浓度(假设溶液体积无变化)________.
查看答案和解析>>
科目: 来源:2008-2009学年度济宁市育才中学高三阶段性测试、化学试卷 题型:022
某未知溶液可能由多种常见的阳离子和阴离子混合成,已知其中无Zn2+,为了确定其组成,做了如下所示的实验.

(1)未知液中肯定存在的离子有:__________________
(2)不能肯定存在的离子:________,理由是________
(3)判断Fe2+和Fe3+是否存在的依据是______________.
(4)生成D的离子方程式为________________________.
查看答案和解析>>
科目: 来源:2007-2008学年上海市嘉定一中第一学期高三年级测试(二)、化学试题 题型:022
据2004年1月17日报道,意大利科学家使用普通氧化子和带正电的氧化离子作用,制出了新型的氧分子O4,它的结构很复杂,可能具有与S4相似的长方形结构.
(1)下列有关O4的说法正确的是________
A.O4分子内存在极性共价健
B.合成O4的反应可看互核聚变反应,即不属于化学反应
C.O4与O3、O2都是氧的同素异形体
D.O4将来可用作更强有力的火箭推进的氧化剂
(2)制备含O-2、O2-2甚至O+2的化合物都是可能的,通常它们在氧分子进行下列各种反应时生成的:
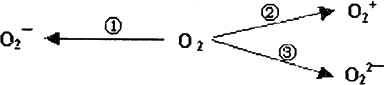
上述反应中,________(填序号)相当于氧分子被氧化;________(填序号)相当于氧分子被还原.
(3)写出O2-2的电子式:________
(4)O2[PtF6]是一种含有O+2的化合物,请写出一种含有O-2的化合物的化学式
___________________
查看答案和解析>>
科目: 来源:2007-2008学年上海市嘉定一中第一学期高三年级测试(二)、化学试题 题型:022
有A、B、C、D、E、F六种短周期元素,原子序数依次增大,其中A、D元素的原子最外层电子均只有一个电子,且A和D可形成离子化合物;C、F同主族,B元素位于元素周期表中第二周期,且原子最外层电子数占核外电子总数的3/4;F元素原子最外电子层比同周期的E元素原子的最外层多4个电子,请回答:
(1)写出A、D两种元素组成的化合物的电子式________;
(2)写出B、D、E三种元素组成的常见化合物的名称________;
(3)工业生产E的方法是________;
(4)D、F两元素最高价氧化物的水化物之间发生的反应的化学方程式
_________________
(5)D的氢氧化物和C的氢化物在水溶液中反应的离子方程式为
_________________
查看答案和解析>>
科目: 来源:2007-2008学年上海市嘉定一中第一学期高三年级测试(二)、化学试题 题型:022
高炉炼铁的基本反应之一如下:
FeO(s)+CO(g)![]() Fe(s)+CO2(g)-Q
Fe(s)+CO2(g)-Q
该反应达到平衡时,![]() 是一个常数(用K表示),已知1100℃时,K=0.263.
是一个常数(用K表示),已知1100℃时,K=0.263.
(1)温度升高,化学平衡移动后达到新的平衡,高炉内CO2和CO的体积比值________,K值________(填“增大”“减小”或“不变”)
(2)1100℃时测得高炉中c(CO2)=0.025 mol·L-1,c(CO)=0.1 mol·L-1,此时该反应是否处于化学平衡状态________,此时化学反应速度是v正________v逆,其原因是________.
查看答案和解析>>
科目: 来源:2007-2008学年海南东方铁路中学高三第一学期化学期末考试 题型:022
A、B、C、D、E、F是常见单质,其中A是用量最大,应用最广泛的金属;元素D是地壳中含量最多的金属元素;D元素和E元素在周期表中相邻.G、H、I、J、K、L是常见化合物,其中G在常温下是无色液体,H是黑色固体.以上物质相互间的转化关系如下图所示:
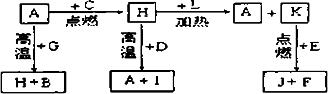
请回答下列问题:
(1)元素A在元素周期表中的位置为________周期________族.
(2)写出K的电子式________.
(3)写出H和D反应的化学方程式________.
(4)D能与氢氧化钠溶液反应,请写出该反应的离子方程式________.
查看答案和解析>>
科目: 来源:2007-2008年北京四中高三年级第一学期期中测验、化学试卷 题型:022
A为药用有机物,从A出发可发生图5所示的一系反应.已知A在一定条件下能跟醇发生酯化反应,A分子中苯环上的两个取代基连在相邻的碳原子上;D不能跟NaHCO3溶液反应,但能跟NaOH溶液反应.
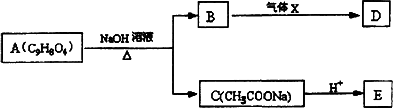
试回答:
(1)A转化为B、C时,涉及到的反应类型是有________、________;
(2)E的两种同分异构体Q、R都能在一定条件下发生银镜反应,R能跟金属钠反应放出氢气,而Q不能.Q、R的结构简式分别为:
Q________、R________.
(3)气体X的化学式为________,D的结构简式为________;
(4)A的加热条件下与NaOH溶液反应的化学方程式为________.
(5)试分析A在NaOH溶液并加热的条件下进行反应的原因是________.
查看答案和解析>>
科目: 来源:2007-2008年北京四中高三年级第一学期期中测验、化学试卷 题型:022
氧化还原反应中实际上包含氧化和还原两个过程.下面是一个还原过程的反应式:NO3-+4H++3e-→NO↑+2H2O,KMnO4、Na2CO3、Cu2O、Fe(SO4)3四种物质中的一种物质(甲)能使上述还原过程发生.
(1)写出并配平该氧化还原反应的化学方程式:________
(2)反应中硝酸体现了________、________性质
(3)反应中若产生0.2 mol气体,则转移电子的物质的量是________mol.
(4)若1 mol甲与某浓度硝酸反应时,被还原硝酸的物质的量增加,原因是:
_____________________.
查看答案和解析>>
科目: 来源:2008年普通高等学校招生全国统一考试(上海卷)、化学 题型:022
已知:CH2=CH-CH=CH2+CH2=CH2![]()
![]() ,物质A在体内脱氢酶的作用下会氧化为有害物质GHB.下图是关于物质A的一种制备方法及由A引发的一系列化学反应.
,物质A在体内脱氢酶的作用下会氧化为有害物质GHB.下图是关于物质A的一种制备方法及由A引发的一系列化学反应.
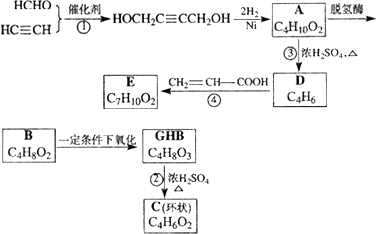
请回答下列问题:
(1)写出反应类型 反应①________ 反应 ③________.
(2)写出化合物B的结构简式________.
(3)写出反应②的化学方程式________.
(4)写出反应④的化学方程式________.
(5)反应④中除生成外,还可能存在一种副产物(含![]() 结构),它的结构简式为________.
结构),它的结构简式为________.
(6)与化合物互为同分异构体的物质不可能为________(填写字母).
a.醇 b.醛 c.羧酸 d.酚
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com