
科目: 来源:湖南省长沙市一中2009-2010年高三第二次月考 化学试卷 题型:022
混合物A,含有KAl(SO4)2、Al2O3和Fe2O3,在一定条件下可实现下图所示的物质之间的变化:
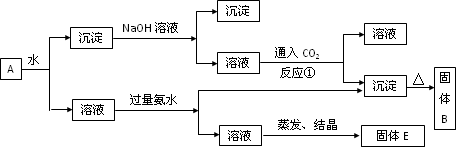
据此判断:
(1)固体B所含物质的化学式为________.
(2)固体E所含物质的化学式为________.
(3)反应①的离子方程式为________.
查看答案和解析>>
科目: 来源:湖南省长沙市一中2009-2010年高三第二次月考 化学试卷 题型:022
将2.5 g碳酸钠、碳酸氢钠和氢氧化钠的固体混合物完全溶解于水,制成稀溶液,然后向该溶液中逐滴加入1 mol·L-1的盐酸,所加入盐酸的体积与产生CO2的体积(标准状况)关系如下图所示:

(1)写出OA段所发生反应的离子方程式________、________.
(2)当加入35 mL盐酸时,产生CO2的体积为________mL(标准状况).
(3)原混合物中NaOH的质量为________g,碳酸钠的质量分数为________.
查看答案和解析>>
科目: 来源:黑龙江省哈师大附中2010届高三上学期第一次月考化学试题 题型:022
根据下列框图回答问题(答题时,方程式中的M、E用所对应的元素符号表示):
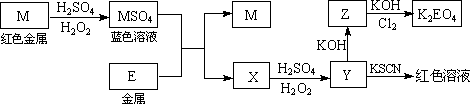
(1)写出M溶于稀H2SO4和H2O2混合液的化学方程式:________.
(2)某同学取X的溶液,酸化后加入KI淀粉溶液,变为蓝色.写出与上述变化过程相关的离子方程式:________、________.
(3)写出Cl2将Z氧化为K2EO4的化学方程式:________.
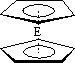
(4)由E制备的E(C5H5)2的结构如图,其中氢原子的化学环境完全相同.但早期人们却错误地认为它的结构为:![]() .核磁共振法能够区分这两种结构.在核磁共振氢谱中,正确的结构有________种峰,错误的结构有________种峰.
.核磁共振法能够区分这两种结构.在核磁共振氢谱中,正确的结构有________种峰,错误的结构有________种峰.
查看答案和解析>>
科目: 来源:黑龙江省哈师大附中2010届高三上学期第一次月考化学试题 题型:022
KClO3和浓盐酸在一定温度下反应会生成黄绿色的易爆物二氧化氯.其变化可
表述为:
□KClO3+□HCl(浓)-□KCl+□Cl2↑+□ClO2↑+□________
(1)配平化学方程式并标出电子转移的方向和数目(未知物化学式和系数填入框内)
(2)浓盐酸在反应中显示出来的性质是________(填写编号,多选倒扣).
①只有还原性
②还原性和酸性
③只有氧化性
④氧化性和酸性
(3)产生0.1 mol Cl2,则转移的电子的物质的量为________.
(4)ClO2具有很强的氧化性.因此,常被用作消毒剂,其消毒的效率(以单位物质的量得到的电子数表示)是Cl2的________倍.
查看答案和解析>>
科目: 来源:黑龙江省哈师大附中2010届高三上学期第一次月考化学试题 题型:022
提示:某些金属氧化物跟熔融烧碱反应可生成盐.根据以下化学反应框图填空:
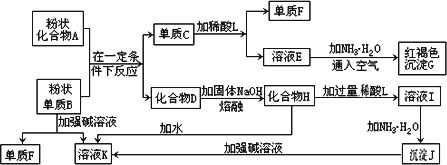
(1)单质F是________.
(2)写出由E生成G的离子反应方程式(或化学方程式)________.
(3)溶液I中所含金属离子是________.
(4)由C→E+F若改用浓酸,则不能选用的浓酸是(写分子式)________、________.
查看答案和解析>>
科目: 来源:黑龙江省哈尔滨三中2010届高三9月月考化学试题 题型:022
下图表示某固态单质A及其化合物之间的转化关系(某些产物和反应条件已略去).化合物B在常温常压下为气体,B和C的相对分子质量之比为4∶5,化合物D是重要的工业原料.
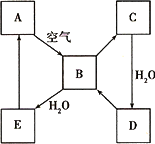
(1)写出A在加热条件下与H2反应的化学方程式________.
(2)写出E与A的氢化物反应生成A的化学方程式________.
(3)写出一个由D生成B的化学方程式________.
(4)将5 mL 0.10 mol·L-1的E溶液与10 mL 0.10 mol·L-1的NaOH溶液混合.
①写出反应的离子方程式________;
②反应后溶液的pH________7(填“大于”、“小于”或“等于”),理由是________;
③加热反应后的溶液,其pH________(填“增大”、“不变”或“减小”),理由是________.
查看答案和解析>>
科目: 来源:黑龙江省哈尔滨三中2010届高三9月月考化学试题 题型:022
在已提取氯化钠、溴、镁等化学物质后的富碘卤水中,采用下面的工艺流程生产单质碘:

试回答:
(1)书写化学式:沉淀甲________,丙中的溶质________.
(2)步骤③中加铁屑的量为________.
(3)第④步操作中用稀H2SO4浸洗的目的是________.(填写字母编号)
a.除去未反应的NO3-
b.除去未反应的I-
c.除去未反应的Fe
d.除去碱性物质
(4)第⑦步提纯操作你认为最合适的是________.(填写字母编号)
A.分液
B.减压蒸馏
C.渗析
D.重结晶
(5)第⑥步操中反应的离子方程式________.
(6)鉴别丙和丁可选用的试剂是________.分离混合物和丁的方法是________.
查看答案和解析>>
科目: 来源:河南省济源一中2010届高三9月月考化学试题 题型:022
下图是一些常见元素的单质或化合物之间的转化关系.溶液中的水以及部分反应物或生成物未标出.A、E是空气中的两种主要成分,C是由两种元素组成的新型材料,且和SiC具有相同的价电子数和原子数,J是一种能引起温室效应的气体,K是两性化合物.反应③、④、⑤用于工业中生产H.回答下列问题:
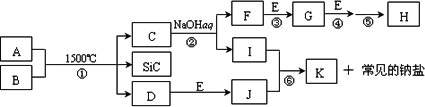
(1)写出下列物质的化学式:F________,I________,H________;
(2)写出反应③的化学方程式:________;
(3)写出反应⑥的离子方程式:________;
(4)B和SiC的纳米级复合粉末是新一代大规模集成电路理想的散热材料.反应①是科学家研究开发制备该纳米级复合粉末的最新途径.已知B由Si及另外两种元素组成,且Si与另外两种元素的物质的量之比均为1∶4,写出反应①的化学方程式:________.
查看答案和解析>>
科目: 来源:广东省湛江市第二中学2009-2010学年度高三第一次月考化学试题 题型:022
已知可逆反应:M(g)+N(g)![]() P(g)+Q(g),ΔH>0,
P(g)+Q(g),ΔH>0,
请回答下列问题:
(1)在某温度下,反应物的起始浓度分别为:c(M)=1 mol·L-1,c(N)=2.4 mol·L-1;达到平衡后,M的转化率为60%,此时N的转化率为________;
(2)若反应温度升高,M的转化率________(填“增大”“减小”或“不变”;)
(3)若反应温度不变,反应物的起始浓度分别为:c(M)=4 mol·L-1,c(N)=a mol·L-1;达到平衡后,c(P)=2 mol·L-1,a=________;
(4)若反应温度不变,反应物的起始浓度为:c(M)=c(N)=b mol·L-1,达到平衡后,M的转化率为________.
查看答案和解析>>
科目: 来源:广东省湛江市第二中学2009-2010学年度高三第一次月考化学试题 题型:022
称取6.0 g含H2C2O4·2H2O、KHC2O4和K2SO4的试样,加水溶解,配成250 mL溶液.量取两份此溶液各25 mL,分别置于两个锥形瓶中.
①第一份溶液中加入2滴酚酞试液,滴加0.25 mol/L NaOH溶液至20 mL时,溶液由无色变为浅红色.该溶液被中和的H+的物质的量为________mol.
②第二份溶液滴加0.10 mol/L酸性KMnO4溶液至16 mL时反应完全,此时溶液颜色,由________变为________.该溶液中还原剂的物质的量________mol.
③原试样中H2C2O4·2H2O的质量分数为________,KHC2O4的质量分数为________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com