
科目: 来源:湖南省衡阳八中2010届高三第四次月考、化学试卷 题型:022
单质A在适宜条件下有如图所示的一系列转化,其中F是一种红褐色物质.
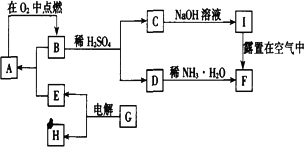
(1)写出下列物质的化学式:A________,B________.
(2)用化学方程式表示下列转化过程B+H2SO4→C+D:________.I露置在空气中转化为F:________.
(3)G
可能是________或________.查看答案和解析>>
科目: 来源:湖南省衡阳八中2010届高三第四次月考、化学试卷 题型:022
W、X、Y和Z都是周期表中前20号元素,已知:
①W的阳离子Y的阴离子核外电子数为18,且能形成组成为WY的化合物;
②Y和Z属同族元素,它们能形成两种常见化合物;
③X和Z属同一周期元素.它们能形成两种气态化合物;
④X是形成化合物最多的元素,且W和X能形成组成为WX2的化合物;
⑤X和Y不在同一周期,它们能形成组成为XY2的化合物.请回答:
(1)W元素是________;Z元素是________.
(2)化合物WY和WX2中WY的电子式是________.
(3)Y和Z形成的两种常见化合物,其中可作漂白剂使用的化合物分子式是________.
(4)写出X的最高价和Z形成的化合物的结构式________.
查看答案和解析>>
科目: 来源:湖南省长沙市一中2010届高三第四次月考、化学试卷 题型:022
已知X为中学化学中的一种常见的盐,F为淡黄色固体;M、N为常见的金属;H为气体单质,D为无色气体,在空气中会出现红棕色.各物质的转化关系如下图(部分反应产物已略去).
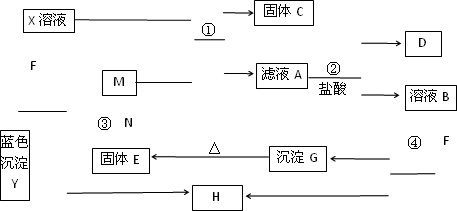
请回答下列问题:
(1)X的化学式为________.
(2)在反应①②③④中属于置换反应的是________(填序号).
(3)反应②的离子方程式为________.
(4)X溶液与F反应的总化学方程式为________.
查看答案和解析>>
科目: 来源:河南省沁阳一中2010届高三第四次月考、化学试卷 题型:022
将一定量的混合均匀的铁粉和硫粉在隔绝空气的条件下共热,充分反应后冷却至室温,得到固体A.将质量为m的固体A加入到300 mL 2 mol·L-1盐酸中使之完全溶解,测得室温下加入的固体A的质量与收集到的气体体积(已换算成标准状况)的关系如图,(假设氢硫酸溶液饱和之前无硫化氢逸出).已知加入固体A的质量m≤3.2 g时,收集到的气体为氢气,当m>3.2 g时收集到的气体为氢气和硫化氢的混合气.
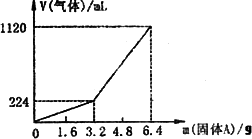
试分析与计算:
(1)3.2 g固体A中所含的物质有(写化学式)________.
(2)3.2 g固体A中各物质的物质的量分别为________.溶于上述盐酸充分反应后,所得的溶液中氢硫酸的物质的量浓度为(忽略体积变化)________.
(3)当固体A全部溶于上述盐酸,且A的质量m>3.2 g时,收集到的气体体积(标准状况下)V=________mL.(用含m的代数式)
查看答案和解析>>
科目: 来源:河南省沁阳一中2010届高三第四次月考、化学试卷 题型:022
下图中,A、C是工业上用途很广的两种重要化工原料,B为日常生活中常见的金属,H、G是正四面体结构的非极性分子,H是一种重要的能源,J是一种耐高温材料,K是由两种常见元素组成的化合物(图中部分反应物或生成物没有列出).
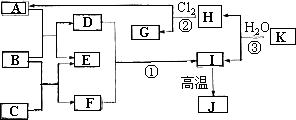
请按要求回答:
(1)写出B的化学式________,G的电子式________.
(2)反应①的离子方程式为________.
(3)反应③的化学方程式为________.
查看答案和解析>>
科目: 来源:河南省沁阳一中2010届高三第四次月考、化学试卷 题型:022
以石墨做电极电解200 mL 0.5 mol/L的CuSO4溶液,在标准状况下,阴极上收集到2.24 L气体时,停止通电.请回答下列问题:
(1)电解过程中阴极的电极反应式为________、________;
(2)电解过程中共收集到气体的体积为________;
(3)若电解前后溶液的体积变化忽略不计,电解后溶液的pH值约为________;
(4)电解结束后,欲使溶液恢复到电解前溶液的组成和浓度,可加入________mol________;
(5)电解时的电流强度为20安培,理论上所需电解时间为________分.(设1 mol电子的电量为96500库仑)
查看答案和解析>>
科目: 来源:山东省淄博市2010届高三上学期期末考试化学试卷 题型:022
从铝土矿(主要成分是Al2O3,含SiO2、Fe2O3、MgO等杂质)中提取氧化铝的两种工艺流程如下:
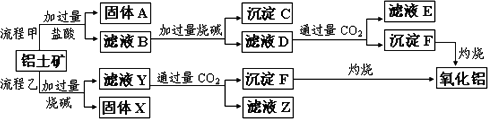
请回答下列问题:
(1)Fe的原子序数为26,Fe位于元素周期表中第________周期,第________族.
(2)流程甲加入盐酸后生成Al3+的离子方程式为________;
流程乙加入烧碱后生成SiO32-的离子方程式为________.
(3)滤液E中溶质的主要成份是________(填化学式),写出该溶液的一种用途:________.
(4)写出检验滤液B中是否含Fe3+离子的方法:
____________________
查看答案和解析>>
科目: 来源:山东省淄博市2010届高三上学期期末考试化学试卷 题型:022
如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,请回答:
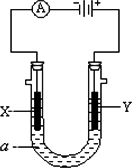
(1)X极上的电极反应式:________.在X极附近观察到的现象是________.
(2)Y电极上的电极反应式为________,检验该电极反应产物的方法是________.
查看答案和解析>>
科目: 来源:山东省淄博市2010届高三上学期期末考试化学试卷 题型:022
| |||||||||||||||||||||||||||
查看答案和解析>>
科目: 来源:福建省泉州市德化县2010届高三上学期期末考试化学试卷 题型:022
| |||||||||||||||||||||||||||||||||||||||||||
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com