
科目: 来源:江苏省南通市2010届高三第二次模拟考试化学试题 题型:022
一种以黄铜矿和硫磺为原料制取铜和其他产物的新工艺,原料的综合利用率较高.其主要流程如下:
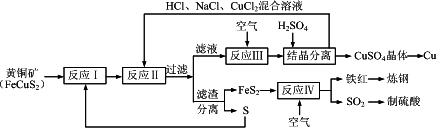
注:反应Ⅱ的离子方程式为Cu2++CuS+4Cl-=2[CuCl2]-+S
请回答下列问题:
(1)反应Ⅰ的产物为(填化学式)________________.
(2)反应Ⅲ的离子方程式为____________.
(3)一定温度下,在反应Ⅲ所得的溶液中加入稀硫酸,可以析出硫酸铜晶体,其原因是___________________.
(4)炼钢时,可将铁红投入熔融的生铁中,该过程中主要反应的化学方程式是________________.
(5)某硫酸厂为测定反应Ⅳ所得气体中SO2的体积分数,取280 mL(已折算成标准状况)气体样品与足量Fe2(SO4)3溶液完全反应后,用浓度为0.02000 mol/L的K2Cr2O7标准溶液滴定至终点,消耗K2Cr2O7溶液25.00 mL.
已知:Cr2O72-+Fe2++H+→Cr3++Fe3++H2O(未配平)
①SO2通入Fe2(SO4)3溶液,发生反应的离子方程式为________.
②反应Ⅳ所得气体中SO2的体积分数为________.
查看答案和解析>>
科目: 来源:江苏省南京市2010届高三第二次模拟考试化学试题 题型:022
高效、低毒农药杀灭菊酯的合成路线如下:
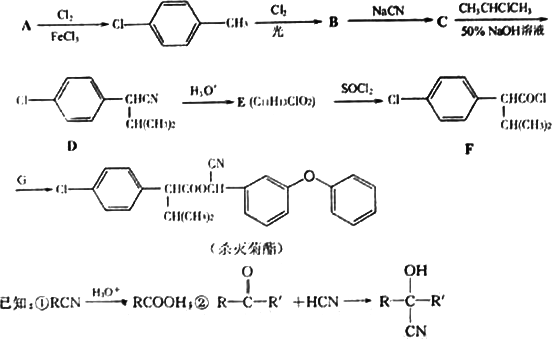
(1)写出A的结构简式________
(2)写出E中官能团的名称________.
(3)写出符合下列条件的E的一种同分异构体的结构简式________.
①苯的衍生物,且苯环上只有两个对位取代基;
②与Na2CO3溶液反应放出CO2气体
③氯原子不与苯环上碳原子相连,且与NaOH醇溶液共热不能发生消去反应;
④分子中含有两个甲基.
(4)G可由一种含有醛基的物质和HCN加成制得,写出合成G的化学方程式________.
(5)请设计合理的方案以丙酮(CH3COCH3)和甲醇为原料合成有机玻璃的单体甲基丙烯酸甲酯
(用合成路线流程图表示,并注明反应条件).
提示:①合成过程中无机试剂任选;
②合成路线流程图示例如下:
![]()
________
查看答案和解析>>
科目: 来源:上海市徐汇区2010届高三第二次模拟考试化学试题 题型:022
已知:①NaNO2具有强氧化性
②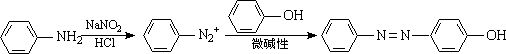
奥沙拉秦是一种抗菌药.其合成路线如下:

(1)写出下列反应的化学方程式:
水杨酸
→A________;A→B________;(2)写出D的结构简式________;
(3)写出下列反应的反应类型:D
→E________,F→奥沙拉秦________;(4)从整个合成路线看,设计B
→C步骤的作用是________;(5)F的结构简式为________;
(6)有机物G(结构简式见下图)也可用于合成奥沙拉秦.它的一种同分异构体X是α-氨基酸,能与FeCl3发生显色反应,其分子中共有6种化学环境不同的H原子.X的结构简式为________
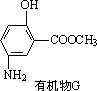
查看答案和解析>>
科目: 来源:上海市虹口区2010届高三第二次模拟考试化学试题 题型:022
2004年国家食品监督局发出公告“警惕油炸食品中的丙烯酰胺(CH2=CH-CONH2)”,丙烯酰胺对人体可造成神经毒性和遗传毒性.下图流程中的有机物K是丙烯酰胺的相邻同系物.
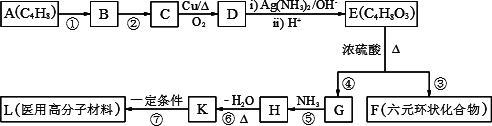
请回答下列问题:
(1)①~⑦反应中属于加成反应的有________,属于消除反应的是________.
(2)写出反应条件②________.
(3)写出结构简式B________,H________.
(4)写出下列反应的化学方程式:
C→D________ E→F________
(5)反应③除生成F、G外,还可能生成其它副产物,任写其中两种不同类别产物的结构简式________、________.
查看答案和解析>>
科目: 来源:上海市虹口区2010届高三第二次模拟考试化学试题 题型:022
| |||||||||||||||||||||||||||||||||
查看答案和解析>>
科目: 来源:山东省莘县实验高中2010届高三上学期模拟考试化学试题 题型:022
| |||||||||||||||||||||||||||||||||||||
查看答案和解析>>
科目: 来源:贵州省云峰中学2010届高三下学期3月月考化学试题 题型:022
下图涉及多种无机化工反应,其中R是一种新型无机材料,M是一种应用广泛的金属材料,F是人工合成的第一种有机物,A、C、D、M均为常见元素的单质,“↑”表示该物质常温下是气体,反应G+J→F+H2O中G与J的最佳配比为2∶1,向Y溶液中通入足量的J气体时可得到一种白色胶状沉淀,将该白色胶状沉淀滤出洗净后加热分解可以得到B.
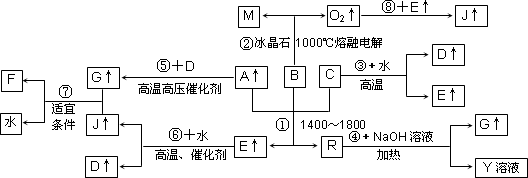
(1)试写出下列指定物质的化学式:D________,F________.
(2)反应①的化学方程式为______________.
(3)反应④的离子方程式为______________.
(4)上述反应中属于非氧化还原反应的有____________(填写相应反应的序号)
查看答案和解析>>
科目: 来源:河北省衡水中学2010届高三上学期第三次调研考试化学试题 题型:022
![]() A、D、E、X、Y五种短周期元素,它们的原子序数依次增大,A元素的原子是半径最小的原子,D元素的最高价氧化物对应的水化物与其氢化物反应生成一种盐;X与A同主族;Y元素的最外层电子数是其次外层电子数的
A、D、E、X、Y五种短周期元素,它们的原子序数依次增大,A元素的原子是半径最小的原子,D元素的最高价氧化物对应的水化物与其氢化物反应生成一种盐;X与A同主族;Y元素的最外层电子数是其次外层电子数的![]() 倍;A、D、X、Y四种元素,每一种均能与E元素形成原子个数比不相同的若干化合物.
倍;A、D、X、Y四种元素,每一种均能与E元素形成原子个数比不相同的若干化合物.
(1)画出Y元素离子的结构示意图________;
写出常温下Y的氢化物与其最高价氧化物对应水化物的浓溶液反应的化学方程式;并用单线桥表示电子转移情况________.
(2)由A、D、E、Y四种元素形成的强酸的酸式盐的名称为________,该盐的水溶液中各离子浓度有大到小的顺序为________.
(3)若1克A的单质燃烧放出的热量为M kJ,试写出表示A单质燃烧热的热化学方程式:________.
(4)科学家用D、E、X三种元素形成的化合物XDE3和X2E,在573K时反应制得了离子化合物X3DE4;经测定X3DE4中各原子的最外层电子都达到了8电子稳定结构,则DE43-的电子式为________,X3DE4与二氧化碳或水均能剧烈反应转化为常见物质,写出其中一个反应的化学方程式:________.
查看答案和解析>>
科目: 来源:河北省衡水中学2010届高三上学期第三次调研考试化学试题 题型:022
| |||||||||||||||||||||||||||||
查看答案和解析>>
科目: 来源:安徽省淮北市第一中学2010届高三上学期第三次月考化学试题 题型:022
人类在使用金属的历史进程中,经历了铜、铁、铝之后,第四种将被广泛应用的金属被科学家预测为是钛(22Ti),它被誉为“未来世纪的金属”.21世纪是钛的世纪.下面是利用钛白粉(TiO2)生产海绵钛(Ti)的一种工艺流程:
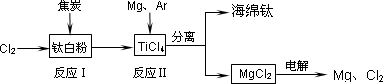
已知:Mg(s)+Cl2(g)![]() MgCl2(s) ΔH=-641 kJ·mol-1
MgCl2(s) ΔH=-641 kJ·mol-1
Cl2(g)+1/2Ti(s)![]() 1/2TiCl4(l) ΔH=-385 kJ·mol-1试回答下列问题:
1/2TiCl4(l) ΔH=-385 kJ·mol-1试回答下列问题:
(1)Ti元素的基态原子的核外电子排布式为________;
(2)钛白粉是利用TiO2+发生水解生成钛酸(H2TiO3)沉淀,再煅烧沉淀制得的.
TiO2+发生水解的离子方程式为________.
(3)反应Ⅰ在800~900℃下进行,还生成一种可燃性无色气体,该反应的化学方程式为________;反应Ⅱ的热化学方程式为________.
(4)该工艺流程中,可以循环使用的物质有________.
(5)在800℃~1 000℃时电解TiO2也可制得海绵钛,装置如下图所示.
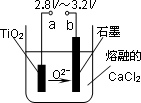
图中b是电源的________极,阴极的电极反应式为________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com