
科目: 来源:山东省汶上一中2012届高三10月月考化学试题 题型:022
已知粗铜中含有少量的锌、铁、银、金等金属和少量矿物杂质(与酸不反应).某化学兴趣小组在实验室条件下用以硫酸铜溶液为电解液,用电解的方法实现了粗铜的提纯,并对阳极泥和电解液中金属进行回收和含量测定.
步骤一:电解精制:
请回答以下问题:
电解时,粗铜应与电源的_________极相连.阴极上的电极反应式为_________.
电解过程中,硫酸铜的浓度会_________(选填:变大、不变、变小).
步骤二:电解完成后,该小组同学按以下流程对电解液进行处理:

(1)阳极泥的综合利用:
稀硝酸处理阳极泥得到硝酸银稀溶液,请你写出该步反应的离子方程式:_________.
残渣含有极少量的黄金,如何回收金,他们查阅了有关资料,了解到了一些有关金的知识,以下是他们获取的一些信息:
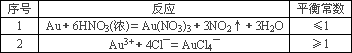
从中可知,金很难与硝酸反应,但却可溶于王水(浓硝酸与盐酸按体积比1∶3的混合物),请你简要解释金能够溶于王水的原因:_________.
(2)滤液含量的测定:
以下是该小组探究滤液的一个实验流程:
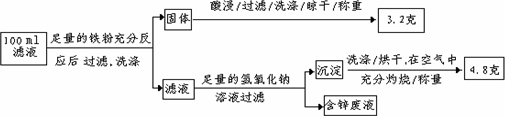
则100 mL滤液中Cu2+的浓度为_________mol·L-1,Fe2+的浓度为_________mol·L-1
查看答案和解析>>
科目: 来源:山东省汶上一中2012届高三10月月考化学试题 题型:022
下图表示各物质之间的转化关系.已知:常温下D、E、F、I、J为气体,H、I、J都为氧化物,C的焰色反应为黄色,M为红褐色固体.
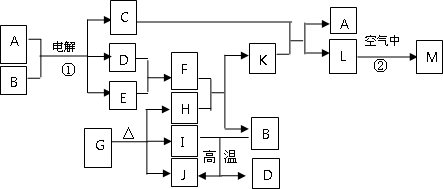
(1)写出:J的结构式_________,M的化学式_________;
(2)基于反应①原理的化学工业称为_________;写出该反应的化学方程式_________;
(3)写出K溶液和E反应的离子方程式_________;写出F溶液和H反应的离子方程式_________;
(4)已知由G分解得到的H、I、J三者的物质的量相等,则G的化学式为_________
查看答案和解析>>
科目: 来源:河南省开封高中2012届高三第一次定位测试化学试题 题型:022
有机高分子化合物甲是一种常用的光敏高分子材料,其结构简式为:
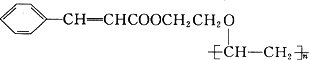
下图是合成甲的路线图,其中试剂I可由相对分子质量为26的烃与水加成制得.
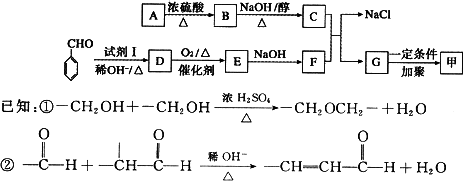
回答下列问题:
(1)试剂I的名称是________;B→C的反应类型是________;
(2)质谱图显示A的相对分子质量是80.5;A分子中氧元素的质量分数为19.88%,碳元素的质量分数为29.81%,其余为氢元素和氯元素,且A的核磁共振氢谱上有三个吸收峰,峰面积的比例为2∶2∶1,则A的结构简式为________.
(3)写出下列反应的化学方程式.
①A→B的反应________
②D→E的反应________
③C与F的反应________.
(4)E的一种同分异构体,水解产物有两种,一种能使溴水褪色,另一种在滴加饱和溴水后,有白色沉淀生成,该物质的结构简式为________.
查看答案和解析>>
科目: 来源:河南省开封高中2012届高三第一次定位测试化学试题 题型:022
(1)立方氮化硼是一种自然界不存在的人工合成超硬材料,硬度仅次于金刚石,是超硬材料领域的最重要成就之一.请回答下列问题:
在第二周期,原子的第一电离能一般随核电荷数的增大而逐渐________,比较下列原子的第一电离能:Be________B,N________O(填“>”“<”),其原因是________.
(2)下图为立方氮化硼的晶胞,则氮化硼的化学式为________,该晶体中B原子填充N原子的________空隙.若该晶胞的边长为a cm,那么该晶体的密度为________g/cm3(只要求列出算式).
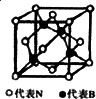
(3)立方氮化硼的晶体结构与金刚石的结构相似,但其熔点比金刚石的低,试分析其原因________.
(4)立方氮化硼由六方氮化硼在高温高压下制备,六方氮化硼又称“白玉墨”,结构和许多性质与石墨相似,六方氮化硼中N原子的杂化轨道类型为________,请在下方的方框中画出六方氮化硼的平面结构示意图(用“O”代表N原子,用“●”代表B原子,每种原子不少于7个).

查看答案和解析>>
科目: 来源:河南省开封高中2012届高三第一次定位测试化学试题 题型:022
| |||||||||||||||||||||||||||||||||||||
查看答案和解析>>
科目: 来源:河南省开封高中2012届高三第一次定位测试化学试题 题型:022
| |||||||||||||||||||||||||||
查看答案和解析>>
科目: 来源:河南省开封高中2012届高三第一次定位测试化学试题 题型:022
下图中,A、G是工业上用途很广的两种重要化工原料,B为日常生活中常见的金属,D、F、M为单质,I、L是正四面体结构的非极性分子,I是一种重要的能源,产物J是含B金属元素的胶状白色沉淀,K是由含B、D两种元素组成的化合物,N是淡黄色固体(图中部分反应物或生成物没有列出).
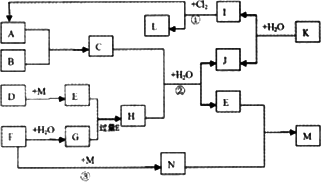
请按要求回答:
(1)元素B在元素周期表中的位置是________(填第几周期第几族).写出K的化学式________,L的电子式________.
(2)反应①进行的条件是________.
(3)反应②的离子方程式为________.
(4)反应③的化学方程式为________.
(5)写出Si与G溶液反应的离子方程式________.
查看答案和解析>>
科目: 来源:辽宁省抚顺二中2012届高三第一次月考化学试题 题型:022
[选修5:有机化学基础]
物质A在体内脱氢酶的作用下会氧化为有害物质CHB.下图是关于物质A的一种制备方法及由A引发的一系列化学反应.
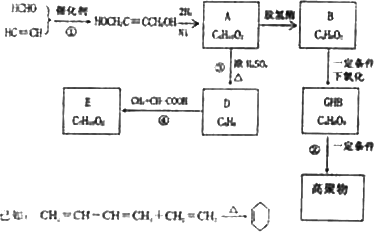
请回答下列问题:
(1)写出反应类型:反应①________,反应③________.
(2)写出化合物B中的官能团名称________.
(3)写出反应②的化学方程式________.
(4)写出反应④的化学方程式________.
(5)反应④中除生成E外,还可能存在一种副产物(含![]() 结构),它的结构简式为________.
结构),它的结构简式为________.
(6)与化合物E互为同分异构体的物质不可能为________(填写字母).
a.醇
b.醛
c.羧酸
d.酚
查看答案和解析>>
科目: 来源:辽宁省抚顺二中2012届高三第一次月考化学试题 题型:022
下图表示各物质之间的转化关系.已知:A、B、I都是XY2型化合物,且阳离子相同,A、B晶体中阴、阳离子个数比都是1∶1,但I晶体中阴、阳离子个数比是2∶1,I常用作干燥剂.
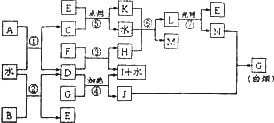
请按要求填空:
(1)I的电子式是________;
(2)反应⑥的化学方程式是________,反应③在工业上的一个重要用途是________;
(3)反应④的化学方程式是________.
(4)已知C的燃料热是1300 kJ·mol-1,表示C的燃烧热的热化学方程式是________.
(5)根据上图中物质之间的转化关系及题中所给信息判断,B的化学式是________.
查看答案和解析>>
科目: 来源:安徽省泗县双语中学2012届高三摸底考试化学试题 题型:022
研究NO2、SO2 、CO等大气污染气体的处理具有重要意义.
(1)NO2可用水吸收,相应的化学反应方程式为________.利用反应6NO2+8NH3 7N5+12H2O也可处理NO2.当转移1.2 mol电子时,消耗的NO2在标准状况下是________L.
7N5+12H2O也可处理NO2.当转移1.2 mol电子时,消耗的NO2在标准状况下是________L.
(2)已知:2SO2(g)+O2(g)![]() 2SO3(g) ΔH=-196.6 kJ·mol-1
2SO3(g) ΔH=-196.6 kJ·mol-1
2NO(g)+O2(g)![]() 2NO2(g) ΔH=-113.0 kJ·mol-1
2NO2(g) ΔH=-113.0 kJ·mol-1
则反应NO2(g)+SO2(g)![]() SO3(g)+NO(g)的ΔH=________kJ·mol-1.
SO3(g)+NO(g)的ΔH=________kJ·mol-1.
一定条件下,将NO2与SO2以体积比1∶2置于密闭容器中发生上述反应,下列能说明反应达到平衡状态的是________.
a.体系压强保持不变
b.混合气体颜色保持不变
c.SO3和NO的体积比保持不变
d.每消耗1 mol SO3的同时生成1 mol NO2
测得上述反应平衡时NO2与SO2体积比为1∶6,则平衡常数K=________.
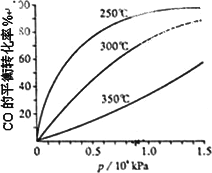
(3)CO可用于合成甲醇,反应方程式为CO(g)+2H2(g)![]() CH3OH(g).CO在不同温度下的平衡转化率与压强的关系如图所示.该反应ΔH________0(填“>”或“<”).实际生产条件控制在250℃、1.3×104 kPa左右,选择此压强的理由是________.
CH3OH(g).CO在不同温度下的平衡转化率与压强的关系如图所示.该反应ΔH________0(填“>”或“<”).实际生产条件控制在250℃、1.3×104 kPa左右,选择此压强的理由是________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com