
科目: 来源:北京市海淀区2012届高三5月查漏补缺化学试题 题型:022
图中X、Y、Z为中学化学中常见的单质,其他为化合物,它们之间存在如下转化关系(部分产物已略去).其中A俗称磁性氧化铁;E是不溶于水的酸性氧化物,能与氢氟酸反应.

(1)组成单质Y的元素在周期表中的位置是________;M中存在的化学键类型
为________;R的化学式是________.
(2)一定条件下,Z与H2反应生成ZH4,ZH4的电子式为________.
(3)已知A与1 mol Al反应转化为X时(所有物质均为固体).放出a kJ热量.写出该反应的热化学方程式:________.
(4)写出A和D的稀溶液反应生成G的离子方程式:________.
(5)向含4 mol D的稀溶液中,逐渐加入X粉末至过量.假设生成的气体只有一
种,请在坐标系中画出n(X2+)随n(X)变化的示意图,并标出n(X2+)的最大值.

查看答案和解析>>
科目: 来源:北京市海淀区2012届高三5月查漏补缺化学试题 题型:022
下图是元素周期表的一部分,A、B、C、D、E、X是周期表给出元素组成的常见单质或化合物.

Ⅰ.已知A、B、C、D、E、X存在如图所示转化关系(部分生成物和反应条件略去).
(1)若E为氧化物,则A的化学式为________,A与水反应的化学方程式________,该反应中氧化剂和还原剂的物质的量之比为________.
①当X是碱性盐溶液,C分子中有22个电子时,表示X呈碱性的离子方程式为________,用电子式表示C的形成过程:________.
②当X为金属单质时,则X与B的稀溶液反应生成C的离子反应方程式为________.
(2)若E为单质气体,D为白色沉淀,A的化学式可能是________,B含有的化学键类型为________,C与X反应的离子方程式为________.
(3)若B为单质气体,D可与水蒸气在一定条件下发生可逆反应,生成C和一种可燃性气体单质,则该可逆反应的化学方程式为________.t℃时,在密闭恒容的某容器中投入等物质的量的D和水蒸气,一段时间后达平衡,该温度下反应的平衡常数K=1,D的转化率为________.
Ⅱ.元素周期表是人们研究物质性质的重要工具
(1)列举一条能够说明⑤的非金属性强于④的事实:________,
从原子结构的角度解释⑤的非金属性强于④的原因:________.
(2)As在元素周期表中的位置:________.
(3)As的原子结构示意图为________,其氢化物的化学式为________.
(4)Y由②⑥⑦三种元素组成,它的水溶液是生活中常见的消毒剂.As可与Y的水溶液反应,生成H3AsO4,当消耗1 mol氧化剂时,电子转移了2 mol,该反应的化学方程式为________.
查看答案和解析>>
科目: 来源:江苏省梅村高级中学2012届高三1月双周练化学试题 题型:022
在一个装有可移动活塞的容器中模拟传统工业合成氨的反应:N2(g)+3H2(g)![]() 2NH3(g),反应达到平衡后,测得NH3的物质的量为a mol
2NH3(g),反应达到平衡后,测得NH3的物质的量为a mol
(1)保持容器内的温度和压强不变,向平衡体系中又通入少量的H2,再次达到平衡后,测得NH3的物质的量为b mol,则a________b(填入“>”或“<”或“=”或“无法确定”,下同).若向平衡体系中通入的是少量N2,则a________b.
煤制油是一项
新兴的、科技含量较高的煤化工技术,发展煤制油对我国而言具有重大意义.下列是煤通过间接液化技术制汽油和丙烯的主要工艺流程图.
已知甲醇制烃的反应原理为:
(2)为了提高原料利用率,上述工艺中应控制合成气中V(CO)∶V(H2)=________.
(3)由二甲醚在催化剂作用下转化为丙烯的化学方程式为:________.
(4)每生产1 t甲醇约耗煤1.5 t,每生产1 t汽油约需耗2.4 t甲醇,2015年我国煤制油将达到1000万吨,则2015年当年需消耗原煤约________万吨.
(5)采用MTG法生产的汽油中,均四甲苯(1,2,4,5-四甲基苯)质量分数约占4%~7%,均四甲苯的结构简式为:________.
(6)采用DMTO技术,若获得乙烯和丙烯及丁烯3种烃,生成丁烯的选择性(转化丁烯的甲醇的物质的量与甲醇总物质的量之比)为20%,其余生成乙烯和丙烯,设丙烯的选择性为x,今有403.2 L(标准状况)合成气,且完全转化为甲醇,甲醇转化为烯烃的总转化率亦为100%,请作出丙烯的物质的量随x变化的曲线.
查看答案和解析>>
科目: 来源:江苏省梅村高级中学2012届高三1月双周练化学试题 题型:022
草酸亚铁可用于合成锂电池的正极材料硅酸亚铁锂(Li2FeSiO4)等,其制备过程主要包括:
a.将硫酸亚铁铵[(NH4)2Fe(SO4)2·6H2O]晶体溶于适量蒸馏水,加入适量稀硫酸酸化.
b.将上述溶液煮沸,逐滴加入H2C2O4溶液,直至沉淀完全.
c.静置、倾去上层清液、过滤、洗涤、50℃以下烘干.试回答下列问题:
(1)配制(NH4)2Fe(SO4)2·6H2O溶液时,需加入少量稀硫酸,目的是________.
(2)将制得的产品(FeC2O4·2H2O)在氩气气氛中进行热重分析,结果如图(TG%表示残留固体质量占原样品总质量的百分数).
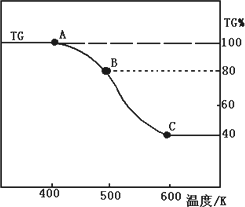
①则A-B发生反应的化学方程式为:________.
②精确研究表明,B-C实际是分两步进行的,每步释放一种气体,其中第一步释放的气体相对分子质量较第二步的小,试写出B-C两步反应的方程式:________、________;
(3)Li2CO3、FeC2O4·2H2O和SiO2粉末均匀混合,在800℃.
的氩气中烧结6小时,即可制成硅酸亚铁锂.①合成硅酸亚铁锂的化学方程式为:________.
②该锂电池放电时的总反应式为LiFeSiO4+Li=Li2FeSiO4,写出相应的电极反应式:正极________、负极________.
查看答案和解析>>
科目: 来源:江苏省梅村高级中学2012届高三1月双周练化学试题 题型:022
MnSO4·H2O在工业、农业等方面有广泛的应用.
(一)制备:工业上用化工厂尾气中低浓度SO2还原MnO2矿制备MnSO4·H2O过程如下:
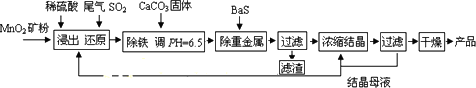
已知:常温时部分硫化物难溶盐的Ksp:CuS-6.3×10-36、PbS-1.0×10-28、NiS-2.0×10-26、MnS-2.5×10-10,请回答下列问题:
(1)生产中MnO2矿粉碎的目的是________.
(2)除铁发生的离子反应方程式为________.
(3)除重金属离子后,若混合溶液中Cu2+、Pb2+、Ni2+的浓度均为1.0×10-5 mol/L,则c(S2-)最大=________mol/L.
(二):性质-热稳定性:MnSO4·H2O在1150℃高温下分解的产物是Mn3O4、含硫化合物、水,在该条件下硫酸锰晶体分解反应的化学方程式是________
(三)废水处理:工厂废水中主要污染为Mn2+和Cr6+,现研究铁屑用量和pH值对废水中铬、锰去除率的影响,(1)取100 mL废水于250 mL三角瓶中,调节pH值到规定值,分别加入不同量的废铁屑.得到铁屑用量对铬和锰去除率的影响如下图1所示.则在pH一定时,废水中铁屑用量为________时锰、铬去除率最好

(2)取100 mL废水于250 mL三角瓶中,加入规定量的铁粉,调成不同的pH值.得到pH值对铬和锰去除率的影响如下图2所示.则在铁屑用量一定时,废水pH=________时锰、铬去除率最好
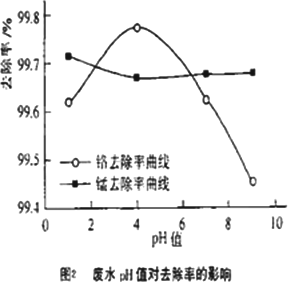
查看答案和解析>>
科目: 来源:江苏省梅村高级中学2012届高三1月双周练化学试题 题型:022
炔抑制剂的合成路线如下:
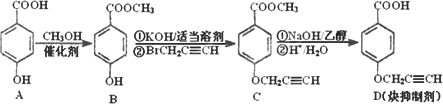
(1)化合物A核磁共振氢谱有________种峰.
(2)化合物C中含氧官能团有________、________(填名称).
(3)鉴别化合物B和C最适宜的试剂是________.
(4)写出A-B的化学方程式________.
(5)B的同分异构体很多,符合下列条件的异构体有________种.
①苯的衍生物
②含有羧基和羟基
③分子中无甲基
(6)试以苯酚、氯乙酸钠(ClCH2COONa)、正丁醇为原料(无机试剂任用),结合题中有关信息,请补充完整的合成路线流程图.
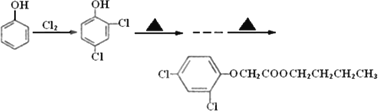
查看答案和解析>>
科目: 来源:2013年普通高等学校招生全国统一考试广东卷理综化学 题型:022
大气中的部分碘源于O3对海水中I-的氧化.将O3持续通入NaI溶液中进行模拟研究.
(1)O3将I-氧化成I2的过程由3步反应组成:
①I-(aq)+O3(g)=IO-(aq)+O2(g) ΔH1
②IO-(aq)+H+(aq)![]() HOI(aq) ΔH2
HOI(aq) ΔH2
③HOI(aq)+I-(aq)+H+(aq)![]() I2(aq)+H2O(l) ΔH3
I2(aq)+H2O(l) ΔH3
总反应的化学方程式为________,其反应ΔH=________.
(2)在溶液中存在化学平衡:I2(aq)+I-(aq)![]() I3-(aq),其平衡常数表达式为________.
I3-(aq),其平衡常数表达式为________.
(3)为探究Fe2+对O3氧化I-反应的影响(反应体图1),某研究小组测定两组实验中I3-浓度和体系pH,结果见图2和下表.
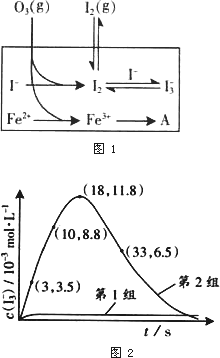
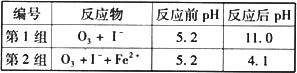
①第1组实验中,导致反应后pH升高的原因是________.
②图1中的A为________,由Fe3+生成A的过程能显著提高Ⅰ-的转化率,原因是________.
③第2组实验进行18 s后,I3-浓度下降.导致下降的直接原因有(双选)________.
A.c(H+)减小
B.c(I-)减小
C.I2(g)不断生成
D.c(Fe3+)增加
(4)据图2,计算3~18 s内第2组实验中生成I3-的平均反应速率(写出计算过程,结果保留两位有效数字).
查看答案和解析>>
科目: 来源:2013年普通高等学校招生全国统一考试广东卷理综化学 题型:022
脱水偶联反应是一种新型的直接烷基化反应,例如:
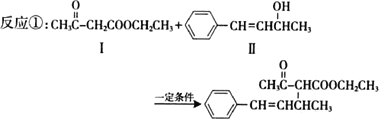
(1)化合物Ⅰ的分子式为________,1 mol该物质完全燃烧最少需要消耗________mol O2.
(2)化合物Ⅱ可使________溶液(限写一种)褪色;化合物Ⅲ(分子式为C10H11Cl)可与NaOH水溶液共热生成化合物Ⅱ,相应的化学方程式为________.
(3)化合物Ⅲ与NaOH乙醇溶液共热生成化合物Ⅳ,Ⅳ的核磁共振氢谱除苯环峰外还有四组峰,峰面积之比为为1∶1∶1∶2,Ⅳ的结构简式为________.
(4)由CH3COOCH2CH3可合成化合物Ⅰ.化合物Ⅴ是CH3COOCH2CH3的一种无支链同分异构体,碳链两端呈对称结构,且在Cu催化下与过量O2反应生成能发生银镜反应的化合物Ⅵ.Ⅴ的结构简式为________,Ⅵ的结构简式为________.
(5)一定条件下,![]() 也可以发生类似反应①的反应,有机产物的结构简式为________.
也可以发生类似反应①的反应,有机产物的结构简式为________.
查看答案和解析>>
科目: 来源:2013年普通高等学校招生全国统一考试天津卷理综化学 题型:022
某市对大气进行监测,发现该市首要污染物为可吸入颗粒物PM2.5(直径小于等于2.5um的悬浮颗粒物)其主要来源为燃煤、机动车尾气等.因此,对PM2.5、SO2、NOx等进行研究具有重要意义.请回答下列问题:
(1)对PM2.5样本用蒸馏水处理制成待测试样.若测得该试样所含水溶性无机离子的化学组分及其平均浓度如下表:
根据表中数据判断PM2.5的酸碱性为________,试样的PH值________
(2)为减少SO2的排放,常采取的措施有:
①将煤转化为清洁气体燃料.已知:
H2(g)+1/2O2(g)=H2O(g) ΔH=-241.8 KJ/molC(s)+1/2O2(g)=CO(g) ΔH=-110.5 KJ/mol
写出焦炭与水蒸气反应的热化学方程式________;
②洗涤含SO2的烟气,以下物质可作洗涤剂的是________.
a.Ca(OH)2
b.Na2CO3
c.CaCl2
d.NaHSO3
(3)汽车尾气中NOx和CO的生成及转化为:
①已知气缸中生成NO的反应为:
N2(g)+O2(g)![]() 2NO(g) ΔH>0
2NO(g) ΔH>0
若1 mol空气含有0.8 mol N2和0.2 mol O2,1300℃时在密闭容器内反应达到平衡.测得NO为8×10-4 mol.计算该温度下的平衡常数K=________.
汽车启动后,气缸温度越高,单位时间内NO排放量越大,原因是________.
②汽车燃油不完全燃烧时产生CO,有人设想按下列反应除去CO:2CO(g)=2C(s)+O2(g)已知该反应的ΔH>0,简述该设想能否实现的依据________.
③目前,在汽车尾气系统中装置催化转化器可减少CO和NO的污染,其化学反应方程式为________.
查看答案和解析>>
科目: 来源:2013年普通高等学校招生全国统一考试天津卷理综化学 题型:022
已知![]() 水杨酸酯E为紫外吸收剂,可用于配制防晒霜.E的一种合成路线如下:
水杨酸酯E为紫外吸收剂,可用于配制防晒霜.E的一种合成路线如下:
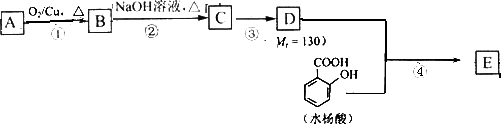
请回答下列问题:
(1)一元醇A中氧的质量分数约为21.6%.则A的分子式为________结构分析显示A只有一个甲基,A的名称为________.
(2)B能与新制的Cu(OH)2发生反应,该反应的化学方程式为________.
(3)C有——种结构;若一次取样,检验C中所含官能团,按使用的先后顺序写出所用试剂________.
(4)第③的反应类型为________;D所含官能团的名称为________.
(5)写出同时符合下列条件的水杨酸所有同分异构体的结构简式:________.
a分子中含有6个碳原子在一条线上;
b分子中所含官能团包括水杨酸具有的官能团
(6)第④步的反应条件为________;写出E的结构简式.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com