相关习题
0 95652 95660 95666 95670 95676 95678 95682 95688 95690 95696 95702 95706 95708 95712 95718 95720 95726 95730 95732 95736 95738 95742 95744 95746 95747 95748 95750 95751 95752 95754 95756 95760 95762 95766 95768 95772 95778 95780 95786 95790 95792 95796 95802 95808 95810 95816 95820 95822 95828 95832 95838 95846 203614
科目:
来源:黄冈重点作业 高三化学(下)
题型:038
某二价金属元素的同位素的碳酸盐(MCO3)粉末4 g,放到50 ml 1 mol·L-1稀硫酸中,有无色无味的气体缓慢生成,同时生成新的不溶物,经过滤、洗涤、干燥后,称得新的不溶物4.72 g;向滤液中加入60 ml 1 mol·L-1的氢氧化钠溶液后,溶液的pH=7,求这种同位素的质量数,若其原子中的中子数为质子数的1.5倍,求该原子中的质子数、中子数和电子数,并写出有关反应的离子方程式.
查看答案和解析>>
科目:
来源:黄冈重点作业 高三化学(下)
题型:038
|
|
不同的卤素原子之间可形成一系列化合物椔彼鼗セ?铮?—4.66 g BrClx溶于水后通入足量SO2与其反应生成氢溴酸、盐酸和硫酸.再用碱将溶液pH调节至中性后,加入过量Ba(NO3)2溶液充分反应后滤去沉淀,再向滤液中加入过量AgNO3溶液,最后得卤化银15.46 g.试求:
| (1) |
|
(2) |
|
|
查看答案和解析>>
科目:
来源:黄冈重点作业 高三化学(下)
题型:038
|
|
已知:标准状况下,1体积水能溶解2.3体积氯气,其中约有 的氯气和水发生反应.20℃时,氯化钠的溶解度为36 g,饱和溶液的密度为1.18 g·cm-3;20℃时,饱和盐酸溶液的质量分数约为37%,溶液密度为1.19 g·cm-3 的氯气和水发生反应.20℃时,氯化钠的溶解度为36 g,饱和溶液的密度为1.18 g·cm-3;20℃时,饱和盐酸溶液的质量分数约为37%,溶液密度为1.19 g·cm-3
| (1) |
|
计算20℃时饱和氯化钠溶液和盐酸溶液的物质的量浓度.
|
|
(2) |
|
通过计算说明20℃时,当氯气中混有少量氯化氢气体时,可以用饱和食盐水除去.
|
|
|
查看答案和解析>>
科目:
来源:黄冈重点作业 高三化学(下)
题型:038
|
|
实验室常用澄清石灰水检验CO2,在20℃时,每100 g水溶解Ca (OH)20.165 g即达饱和.
| (1) |
|
在20℃时500 g水中加入37.0 g Ca(OH)2粉末,经充分搅拌,若液体体积仍为500 ml,求OH-离子的物质的量浓度.
|
|
(2) |
|
若使原500 ml溶液中的c(Ca2+)降低至0.0100 mol·L-1,求需要通入标准状况下二氧化碳气体多少升.
|
|
|
查看答案和解析>>
科目:
来源:黄冈重点作业 高三化学(下)
题型:038
|
|
使一定量的磷化氢和氢气的混合气体,依次通过两支加热的硬质玻璃管,第一支玻璃管中装有铜屑,第二支玻璃管中装有氧化铜,第一支玻璃管中由于发生如下反应:
2PH3+3Cu Cu3P2 (s)+3H2 Cu3P2 (s)+3H2
玻璃管质量增加4.96 g,第二支玻璃管质量在发生反应后减少5.76 g.
| (1) |
|
(2) |
|
|
查看答案和解析>>
科目:
来源:黄冈重点作业 高三化学(下)
题型:038
|
|
有Na2O2与NaHCO3的混合物粉末,将其分为两等份.其中一份加入100 ml盐酸,使其充分反应后的溶液为中性,此时放出的气体(已干燥)2.24 L(标准状况)全部通入另一份混合粉末,充分反应后气体的体积变为2.016 L(标准状况).求:
| (1) |
|
原混合物粉末中Na2O2与NaHCO3各自的物质的量
|
|
(2) |
|
|
查看答案和解析>>
科目:
来源:黄冈重点作业 高三化学(下)
题型:038
有NaOH和NaHCO3固体混合物20.8 g,在密闭容器中加热到250℃,经充分反应后排出气体、冷却,称得剩余固体质量为15.9 g,求原混合物中NaOH的质量分数.
查看答案和解析>>
科目:
来源:黄冈重点作业 高三化学(下)
题型:038
已知热化学方程式:
C (s)+O2 (g)=CO2 (g);ΔH=-393.3 kJ/mol
CaCO3 (s)=CaO (s)+CO2 (g);ΔH=178.2 kJ/mol
若要将1t碳酸钙煅烧成生石灰,理论上需要用不含杂质的焦炭多少千克?
查看答案和解析>>
科目:
来源:黄冈重点作业 高三化学(下)
题型:038
|
|
为了测定某铜银合金的成分,将30.0 g合金溶于80.0 ml 13.5 mol·L-1的浓硝酸中,将合金完全溶解后,收集到气体6.72 L(标准状况),并测得溶液pH=0,假设反应后溶液体积仍为80.0 ml.试计算:
| (1) |
|
(2) |
|
|
查看答案和解析>>
科目:
来源:福建省惠南中学2007届高三第一学期期中考试 化学试卷
题型:038
|
|
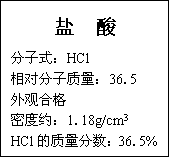
如下图为某市售盐酸试剂瓶标签上的部分数据.问:
| (1) |
|
(2) |
|
取该盐酸25.42 mL与2.00 mol/L的氢氧化钠溶液100 mL混合,再将混合后溶液稀释至1.00 L,此时溶液的pH约为多少?
|
|
|
查看答案和解析>>
