相关习题
0 95658 95666 95672 95676 95682 95684 95688 95694 95696 95702 95708 95712 95714 95718 95724 95726 95732 95736 95738 95742 95744 95748 95750 95752 95753 95754 95756 95757 95758 95760 95762 95766 95768 95772 95774 95778 95784 95786 95792 95796 95798 95802 95808 95814 95816 95822 95826 95828 95834 95838 95844 95852 203614
科目:
来源:2006年普通高等学校招生全国统一考试(江苏省)、化学
题型:038
|
|
下图是部分短周期元素的单质及其化合物的转化关系图(有关反应的条件及生成的H2O已略去),已知:(a)A、B、C、D是非金属单质,其中B、C、D在常温常压下是气体.(b)反应①②是化工生产中的重要反应.(c)化合物E是形成酸雨的污染物之一,化合物K是常用的氮肥.(d)化合物L具有漂白性,可由Cl2与NaOH溶液反应而制得.(e)化合物J由两种元素组成,其相对分子质量为32.
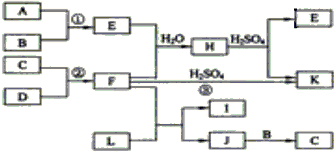
请按要求填空:
| (1) |
|
(2) |
|
C的结构式________;H的化学式________.
|
|
(3) |
|
L的溶液与化合物E反应的离子方程式________.
|
|
(4) |
|
|
查看答案和解析>>
科目:
来源:湖北省黄冈中学、襄樊五中2007届高三年级11月联考、化学试题
题型:038
|
|
将一定量的过氧化钠固体投到一定量的稀硫酸中,待完全反应后,在标准状况下共收集到3.36L的气体,然后将所得溶液蒸干得到不含结晶水的固体36.4g.通过计算回答下列问题 | (1) |
|
(2) |
|
(3) |
|
若加入过氧化钠固体的质量为mg,最后得到固体产物的质量为ng,则n的最大值为________(用含m的表达式表示),此时固体的成份是________.
|
|
|
查看答案和解析>>
科目:
来源:湖北省黄冈中学、襄樊五中2007届高三年级11月联考、化学试题
题型:038
|
|
进行下列实验:将过量Mg粉溶于100mL1.5mol/L.稀H2SO4中,反应结束后,滤去多余Mg粉,滤液在t℃下蒸发,当滤液质量为720g时开始析出MgsO4×H2O晶体,当析出晶体12.3g时,剩下滤液48.0g.通过计算请回答下列问题(请写出计算过程).
| (1) |
|
(2) |
|
开始析出MgSO4·xH2O晶体时溶液的质量分数;
|
|
(3) |
|
(4) |
|
|
查看答案和解析>>
科目:
来源:湖北省黄冈中学、黄石二中2007届高三联考化学试卷
题型:038
查看答案和解析>>
科目:
来源:湖北省华中师大一附中2006-2007学年度第一学期期中检测、高三年级化学试题
题型:038
|
|
硫铁矿又称黄铁矿,是生产硫酸的原料,其主要成分为FeS2.850℃~950℃时,硫铁矿在空气中煅烧,可能发生下列反应(设空气中N2与O2体积比为4∶1):
3FeS2+8O2→Fe3O4+6SO2①
4FeS2+11O2→2Fe2O3+8SO2②
| (1) |
|
含硫35%的硫铁矿样品(杂质不含硫),其FeS2的含量为多少?以此种黄铁矿为原料制取硫酸,再用硫酸制取硫酸铵.燃烧75t黄铁矿生产出79.2t硫酸铵.若在制取硫酸铵时硫酸的利用率为90%,则用黄铁矿制取硫酸时的损失率为多少?
|
|
(2) |
|
把1.00g含脉石(SiO2)的黄铁矿试样在氧气中灼烧后,得到0.78g残渣,则黄铁矿的纯度为多少?
|
|
(3) |
|
为使FeS2煅烧完全生成Fe2O3,工业上使用过量空气,当空气过量20%时,所得炉气中SO2的体积分数为多少?
|
|
(4) |
|
480g纯净的FeS2在空气中完全反应,若所得固体中,Fe和O的物质的量之比n(Fe)∶n(O)=4∶a,此时消耗空气为bmol.试写出b与a的关系式:________.
|
|
|
查看答案和解析>>
科目:
来源:河南省西华一高2006-2007学年高三年级化学第一次月考
题型:038
|
|
化合物KxFe(C2O4)y·zH2O是一种重要的光化学试剂,其中铁为+3价.分别称取该样品0.49lg两份,其中一份在110℃干燥脱水,至质量恒定为0.437g.另一份置于锥形瓶中,加入足量的3mol·L-1H2SO4和适量的蒸馏水,加热至75℃,趁热加入0.0500mol·L-1KMnO4溶液24.0mL,恰好完全反应;再向溶液中加入适量的某种还原剂,将Fe3+完全转化为Fe2+,该溶液中Fe2+刚好与4.0mL0.0500mol·L-1KMnO4溶液完全反应.通过计算,分别求:
| (1) |
|
(2) |
|
(3) |
|
化合物的化学式.
己知:2KMnO4+5H2C2O4+3H2SO4=2MnSO4+K2SO4+10CO2↑+8H2O
MnO4—+5Fe2++8H+=Mn2++5Fe3++4H2O
|
|
|
查看答案和解析>>
科目:
来源:河南省实验中学2006-2007学年度上学期高三年级期中考试、化学试题
题型:038
把两块质量相同的铜片作电极平行插入CuSO4溶液中,电解一段时间后,取出电极洗净、烘干、称量,质量差为2.56g,在通电过程中,电路中通过的电子为多少mol?
查看答案和解析>>
科目:
来源:河南省实验中学2006-2007学年度上学期高三年级期中考试、化学试题
题型:038
右图为10mL一定物质的量的盐酸用一定浓度的NaOH溶液中和的图示,依据图示推算出HCl和NaOH的物质的量浓度各是多少?(注:溶液混合时造成的体积缩小忽略不计)

查看答案和解析>>
科目:
来源:和风中学2007届高三月考化学试卷
题型:038
|
|
某有机化合物A含碳77.8%,氢为7.40%,其余为氧,A的相对分子质量为甲
烷的6.75倍.
| (1) |
|
(2) |
|
|
查看答案和解析>>
科目:
来源:海门市2007学年第一学期高三第一次诊断考试、化学试卷
题型:038
|
|
在t℃时,向盛有500g水的烧杯中加入3.7gCa(OH)2粉末,充分搅拌.已知t℃时,Ca(OH)2的溶解度是0.185g.并假设在溶解和反应过程中溶液的体积温度基本保持不变,所得溶液的密度约为1.00g/cm3.试计算下列问题(计算结果保留2位小数).
| (1) |
|
求烧杯中所得的石灰水中OH?/SUP>离子的物质的量浓度.
|
|
(2) |
|
若采用向上述烧杯中通入CO2气体的方法,使溶液中的Ca2+离子浓度等于0.01mol·L—1,则需要向烧杯中通入标准状况下CO2的体积是多少?
|
|
|
查看答案和解析>>

![]()
![]() 和
和![]() 的混合粉末加入足量1
的混合粉末加入足量1![]() 的
的![]() 溶液中,反应后溶液的体积为1
溶液中,反应后溶液的体积为1![]() ,测得溶液中
,测得溶液中![]() 浓度为0.1
浓度为0.1![]() ,求混合物中
,求混合物中![]() 的质量.
的质量.