相关习题
0 95661 95669 95675 95679 95685 95687 95691 95697 95699 95705 95711 95715 95717 95721 95727 95729 95735 95739 95741 95745 95747 95751 95753 95755 95756 95757 95759 95760 95761 95763 95765 95769 95771 95775 95777 95781 95787 95789 95795 95799 95801 95805 95811 95817 95819 95825 95829 95831 95837 95841 95847 95855 203614
科目:
来源:辽宁省师大附中2006-2007学年度上学期高三年级期中考试、化学试题
题型:038
|
|
将铁粉与氧化铁的混合物19.2g,加入200mL稀H2SO4,放出3360mL氢体(标况),反应后溶液中无固体剩余.向反应后的溶液里加入KSCN溶液,不呈血红色.中和过剩的酸,并将全部Fe2+沉淀为Fe(OH)2,共用去4mol/LNaOH溶液200mL.
求:
| (1) |
|
(2) |
|
|
查看答案和解析>>
科目:
来源:辽宁省鞍山13中学2007届高三化学第二次模拟考试卷、新课标人教版 人教版新课标
题型:038
在10mL硫酸和硫酸钾的混合溶液中,硫酸的物质的量浓度为1.6mol/L,硫酸钾的物质的量浓度为3.0mol/L.欲使硫酸的浓度变为2.0mol/L,硫酸钾的浓度变为0.30mol/L,现用98%的浓硫酸(ρ=1.84g·cm—3)和蒸馏水进行配制.试求需要取用浓硫酸的体积.
查看答案和解析>>
科目:
来源:辽宁省2007年上学期高三年级期中联合考试、化学试题
题型:038
|
|
将一定量C12通入250mLKBr溶液中,反应后将溶液蒸干,测知所得固体中含溴元素10g,且K+和C1-的物质的量之比为2:1,求:
| (1) |
|
标准状况下通入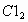 的体积. 的体积.
|
|
(2) |
|
|
查看答案和解析>>
科目:
来源:连州中学2007届高三第二次月考、化学试卷
题型:038
环保检测部门测定某气体样品中含一氧化碳的含量,其方法和实验步骤如下:
①将2.000L的气体样品通过盛有I2O5固体的加热管,发生的反应为:
5CO+I2O5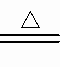 5CO2+I2.
5CO2+I2.
②将所产生的碘升华,并加入30.00mL0.0050mol·L-1的硫代硫酸钠溶液,发生的反应为:I2+2S2O32-=2I-+S4O62-
③将②中溶液取出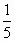 ,加入1.000mL0.0100mol·L-1的碘水,正好将所取溶液中过量的Na2S2O3全部氧化.
,加入1.000mL0.0100mol·L-1的碘水,正好将所取溶液中过量的Na2S2O3全部氧化.
试计算1L该气体样品中有多少毫克(mg)的CO?
查看答案和解析>>
科目:
来源:旧版邵东一中2007届高三第五次月考化学试题
题型:038
|
|
计算题:合成氨工业生产中所用的α-Fe催化剂的主要成分是FeO、Fe2O3
| (1) |
|
某FeO、Fe2O3混合物中,铁、氧的物质的量之比为4︰5,其中Fe2+与Fe3+物质的量之比为________.
|
|
(2) |
|
当催化剂中Fe2+与Fe3+的物质的量之比为1︰2时,其催化活性最高,此时铁的氧化物混合物中铁的质量分数为________(用小数表示,保留2位小数).
|
|
(3) |
|
以Fe2O3为原料制备上述催化剂,可向其中加入适量炭粉,发生如下反应:
2Fe2O3+C 4FeO+CO2↑.为制得这种活性最高的催化剂,应向480gFe2O3粉末中加入炭粉的质量为________g. 4FeO+CO2↑.为制得这种活性最高的催化剂,应向480gFe2O3粉末中加入炭粉的质量为________g.
|
|
|
查看答案和解析>>
科目:
来源:揭东一中2007届高三级第一次月考化学试题
题型:038
|
|
在密闭容器中,通入AmolN2和BmolH2,在一定条件下达到平衡,容器中还剩余CmolN2,
| (1) |
|
(2) |
|
(3) |
|
若把容器体积减小一半,则正反应速率________,逆反应速率________,N2转化率________.(填“变大”、“变小”、“不变”)
|
|
|
查看答案和解析>>
科目:
来源:江苏省张家港高级中学2007届高三化学综合练习
题型:038
|
|
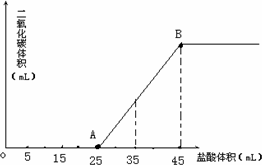
将2.5g碳酸钠、碳酸氢钠和氢氧化钠固体混合物完全溶解于水,制成稀溶液,然后向该溶液中逐滴加入1mol/L的盐酸,所加入盐酸的体积与产生CO2的体积(标准状况)关系如图所示:
| (1) |
|
写出OA段所发生反应的离子方程式.________
|
|
(2) |
|
当加入35mL盐酸时,产生二氧化碳的体积为________mL(标准状况).
|
|
(3) |
|
|
查看答案和解析>>
科目:
来源:江苏省张家港高级中学2007届高三化学综合练习
题型:038
|
|
将5.500g铁铝混合物粉末加入900.00mL1.00mol/LHNO3溶液中,充分反应后,得aL(标准状况)NO气体.
| (1) |
|
HNO3是否过量________,判断的理由是________.
|
|
(2) |
|
若a=3360mL(标准状况),则混合物中铝的质量分数为________%.
|
|
(3) |
|
若a=3360mL(标准状况),往反应后的溶液中加入________mL1.000mol/LNaOH溶液时生成的沉淀量最大,还要加________mL1.000mol/LNaOH溶液才能使沉淀的量保持不变.
|
|
|
查看答案和解析>>
科目:
来源:江苏省盐城上冈高级中学2007高三第二次阶段考试、化学试题
题型:038
|
|
向Cu与CuO的混合物中加入混酸(硝酸和硫酸)后加热,使之恰好完全反应,反应中不产生SO2和Cu(NO3)2,硝酸的还原产物只有NO,且得到NO8.96L(标准状况).将溶液冷却后刚好全部结晶(无其它任何残留物),得到CuSO4·5H2O250g.
求:
| (1) |
|
(2) |
|
(3) |
|
|
查看答案和解析>>
科目:
来源:江苏省盐城上冈高级中学2007高三第二次阶段考试、化学试题
题型:038
|
|
目前工业上主要采用离子交换膜法电解饱和食盐水,制得Cl2和H2,并将电解后所得的Cl2和H2按一定体积比,按图示流程合成质量分数为36.5%的浓盐酸.
H2和Cl2→合成炉→石墨冷凝器→一级干燥塔→二级干燥塔→吸收塔
| (1) |
|
已知在该生产条件下食盐的溶解度为36.5g,则此时饱和食盐水溶质的质量分数为________.
|
|
(2) |
|
若每台电解槽平均每天消耗2.2×104mol食盐,电解生成的Cl2与H2按体积比1∶1.1通入合成塔,不考虑各阶段的物料损耗,尾气不再用于合成盐酸.则理论上每天每台电解槽可生产36.5%的盐酸________t.
|
|
(3) |
|
某厂现有相同的电解槽n台,每台每天消耗食盐at,氯气与氢气以1∶b(b>1)的体积比通入合成塔,同样不考虑各阶段的物料损耗,则该厂每天可生产36.5%的盐酸________t.
|
|
|
查看答案和解析>>

![]() 5CO2+I2.
5CO2+I2.![]() ,加入1.000mL0.0100mol·L-1的碘水,正好将所取溶液中过量的Na2S2O3全部氧化.
,加入1.000mL0.0100mol·L-1的碘水,正好将所取溶液中过量的Na2S2O3全部氧化.