相关习题
0 95662 95670 95676 95680 95686 95688 95692 95698 95700 95706 95712 95716 95718 95722 95728 95730 95736 95740 95742 95746 95748 95752 95754 95756 95757 95758 95760 95761 95762 95764 95766 95770 95772 95776 95778 95782 95788 95790 95796 95800 95802 95806 95812 95818 95820 95826 95830 95832 95838 95842 95848 95856 203614
科目:
来源:山东省潍坊市2006-2007学年度第一学期高三年级教学质量检测、化学试题
题型:038
|
|
在一定温度下,发生如下反应:N2+3H2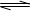 2NH3起始时充入的N2和H2的物质的量分别是3.0mol和6.0mol,平衡时,生成NH3的物质的量是2.4mol.已知容器的容积为5.0L,试求: 2NH3起始时充入的N2和H2的物质的量分别是3.0mol和6.0mol,平衡时,生成NH3的物质的量是2.4mol.已知容器的容积为5.0L,试求:
| (1) |
|
(2) |
|
|
查看答案和解析>>
科目:
来源:山东省聊城市2006-2007学年度第一学期高三年级期中考试、化学试题
题型:038
金属锡(Sn)的纯度可以通过下述方法分析:将试样溶于盐酸,反应的化学方程式为:Sn+2HC1=SnC12+H2↑,再加入过量FeC13溶液,发生如下反应:SnC12+2FeC13=SnC14+2FeC12最后用已知浓度K2Cr2O7cy溶液滴定生成的Fe2+离子,反应的化学方程式为:6FeC12+K2Cr2O7+14HC1=6FeC1+2CrCl32KC13+7H2O
现有金属锡试样0.613克,经上述各步反应后,共用去0.100mol/LK2Cr2O7溶液16.0毫升,求试样中锡的百分含量(假定杂质不参加反应).
查看答案和解析>>
科目:
来源:普宁一中2007年高三级第三次阶段考、化学科试题卷
题型:038
|
|
现在由等物质的量的NaHCO3和KHCO3组成的混合物a g,与100mL盐酸反应。
(题中涉及的气体体积均以标准状况计,填空时可以用带字母的式子表示。)
| (1) |
|
该混合物中NaHCO3与KHCO3的质量之比为________。
|
|
(2) |
|
如碳酸氢盐与盐酸恰好完全反应,则盐酸的物质的量浓度为________mol·L—1。
|
|
(3) |
|
如果盐酸过量,生成CO2的体积为________L。
|
|
(4) |
|
如果反应后碳酸氢盐有剩余,盐酸不足量,要计算生成CO2的体积,还需要知道________。
|
|
(5) |
|
若NaHCO3和KHCO3不是以等物质的量混合,则a g固体混合物与足量的盐酸完全反应时生成CO2的体积[V(CO2)]范围是________。(不要求写计算过程)
|
|
|
查看答案和解析>>
科目:
来源:平阳中学2006-2007学年度第一学期高三年级期中考试、化学试题
题型:038
|
|
等物质的量的NaHCO3和KHCO3的混合物9.20g与100mL盐酸反应.
| (1) |
|
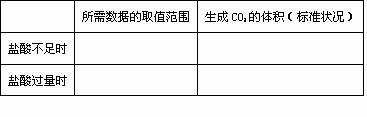
试分析,欲求标准状况下生成的CO2的体积时,还需什么数据________(用a、b等表示,要注明单位).
|
|
(2) |
|
利用所确定的数据,求标准状况下生成的CO2的体积:
|
|
(3) |
|
若NaHCO3和KHCO3不是等物质的量混合,则9.2g固体与盐酸完全反应时,在标准状况下生成CO2气体的体积大于________L,小于________L(小数点后保留2位数).
|
|
|
查看答案和解析>>
科目:
来源:南通中学2007届高三期中考试化学试卷
题型:038
|
|
硝酸工业生产中的尾气可用纯碱溶液吸收,有关的化学反应为:
2NO2+Na2CO3→NaNO2+NaNO3+CO2↑①
NO+NO2+Na2CO3→2NaNO2+CO2↑②
| (1) |
|
根据反应①,每产生22.4L(标准状况下)CO2,吸收液质量将增加________g.
|
|
(2) |
|
配制1000g质量分数为21.2%的纯碱吸收液,需Na2CO3·10H2O________g.
|
|
(3) |
|
现有1000g质量分数为21.2%的纯碱吸收液,吸收硝酸工业尾气,每产生22.4L(标准状况下)CO2时,吸收液质量就增加44g.
①计算吸收液中NaNO2和NaNO3的物质的量之比
②1000g质量分数为21.2%的纯碱在20℃经充分吸收硝酸工业尾气后,蒸发掉688g水,冷却到0℃,最多可析出NaNO2多少克?(0℃时,NaNO2的溶解度为71.2g/100g水)
|
|
|
查看答案和解析>>
科目:
来源:南通中学2007届高三期中考试化学试卷
题型:038
|
|
能源是人类社会发展进步的物质基础.在当代,能源同信息、材料一起构成了现代文明的三大支柱.
| (1) |
|
为了降低汽车尾气对大气的污染,江苏有关部门拟用甲醇替代液化石油气作为公交车的燃料.已知在:25℃、101kPa下,1g甲醇燃烧生成CO2和液态水时放热22.68kJ.则甲醇的燃烧热为________
|
|
(2) |
|
测定工业甲醇中CH3OH的质量分数可用下法:取0.1000g工业甲醇样品,以适量H2SO4酸化后,加入20.00mL0.2000mol/L的K2Cr2O7溶液,再用0.3000mol/L(NH4)2Fe(SO4)2标准溶液滴定,耗去此标准液20.00mL时,刚好到达滴定终点.
已知CH3OH+Cr2O72-+8H+=CO2↑+2Cr3++6H2O
①写出H2SO4酸化的K2Cr2O7溶液与(NH4)2Fe(SO4)2溶液反应的离子方程式.
②求此工业甲醇中CH3OH的质量分数.
|
|
|
查看答案和解析>>
科目:
来源:南通市2007届高三基础调研测试、化学
题型:038
|
|
铜是重要的工业原材料,现有Cu、Cu2O和CuO组成的混合物,某研究性学习小组为了探究其组成情况,向混合物中加入100mL0.6mol/LHNO3溶液刚好使其溶解,同时收集到224mLNO气体(标准状况).请回答下列问题:
| (1) |
|
写出Cu2O跟稀硝酸反应的化学反应方程式________;
|
|
(2) |
|
(3) |
|
如混合物中含0.01molCu,则其中Cu2O、CuO的物质的量分别是________mol、________mol;
|
|
(4) |
|
如混合物中Cu的物质的量为X,求X的取值范围________.
|
|
|
查看答案和解析>>
科目:
来源:南京市2007届高三质量检测、化学
题型:038
|
|
碳酸氢铵和熟石灰共热时可能发生如下反应:
NH4HCO3+Ca(OH)2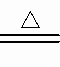 CaCO3+NH3↑+2H2O CaCO3+NH3↑+2H2O
NH4HCO3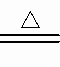 NH3↑+CO2↑+H2O NH3↑+CO2↑+H2O
取碳酸氢铵和熟石灰的混合物共0.1mol,在密闭容器中加热至200℃(200℃时CaCO3、Ca(OH)2不分解),充分反应后,排出多余气体,冷却后称量,固体剩余物质量为ag.
| (1) |
|
若碳酸氢铵和熟石灰以等物质的量混合时,a=________g.
|
|
(2) |
|
若以bmol表示混合物中碳酸氢铵的物质的量,通过计算确定a随b变化的数学表达式.
|
|
|
查看答案和解析>>
科目:
来源:南京市2007届高三质量检测、化学
题型:038
|
|
在某浓度的氯化钡溶液VmL中,加入一定体积、物质的量浓度为0.0500mol/L的稀硫酸时,两者恰好完全反应,此时溶液的pH=3.试求:
| (1) |
|
加入稀硫酸的体积(用含V的数学式表示,两溶液混合时体积变化忽略不计).
|
|
(2) |
|
|
查看答案和解析>>
科目:
来源:龙西北高三年级2007届第一学期调研化学试卷
题型:038
|
|
将51g镁铝合金溶于60mL50mol·L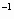 H H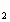 SO SO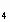 溶液中,完全溶解后再加入65mL10.0mol·L 溶液中,完全溶解后再加入65mL10.0mol·L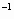 的NaOH溶液,得到沉淀的质量为9.7g,继续滴加NaOH溶液时沉淀会减少. 的NaOH溶液,得到沉淀的质量为9.7g,继续滴加NaOH溶液时沉淀会减少.
| (1) |
|
当加入________mLNaOH溶液时,可使溶液在硫酸中的Mg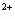 和Al 和Al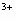 恰好完全沉淀. 恰好完全沉淀.
|
|
(2) |
|
计算合金溶于硫酸时所产生的氢气在标准状况下的休积.
|
|
|
查看答案和解析>>
