
科目: 来源:山东省青州一中2012届高三化学一轮跟踪训练:第8章 第3讲 盐类的水解(鲁科版) 鲁科版 题型:043
在纯碱溶液中滴入酚酞,溶液变红色,若在该溶液中再滴入过量的BaCl2溶液,所观察到的现象是________,其原因是________.
查看答案和解析>>
科目: 来源:山东省青州一中2012届高三化学一轮跟踪训练:第6章第3讲化学能转化为电能——电池(鲁科版) 题型:043
微型纽扣电池在现代生活中有广泛应用,有一种银锌电池,其电极材料分别是Ag2O和Zn,电解质溶液为KOH,总反应为Ag2O+Zn![]() 2Ag+ZnO,试写出该电池的电极反应.
2Ag+ZnO,试写出该电池的电极反应.
查看答案和解析>>
科目: 来源:浙江省杭州十四中2012届高三9月月考化学试题 题型:043
海水中含有多种盐类物质,在一定温度下将海水不断浓缩,其间会不断有晶体析出,且海水的密度逐渐增大,下表为一定温度下不同密度的海水中几种盐类的含量(g/mL)
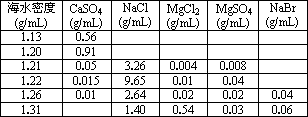
回答下列问题:
(1)在该温度下恒温蒸发海水时,海水的密度从1.13 g/mL增大到1.21 g/mL时是否有硫酸钙析出?
(2)恒温下,当蒸发1 m3密度为1.22 g/mL的海水达到密度为1.26 g/mL时,析出MgSO4的质量为kg,析出NaCl的质量为kg.
查看答案和解析>>
科目: 来源:上海市浦东新区2012届高三4月(二模)质量抽测化学试题 题型:038
防治环境污染是当前环保工作的重要研究内容之一.二氧化硫和氮氧化物是大气的主要污染物.
1.将1.5 mol SO2用氢氧化钠溶液、石灰及氧气处理后,假设硫元素不损失,理论上可得到________g石膏(CaSO4·2H2O).
2.用CH4消除NOx污染的化学方程式为:CH4+4NO→2N2+CO2+2H2O;CH4+2NO2→N2+CO2+2H2O现有11.2 L NO2、NO的混合气体NOx,将其还原为N2,需要4.48 L的CH4,则混合气体中NO2、NO的物质的量分别为________.(体积都已换算为标准状况)
3.(1)常温下用氧缺位铁酸锌ZnFe2Oy可以消除NOx污染,使NOx转变为N2,同时ZnFe2Oy转变为ZnFe2O4.若2 mol ZnFe2Oy与足量NO2可生成0.5 mol N2,则y=________.
(2)氧缺位铁酸锌ZnFe2Oz化学式的氧化物形式为aZnO·bFeO·cFe2O3.已知1 mol ZnFe2Oz最多能使4.0 L(标况)NO1.4转化为N2.则上述氧化物形式的化学式可具体表示为________.
4.低温臭氧氧化脱硫脱硝技术可以同时吸收烟气中的氮氧化物和二氧化硫,反应原理是将NOx氧化成N2O5,通过洗涤形成硝酸盐,二氧化硫形成硫酸盐.其主要反应如下:
NO+O3→NO2+O2 ①
2NO2+O3→N2O5+O2 ②
N2O5+2NH3+H2O→2NH4NO3 ③
SO2+O3+2NH3+H2O→(NH4)2SO4+O2 ④
某热电厂烟气中平均含NOx 4.5‰、SO2 9.0‰(体积分数),压缩空气经臭氧发生器变成臭氧空气,其中O3浓度为90 L/m3,臭氧空气与加湿氨气和烟气混合反应.若![]() 流量比为y,请通过计算列出y与x的关系式.
流量比为y,请通过计算列出y与x的关系式.
查看答案和解析>>
科目: 来源:上海市虹口区2013年高考一模化学试题 题型:038
铁是一种典型的过渡金属,铁和铁的化合物在生产和生活中有广泛的应用.完成下列计算∶
1.将11.802 g钢样粉末(只含铁和碳)于高温下置于足量的纯氧中充分反应,冷却后得到16.240 g磁性氧化铁.
(1)钢样中含铁________g.
(2)生成的CO2在标准状况下体积为________mL.
2.向10 mL氯化铁溶液(含盐酸0.001 mol)中加入16.8 g 5%的烧碱溶液(足量),充分反应后过滤.洗涤沉淀,将洗涤液与滤液合并后稀释至250 mL.取25 mL稀释液,用0.100 mol/L盐酸滴定,终点时消耗盐酸的体积15.50 mL.计算原溶液中Fe3+的物质的量浓度.
3.铁锈的主要成分实为羟基氧化铁[化学式FeO(OH)].将一块带锈铁片放入700 mL pH=0的稀硝酸中充分反应,收集到标准状况下NO气体3.584 L,最终剩余2.020 g铁.求∶
(1)反应后溶液中溶质的成分与物质的量.
(2)原带锈铁片中铁锈的质量分数.
4.用FeSO4和NaOH制备Fe(OH)2时,往往会形成一种灰绿色的中间物(用X表示).经分析,X中含有三种阴离子与两种阳离子,阴、阳离子的总质量之比为11∶12.已知两种阳离子为Fe2+与Fe3+,物质的量之比为2∶1.请通过计算确定X的化学式.
查看答案和解析>>
科目: 来源:上海市长宁区2013年高考一模化学试题 题型:038
钠是活泼的碱金属元素,钠及其化合物在生产和生活中有广泛的应用.完成下列计算∶
1.叠氮化钠(NaN3)受撞击分解产生钠和氮气,故可应用于汽车安全气囊.若78克叠氮化钠完全分解,产生标准状况下氮气________L.
2.钠-钾合金可在核反应堆中用作热交换液.5.05 g钠-钾合金溶于200 mL水生成0.075 mol氢气.计算溶液中氢氧化钠的物质的量浓度(忽略液体体积变化).
3.氢氧化钠溶液处理铝土矿并过滤,得到含铝酸钠的溶液.向该溶液中通入二氧化碳,有下列反应∶2NaAl(OH)4+CO2→2Al(OH)3↓+Na2CO3+H2O
己知通入二氧化碳112 L(标准状况下),生成的Al(OH)3和Na2CO3的物质的量之比为4∶5.若向该溶液中通入的二氧化碳为224 L(标准状况下),计算生成的Al(OH)3和Na2CO3的物质的量的最大值.
4.为测定某硫酸吸收含氨气废气后,所得铵盐中氮元素的质量分数,现将不同质量的铵盐固体分别加入到50.00 mL相同浓度的氢氧化钠溶液中,沸水浴加热至气体全部逸出(此温度下铵盐不分解).该气体经干燥后用浓硫酸吸收完全,测定浓硫酸增加的质量.部分测定结果如下表∶
试回答∶
该铵盐的成分为________.
该铵盐中氮元素的质量分数为∶________(须列式计算)
查看答案和解析>>
科目: 来源:上海市闵行区2013年高考一模化学试题 题型:038
黄铁矿(主要成分为FeS2)是生产硫酸的主要原料.高温时,黄铁矿在空气中煅烧[设空气中V(N2)∶V(O2)=4∶1且不含其他气体],可发生下列反应:
4FeS2+11O2根据题意完成下列计算:
1.若把2.00 g某黄铁矿试样在足量空气中充分灼烧后(杂质不反应、不挥发),得到1.56 g残渣,则该黄铁矿的纯度为________.
2.煅烧70t黄铁矿(含硫35%,杂质不含硫且不反应)生产出72.8t硫酸铵.若黄铁矿制取硫酸时的利用率为80%,则在制取硫酸铵时硫酸的利用率为________(答案保留两位小数).
3.为使FeS2煅烧完全生成Fe2O3,工业上使用过量空气,当空气过量20%时,煅烧后的混合气体平均相对分子质量为________(答案保留两位小数).
4.硫酸工业的尾气可以使用氨水进行吸收,既防止了有害物质的排放,也同时生产副产品氮肥.已知吸收尾气后的氨水全部转化为铵盐.取两份相同体积的铵盐溶液,一份中加入足量硫酸,产生0.09 mol SO2(假设气体已全部逸出,下同);另一份中加入足量Ba(OH)2,产生0.16 mol NH3,同时得到21.86 g沉淀.通过计算,求铵盐溶液中各溶质成分与物质的量浓度之比.
查看答案和解析>>
科目: 来源:上海市黄浦区2013年高考一模化学试题 题型:038
纯碱是主要的化工原料,化学家发明了其不同的工业制法,其中法国化学家尼古拉斯·勒布朗早在1791年发明的工业合成碳酸钠的方法,简称勒布朗制碱法.该方法包括以下两个阶段:首先从原料氯化钠与浓硫酸在高温下的反应得到中间产物硫酸钠,然后通过硫酸钠与木炭和碳酸钙的反应来得到碳酸钠.各步骤反应的化学方程式如下:
①2NaCl+H2SO4![]() Na2SO4+2HCl↑
Na2SO4+2HCl↑
②Na2SO4+2C![]() Na2S+2CO2↑
Na2S+2CO2↑
③Na2S+CaCO3![]() Na2CO3+CaS
Na2CO3+CaS
完成下列计算(计算过程保留3位有效数字)
1.假设每一步反应物的量足够,反应完全,理论上每获得1 kg纯度为80%的纯碱需要氯化钠的的质量是________kg.
2.步骤②碳单质过量时也同样可以反应获得Na2S,此时所发生的反应的化学方程式是________.若其它条件不变,步骤②按此反应进行,每获得1 kg纯度为80%的纯碱需要氯化钠的的质量是________kg,此时消耗碳单质的量
是原步骤②反应用碳量的________倍.
3.通过定性分析,勒布朗制碱法获得的纯碱含有杂质CaCO3和CaS,为了测定产品纯度,取10 g样品与稀硝酸反应,硫元素全部转化成淡黄色固体,称量其质量为0.16 g,另取10 g样品与稀盐酸反应,得到气体(忽略气体在水中的溶解),折算为标况下,体积为2.162 L,计算求出该产品中Na2CO3的纯度.
4.若除氯化钠和碳单质的量外,其它反应物足量,反应充分,如果加入a mol氯化钠时,生成的Na2CO3为yg,电子转移数为z mol,讨论分析当氯化钠与碳的物质的量之比x的值不同时,用函数式表示y和z的值是多少.
查看答案和解析>>
科目: 来源:上海市奉贤区2012届高三4月调研考试(二模)化学试题 题型:038
硫元素价态众多,可与卤素、氮等元素化合形成许多复杂化合物,在科学技术和生成中有重要的应用.根据题意完成下列计算:
1.由硫与限量氯气在50~60℃反应16~20小时,可恰好完全反应,得到两种硫的氯化物A和B.A物质中的含硫量为0.131,B物质中的含氯量为0.816,A的相对分子质量比B大71.计算确定这两种氯化物的分子式分别为________.
若上述反应得到的A、B的物质的量比为3:2,则参加反应的S和氯气的物质的量之比为________.
2.硫的卤化物或卤氧化物都有强水解性,可以作脱水剂.SF4吸收V mL液态水(4℃),完全反应,得到3.2 g SO2气体(假设SO2完全逸出)和10%的酸溶液,计算吸收的液态水的体积V为________mL.
3.S4N4是亮橙色固体,不溶于水和有机溶剂,是一种重要的金属有机化学反应物.一般用S2Cl2、SCl2的惰性溶剂(CS2)氨解制得:
6S2Cl2+16NH3→S4N4+S8+12NH4Cl;
24SCl2+64NH3→4S4N4+S8+48NH4Cl.
S2Cl2、SCl2的混合液体52.86 g溶于足量的CS2中,再通入35.84 L氨气(标准状况)完全氨解,产生14.080 g硫单质.剩余氨气用40 g水完全吸收形成氨水(密度为0.923 g/mL).
计算:①该混合液体中S2Cl2、SCl2的物质的量之比为________.
②所得氨水的物质的量浓度为________(保留1位小数).
4.S4N4与Ag在一定条件下反应,失去N2而缩合成(SN)x,(SN)x合成于1910年,过了五十年,才发现它在0.26 K的低温下,可转变为超导体(superconductor).(SN)x的结构式为:

已知1.20×105 mol S4N4与Ag发生缩合,失去了1.20×105 mol N2,生成二百聚物[(SN)200]和三百聚物.测得缩合产物中二百聚物的质量分数为0.50.
计算:①缩合产物中各缩合物的物质的量.
②若Ag的实际使用量为8.64 kg,求Ag的循环使用次数.
查看答案和解析>>
科目: 来源:上海市嘉定区2013年高考一模化学试题 题型:038
1.NA为阿伏加德罗常数.25℃时,1 g水中含H+离子个数约为________NA.
2.通过氨的催化氧化法制取硝酸,在此全过程中,理论上氨与所耗氧气的物质的量比为________,这样所得硝酸的质量分数为________.
3.往含0.2 mol NaOH和0.1 mol Ca(OH)2的混合溶液中持续稳定地通入CO2气体0.5 mol.请以CO2的量为横坐标,以溶液中离子的总量为横坐标,画出离子总量随CO2加入量变化的折线图.(不计弱电解质的电离和盐的水解)

4、某研究性学习小组拟用铜屑与氧化铜混合物与硫酸和硝酸组成的混酸反应来制取CuSO4·5H2O晶体,混酸中硝酸的还原产物为NO,反应过程中不产生SO2,反应后的溶液中不含Cu(NO3)2,反应中固体完全溶解,两种酸均恰好完全反应.设固体混合物的总质量为480 g,其中铜屑的质量分数为0.4,480 g固体混合物与一定量混酸微热后,充分反应,冷却恰好只得到CuSO4·5H2O,试求原混酸中H2SO4的质量分数(写出计算过程)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com