
科目: 来源:广东省2009届高三化学各地名校月考试题汇编:化学反应速率 题型:058
某化学兴趣小组研究双氧水的分解时,设计了以下三组实验,每一小组取若干支试管分别加入相同体积5%的双氧水,在实验室观察只有极少量的气泡产生.
(1)双氧水发生分解的化学方程式为________.
(2)根据下表中其他实验操作各实验现象填写实验结论:

查看答案和解析>>
科目: 来源:甘肃省兰州一中2009届高三上学期第三次月考化学试题 题型:058
实验室制中备少量硫酸亚铁晶体的实验步骤如下:
取废铁悄放入碳酸钠溶液中加热,用蒸馏水把铁屑冲洗干净,取过量洁净的铁屑,加入20%-30%的稀硫酸溶液,在50℃-80℃水浴中加热仍有少量铁屑.将该溶液趁热过滤,滤液移至试管中,用橡胶塞塞紧试管口,静置,冷却时间后收集产品.
(1)废铁悄放入碳酸钠溶液中加热目的________.
(2)硫酸溶液过稀会导致________.
(3)采用水浴加热的原因是________.温试控制到50℃-80℃原因________.
(4)反应时铁屑过量的目的是(用离子方程式表示)________.
(5)溶液趁热时过滤的原因是________.
(6)静置冷却一段时间后,在试管中观察到的现象是________.
查看答案和解析>>
科目: 来源:甘肃省兰州一中2009届高三上学期第三次月考化学试题 题型:058
某无色溶液,其中有可能存在离子如下:Na+、Ba2+、AlO3+、Al![]() 、S2-、SO
、S2-、SO![]() 、SO
、SO![]() .现取该溶液进行有关实验,实验结果如下图所示.
.现取该溶液进行有关实验,实验结果如下图所示.

请回答下列问题:
(1)沉淀甲是________;
(2)沉淀乙是________由溶液甲生成沉淀乙的离子方程式为:________;
(3)沉淀丙是________;
(4)写出生成甲的离子方程式________
(5)综合上述信息,可以肯定存在的离子________.
查看答案和解析>>
科目: 来源:江西吉安一中2007-2008学年度上学期高三第一次段考化学试卷 题型:058
实验室需用480 mL 1.0 mol/L的NaOH溶液.下图是该学生在实验室配制该NaOH溶液的过程示意图,请据此回答有关问题.

(1)在上述实验过程中,用到的容量的规格是____________.
(2)用已知质量为y g的表面皿,准确称取________________g NaOH固体.
(3)观察配制NaOH溶液的过程示意图,指出其中有错误的是________(填操作序号).在①-⑥中,没有体现出来的一个重要步骤是:_______________________________.
查看答案和解析>>
科目: 来源:江苏省众兴中学2008届高三第三次调研考试、化学 题型:058
用6 mol·L-1硫酸配制100 mL 1.0 mol·L-1酸,若实验仪器有:
(1)实验时应选用仪器的是(填入编号)_________________________.
(2)在容量瓶的使用方法中,下列操作不正确的是(填写号)___________________.
A.使用容量瓶前检查它是否漏水
B.容量瓶用蒸馏水洗净后,再用待配溶液润洗
C.配制溶液时,如果试样是固体,把称好的试样用纸条小心倒入容量瓶中,缓慢加入蒸馏水到接近标线2 cm~3 cm处,用滴管滴加蒸馏水到标线
D.配制溶液时,如果试样是液体,用量筒量取试样后直接倒入容量瓶中,缓慢加入蒸馏水到接近容量瓶刻度标线1 cm~2 cm处,用滴管滴加蒸馏水到刻度线
E.盖好瓶塞,用食指顶住瓶塞,用另一只手的手指托住瓶底,把容量瓶倒转和摇动多次.
(3)怎样检查容量瓶是否漏水_______________________
查看答案和解析>>
科目: 来源:江苏海门市2008届高三第一次诊断性考试试卷、化学 题型:058
海带中含有丰富的碘.为了从海带中提取碘,某研究性学习小组设计并进行了以下实验:
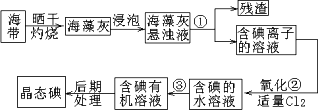
(1)步骤①的实验操作名称是________;
(2)现有烧杯、玻璃棒、集气瓶、酒精灯、导管、圆底烧瓶、石棉网以及必要的夹持仪器、物品.完成该实验尚缺少的玻璃仪器是________;
(3)步骤③中能选用CCl4从碘水中萃取碘的原因是________
A、CCl4与水不互溶
B、CCl4可与I2发生取代反应
C、CCl4的密度比水大
D、CCl4不易燃烧,可作灭火剂
E、碘在CCl4中的溶解度比在水中大很多
(4)步骤②中反应的离子方程式是_______________________;
(5)请设计一种简单的实验方法,检验提取碘后的水溶液中是否还含有单质碘:
_____________________________________________.
查看答案和解析>>
科目: 来源:黑龙江省齐齐哈尔市第八中学2008届高三第二次月考化学试卷 题型:058
有一无色透明溶液,欲确定是否含有下列离子:Na+、Mg2+、Al3+、Fe2+、Ba2+、![]() 、
、![]() 、Cl-、I-、
、Cl-、I-、![]() ,取该溶液实验如下:
,取该溶液实验如下:

(1)溶液中肯定存在的离子是________.
(2)溶液中肯定不存在的离子是________.
(3)为进一步确定其他离子,应该补充的实验是________,________.
查看答案和解析>>
科目: 来源:上海市浦东新区2012届高三4月(二模)质量抽测化学试题 题型:043
铬铁矿的主要成分可表示为FeO·Cr2O3,还含有MgO、Al2O3、Fe2O3等杂质,以下是以铬铁矿为原料制备重铬酸钾(K2Cr2O7)的流程图:
 已知:①4FeO·Cr2O3+8Na2CO3+7O2
已知:①4FeO·Cr2O3+8Na2CO3+7O2②Na2CO3+Al2O3![]() 2NaAlO2+CO2↑;③Cr2O72-+H2O
2NaAlO2+CO2↑;③Cr2O72-+H2O![]() 2CrO42-+2H+
2CrO42-+2H+
根据题意回答下列问题:
1.固体X中主要含有________(填写化学式);要检测酸化操作中溶液的pH是否等于4.5,应该使用________(填写仪器或试剂名称).
2.酸化步骤用醋酸调节溶液pH<5,其目的是________.
3.操作Ⅲ有多步组成,获得K2Cr2O7晶体的操作依次是:加入KCl固体、蒸发浓缩、________、过滤、________、干燥.
4.下表是相关物质的溶解度数据,操作Ⅲ发生反应的化学方程式是:Na2Cr2O7+2KCl→K2Cr2O7↓+2NaCl.
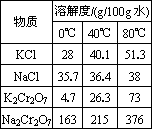
该反应在溶液中能发生的理由是________.
5.副产品Y主要含氢氧化铝,还含少量镁、铁的难溶化合物及可溶性杂质,精确分析Y中氢氧化铝含量的方法是称取n g样品,加入过量________(填写试剂)、溶解、过滤、再________(填写试剂)、……灼烧、冷却、称量,得干燥固体m g .计算样品中氢氧化铝的质量分数为________(用含m、n的代数式表示).
6.六价铬有毒,而Cr3+相对安全.工业含铬(CrO3)废渣无害化处理的方法之一是干法解毒,用煤不完全燃烧生成的CO还原CrO3.在实验室中模拟这一过程的装置如下:
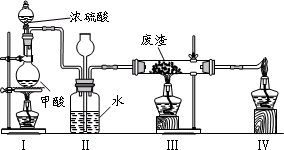
CO由甲酸脱水制得;实验结束时熄灭酒精灯的顺序是________.
查看答案和解析>>
科目: 来源:上海市虹口区2013年高考一模化学试题 题型:043
钯催化偶联反应可表示为∶R-X+CH2=CH-R’![]() R-CH=CH-
R-CH=CH-![]() +HX.美国化学家Richard F.Heck因研究此反应获2010年诺贝尔化学奖.以下是利用钯催化偶联反应合成一种香料A(
+HX.美国化学家Richard F.Heck因研究此反应获2010年诺贝尔化学奖.以下是利用钯催化偶联反应合成一种香料A(![]() )的流程∶
)的流程∶
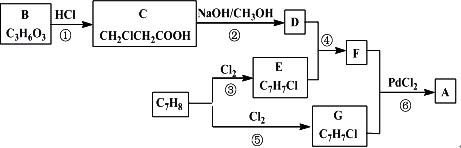
完成下列填空∶
1.写出结构简式.B________E________
2.写出反应②的化学方程式.
3.反应④属于________(填反应类型).反应⑤的条件是________.
4.为了促进反应⑥的进行,通常可以加入一种显________的物质.
a.强酸性
b.弱酸性
c.弱碱性
d.强碱性
5.写出A的两种符合下列条件的同分异构体的结构简式________、________.
ⅰ.含有两个苯环(除苯环外不含其它环状结构);
ⅱ.只存在四种化学环境不同的氢原子.
6.仅以B为有机原料,任选无机试剂,经过三步反应可得到一种含有六元环的酯.写出相关反应的化学方程式.
查看答案和解析>>
科目: 来源:上海市虹口区2013年高考一模化学试题 题型:043
精制氯化钾在工业上可用于制备各种含钾的化合物.完成下列填空∶
1.工业氯化钾中含有Fe3+、SO42-、Br-等杂质离子,可按如下步骤进行精制,完成各步内容.
①溶解;②加入试剂至Fe3+、SO42-沉淀完全,煮沸;③________;④加入盐酸调节pH;⑤________(除Br-);⑥蒸干灼烧.
步骤②中,依次加入的沉淀剂是NH3·H2O、________、________.
证明Fe3+已沉淀完全的操作是________.
2.有人尝试用工业制纯碱原理来制备K2CO3.他向饱和KCl溶液中依次通入足量的________和________两种气体,充分反应后有白色晶体析出.将得到的白色晶体洗涤后灼烧,结果无任何固体残留,且产生的气体能使澄清石灰水变浑浊.写出生成白色晶体的化学方程式∶________.分析该方法得不到K2CO3的原因可能是________.
3.用氯化钾制备氢氧化钾的常用方法是离子交换膜电解法.氢氧化钾在________极区产生.为了避免两极产物间发生副反应,位于电解槽中间的离子交换膜应阻止________(填“阴”、“阳”或“所有”)离子通过.
4.科学家最近开发了一种用氯化钾制氢氧化钾的方法.其反应可分为5步(若干步已合并,条件均省略).请写出第⑤步反应的化学方程式.
第①、②步(合并)∶2KCl+4HNO3→2KNO3+Cl2+2NO2+2H2O
第③、④步(合并)∶4KNO3+2H2O→4KOH+4NO2+O2
第⑤步∶________
总反应∶4KCl+O2+2H2O→4KOH+2Cl2
与电解法相比,该方法的优势可能是________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com