
科目: 来源:灌云县2006-2007学年高三第一次联考、化学试卷 题型:058
| |||||||||||||||||||
查看答案和解析>>
科目: 来源:高州中学2007届高三化学十月份月考 新人教 新人教 题型:058
某实验小组欲制取氧化铜并证明氧化铜能加快氯酸钾的分解,进行了如下实验:
(一)制取氧化铜
①称取2gCuSO4·5H2O研细后倒入烧杯,加10mL蒸馏水溶解;
②向上述CuSO4溶液中逐滴加入NaOH溶液,直到不再产生沉淀,然后将所得混合物转移到蒸发皿,加热至沉淀全部变为黑色;
③将步骤②所得混合物过滤、洗涤,晾干后研细备用.
回答下列问题:
(1)上述实验步骤中需要使用玻璃棒的是________(填实验序号),步骤①、③中研磨固体所用仪器的名称是________;
(2)步骤③中洗涤沉淀的操作是________
(二)证明氧化铜能加快氯酸钾的分解并与二氧化锰的催化效果进行比较
用右图装置进行实验,实验时均以生成25mL气体为准,其它可能影响实验的因素均已忽略,相关数据见下表:
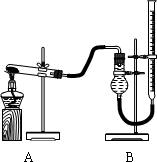
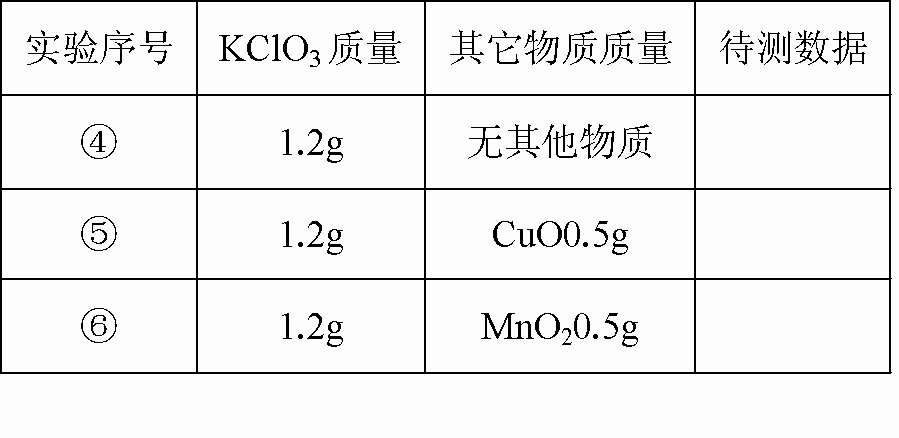
回答下列问题:
⑶上述实验中的“待测数据”指________;
⑷本实验装置图中量气装置B由干燥管、乳胶管和50mL滴定管改造后组装而成,此处所用滴定管是________(填“酸式”或“碱式”)滴定管;
⑸若要证明实验⑤中干燥管内收集的气体是O2,可待气体收集结束后,用弹簧夹夹住B中乳胶管,拔去干燥管上单孔橡皮塞,________;
⑹为探究CuO在实验⑤中是否起催化作用,需补做如下实验(无需写出具体操作):a、________,b、________.
查看答案和解析>>
科目: 来源:高州中学2007届高三化学十月份月考 新人教 新人教 题型:058
| |||||||||||||||
查看答案和解析>>
科目: 来源:飞龙中学高2007级应届班第二次月考试卷、化学试题(人教版) 人教版 题型:058
| |||||||||||||||||||
查看答案和解析>>
科目: 来源:潮阳一中2007届高三化学第一次月考新课标(人教) 人教版 新课标 题型:058
| |||||||||||||||||||
查看答案和解析>>
科目: 来源:潮阳一中2007届高三化学第一次月考新课标(人教) 人教版 新课标 题型:058
| |||||||||||||||||||||||
查看答案和解析>>
科目: 来源:潮阳一中2007届高三化学第一次月考新课标(人教) 人教版 新课标 题型:058
| |||||||||||
查看答案和解析>>
科目: 来源:潮阳一中2007届高三化学第二次月考(人教) 人教 题型:058
在长期载人太空飞行的宇航器中,每个宇航员平均每天需要消耗0.9kg氧气,呼出1.0kg的二氧化碳。为了能保持飞船座舱内空气成分的稳定,宇航科学家进行了大量的科学探索。方法一:有的科学家提出“金属过氧化物处理系统”,即不断的将座舱内的空气通过盛有金属过氧化物(以过氧化钠为例)的容器,并把处理后的气体充入座舱。有关反应的化学方程式为:①________②________;将处理后的气体充入座舱时,应注意采取的一项措施是________
方法二:有的科学家根据电解原理设计了飞船内空气更新实验系统,该系统结构示意图如下:

(1)管道①把飞船座舱内含有较多二氧化碳的潮湿的空气通入“电化学二氧化碳处理系统”的N极室,通过该电极反应可以使二氧化碳不断被吸收;该电极反应式为________
其电解产物吸收二氧化碳的离子反应方程式为________。在N极吸收二氧化碳后形成的离子会通过隔膜进入M极室,通过M极的电极反应可以使二氧化碳从电解液中释放出来,并保持系统的pH不变;该电极反应式为________、________。
(2)管道②是将处理后的空气混入“电解水系统”产生的新鲜氧气,然后通入飞船座舱内供宇航员呼吸用。在“电解水系统”中Y为________极(填“阴”或“阳”)X极的电极反应为________
(3)逸出的二氧化碳没有排出飞船外,而是通过管道③进入“二氧化碳还原系统”。在该系统内,二氧化碳跟氢气在一定条件下反应,其产物中有甲烷等气体,请评价这种处理的意义________
查看答案和解析>>
科目: 来源:潮阳一中2007届高三化学第二次月考(人教) 人教 题型:058
新装修的居室内,甲醛浓度往往很大.严重污染空气.居住者接触时间较长易得白血病。1×10—5mol·L—1的紫色KMnO4溶液遇甲醛气体即褪色,用下面的微型化学实验可测定室内空气甲醛含量:
(1)试设计实验,配制得到100mLl.00×10-4mol·L-1KMnO4溶液;(注意:浓度极小,不宜一次性配制)
(2)用2.5mL注射器准确量取2mLl.00×10—4mol·L—1KMnO4溶液,注入六孔穴板1*孔内,加入3滴6mol·L—1H2SO4溶液,盖好塞子;按图连接好装置。将此装置置于待测地点,缓慢抽气,每次抽气50mL,直到溶液红色褪去,记录抽气次数。写出甲醛与酸性KMnO4溶液反应的化学方程式。
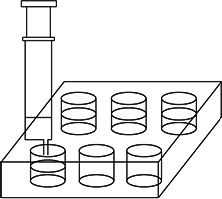
(3)设抽气次数为n,试计算甲醛在空气中的含量(mg/m3)。________
(4)若室内空气中甲醛气体最高允许浓度为20mg·m-3试析讨论室内空气符合标准时n的取值范围。________
(5)为保证实验结果精确性,实验过程中应注意什么?
查看答案和解析>>
科目: 来源:滨海县07届高三第三次月考试卷、化学试题 题型:058
| |||||||||
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com