
科目: 来源:连州中学2007届高三化学第十四周周考 题型:058
| |||||||||||||||
查看答案和解析>>
科目: 来源:连州中学2007届高三第三次月考、化学试卷 题型:058
| |||||||||||||||
查看答案和解析>>
科目: 来源:连州中学2007届高三第三次月考、化学试卷 题型:058
| |||||||||||
查看答案和解析>>
科目: 来源:连州中学2007届高三第二次月考、化学试卷 题型:058
某研究性学习小组在整理实验室化学试剂时,发现一盛有无色溶液的试剂瓶,标签破损,如右图.某同学根据中学化学知识,对该试剂可能是什么物质的溶液进行了如下猜想和验证,选择你认为完全正确(包括猜想物质的化学式、检验需要的试剂、操作、现象及结论)的选项________(多选倒扣分).
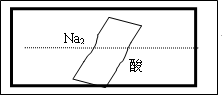
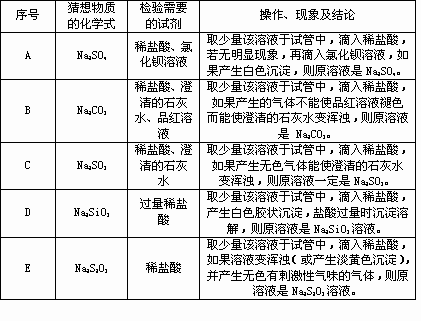
除上述五种可能之外,写出你认为还有可能物质的化学式(1种):________.
查看答案和解析>>
科目: 来源:连州中学2007届高三第二次月考、化学试卷 题型:058
| |||||||||||||||||||
查看答案和解析>>
科目: 来源:旧版邵东一中2007届高三第五次月考化学试题 题型:058
| |||||||||||||||||||||||
查看答案和解析>>
科目: 来源:揭东一中2007届高三级第一次月考化学试题 题型:058
| |||||||||||||||||||||||||||
查看答案和解析>>
科目: 来源:江西省(南昌一中、十中、新建二中)2006-2007学年度高三年级第一学期三校联考、化学试题 题型:058
二氯化硫(SCl2)熔点-78℃,沸点59℃.密度1.638g/L.遇水易分解.二氯化硫与三氧化硫作用可生成重要化工试剂亚硫酰氯(SOCl2).以下是由氯气与硫反应合成二氯化硫的实验装置.
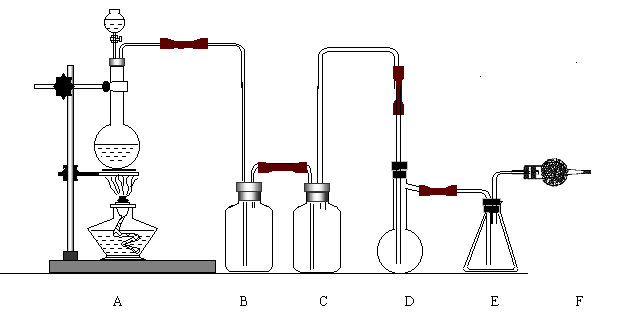
试回答下列问题:
①装置A中发生反应的化学方程式为:________.
②装置B盛放的药品是________C中是________.
③实验开始前先在D中放入一定量的硫粉,加热使硫熔化,然后转动和摇动烧瓶使硫附着在烧瓶内壁形成一薄层表面,这样做的目的是________.
④实验时,D装置需加热至50-59oC,最好采用何种方式加热________.如何防止E中液体挥发________.
⑤F装置中干燥管内所盛物质是________作用是:________.
⑥由二氯化硫与SO3作用生成亚硫酰氯的化学方程式为:________.
查看答案和解析>>
科目: 来源:江西省(南昌一中、十中、新建二中)2006-2007学年度高三年级第一学期三校联考、化学试题 题型:058
下列实验操作或对实验事实的描述不正确的是________(填序号,错选一个倒扣1分,不出现负分)
①用量筒量得稀硫酸溶液8.0mL;②浓硫酸不小心沾在皮肤上,应立即用大量的水冲洗;③用热的浓HCl洗涤附着有MnO2的试管;④在硫酸铜晶体结晶水含量的测定中,若加热后的无水硫酸铜粉末表面发黑,则所测结晶水含量可能会偏高;⑤Fe(OH)3胶体与FeCl3溶液可用过滤的方法分离;⑥用碱式滴定管量得KMnO4溶液20.50mL;⑦实验室快速制备少量H2、O2、NH3、HCl可以用同一种气体发生装置;⑧配制一定浓度的溶液时,若定容时不小心加水超过容量瓶的刻度线,应立即用滴管吸去多余的部分.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com