
科目: 来源:黑龙江省齐齐哈尔市第八中学2008届高三第二次月考化学试卷 题型:058
某研究性学习小组的一个课题是“NO2能否支持木条的燃烧?”由于实验室中没有现成的NO2气体,该小组的同学设计了两个方案(忽略N2O4的存在,图中铁架台等夹持仪器均已略去):
Ⅰ.实验装置如下图1所示

(1)浓硝酸受热分解的化学方程式是________________.
(2)实验开始后木条上的火星逐渐熄灭,有的同学得出“NO2不能支持木条的燃烧”的结论.你认为这一结论是否正确?________(填“正确”或“不正确),理由是________.
Ⅱ.实验装置如图2所示
(1)硝酸铜固体加热分解的产物有氧化铜、二氧化氮和氧气,该反应的化学方程式是________.
(2)当集气瓶中充满红棕色气体时,木条复燃了,有的同学得出“NO2能支持木条的燃烧”的结论.你认为这一结论是否正确?________(填“正确”或“不正确”),理由是________________________.
Ⅲ.为了更直接说明“NO2能否支持木条的燃烧”这一问题,请你重新设计一个简单的实验方案,简述实验原理和主要操作.________________.
查看答案和解析>>
科目: 来源:哈尔滨市第三中学2007-2008学年度高三9月份月考化学试卷 题型:058
| |||||||||||||||||||
查看答案和解析>>
科目: 来源:2008年高考化学第一轮复习练习题二——《碱金属》 题型:058
工业制纯碱时,第一步通过饱和食盐水、氨和二氧化碳反应,获得大酸氢钠晶体,它的反应原理可以用下面的方程式表示:NH3+CO2+H2O=NH4HCO3,NH4HCO3+NaCl(饱和)=NaHCO3↓+NH4Cl.以上反应的总结果是放热反应.请设计一个实验:用最简单的实验装置模拟实现这一过程,获得碳酸氢钠晶体.可供选择的实验用品有:6 mol/L的盐酸、6 mol/L的硫酸、浓氨水、氢氧化钠、消石灰、石灰石、氯化氨、食盐蒸馏水和冰,以及中学化学实验常用仪器.
(1)画出实验装置示意图(包括反应时容器中的物质),并在图中玻璃容器旁自左至右分别用A,B,C符号标明(请见题后说明).
(2)请写出上图中A,B,C各玻璃容器中盛放物质的化学式或名称.
(3)利用在本题所提供的实验用品,如何判断得到的产品是碳酸钠的结晶,而不是碳酸氢氨或食盐结晶.
说明:①本题装置示意图中的仪器可以用下面的方式表示.

②铁架台、石棉网、酒精灯、玻璃导管之间的连接胶管等,在示意图中不必画出,如需要加热,在需要加热的仪器下方,标以“Δ”表示.
查看答案和解析>>
科目: 来源:2008年高考化学第一轮复习练习题二——《碱金属》 题型:058
某样品为Na2C03和NaHCO3的固体混合物.拟将一定质量的样品与稀硫酸反应,用测出生成CO2体积的方法计算出样品中组分的质量分数.为较准确的测出生成的CO2体积,在反应结束后加热混合液,使溶于溶液的CO2逸出,待冷却后再测CO2的体积(加热时蒸发的水的体积不计).下图是实验装置,其中包括B和C可供选择(B,C中所盛的液体为饱和NaHCO3溶液).

(1)用托盘天平称取样品w(g),若所用天平游码的最大刻度为5 g,则与此天平配套的砝码中最小的质量是________.
A.1 g B.2 g C.3 g D.5 g E.10 g
(2)对A进行气体气密性检查的最简单方法是________________________.
(3)已知所用硫酸的浓度为0.5 mol/L,A中试管的规格是20 nm(内径)×200 nm(高度),则在称此样品时,W的值应不大于________g,测定气体的体积所用量筒的规格,合适的是________.
A.100 mL B.200 mL C.500 mL
(4)测量CO2气体的体积时,可选用B,C中的一种与A连接,你将选择________(填B或C),不选另一种的理由是________.
查看答案和解析>>
科目: 来源:2008年普通高等学校招生全国统一考试(天津卷)、理综化学部分及答案 题型:058
化学实验室制取氯化氢气体的方法之一是将浓硫酸滴入浓盐酸中.请从下图中挑选所需仪器,在方框内画出用该方法制备、收集干燥氯化氢气体的装置简图,并在图中标明所用试剂.(仪器可重复使用,固定装置不必画出)
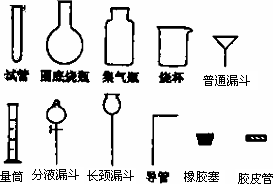
查看答案和解析>>
科目: 来源:连州中学2008届高三化学第二轮复习实验题训练 题型:058
已知当溶液的pH在10左右时,铝元素主要以Al(OH)3形式存在.如果饮用水中含有一定浓度的NO3-将对人体健康产生危害,NO3-能氧化人体血红蛋白中的Fe(Ⅱ)使其失去携氧功能:NO3-还能被水中还原性物质还原成具有强烈致癌作用的NO2-.为此世界卫生组织规定饮用水中NO3-含量(以N计)必须小于10 mg·L-1.为降低饮用水中NO3-的浓度,某研究人员提出以下3种方案:
a.微碱性条件下用Fe2+还原,还原产物为NH3.
b.pH=10.25时,用铝粉还原,NO3-的还原产物主要为N2.
c.在催化剂作用下用氢气还原,还原产物主要为N2.
(1)a方案中的一种产物还有净水作用,这种物质是________.(请填写化学式)
(2)b方案中最好用________调节pH.
A.NaOH B.CaO C.NH3 D.H2O
理由是___________________________________________.
(3)与a、b方案相比,c方案的优点是)___________________________________
查看答案和解析>>
科目: 来源:广东省惠州市第八中学2008届高三化学模拟试题(8) 题型:058
实验室有CuO和Cu粉的混合物.请你利用给出的实验仪器及试剂,设计两种测定该样品(已称得其质量为m克)中氧化铜质量分数的方法,并填写表格中的有关内容.

实验可能用到的主要仪器:
①托盘天平 ②启普发生器 ⑧硬质玻璃管 ④泥三角 ⑤烧杯 ⑥坩埚 ⑦酒精灯 ⑧玻棒 ⑨漏斗 ⑩干燥管
实验可能用到的试剂:
a.锌粒 b.稀硫酸 c.氯化钠溶液 d,浓硫酸
查看答案和解析>>
科目: 来源:广东华附2008届高三5月月考化学试卷 题型:058
为除去粗盐中的Ca2+、Mg2+、Fe3+、SO42-以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):
称取粗盐![]()
![]()
![]()
![]()
![]() 滤液
滤液
![]()
![]() 精盐
精盐
(1)判断BaCl2已过量的方法是________.
(2)第④步中,相关的离子方程式是________.
(3)若先用盐酸调pH值再过滤,将对实验结果产生影响,其原因是________.
(4)为检验精盐纯度,需配制150 mL 0.2 mol/LNaCl(精盐)溶液,如图是该同学转移溶液的示意图,图中的错误是___________________________________________.

查看答案和解析>>
科目: 来源:潮州市2008年高考第二次模拟测试、化学试题 题型:058
在实验室里可用下图所示装置制取KClO3、NaClO.
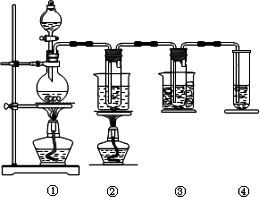
②的试管里盛有15 mL 30%KOH溶液,并置于热水浴中;发生反应生成KClO3.
③的试管里盛有15 mL 8%NaOH溶液,并置于冰水浴中.
请填写下列空白:
(1)制取氯气时,在烧瓶里加入一定量的二氧化锰,通过分液漏斗向烧瓶中加入适量的浓盐酸.实验时为了除去氯气中的氯化氢气体,可在①与②之间安装盛有________(填写化学试剂名称)的净化装置;④中装的试剂是________.
(2)比较制取氯酸钾和次氯酸钠的条件,二者的差异是:_____________.③的试管中反应的离子方程式为________________.
查看答案和解析>>
科目: 来源:2008年中山纪念中学5月份化学模拟试题 题型:058
最近,我国利用生产磷铵排放的废渣磷石膏制取硫酸并联产水泥的技术研究获得成功.具体生产流程如下:
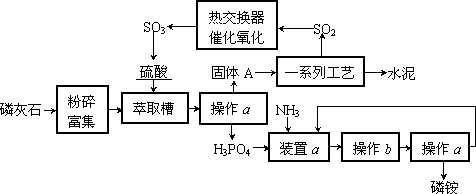
回答下列问题:
(1)若操作a、操作b均在实验室进行,则操作a时用到的玻璃仪器有________;进行操作b时需注意________________.
(2)装置a用于磷酸吸收NH3.若该过程在实验室中进行,请在答题卡的方框内画出装置a的示意图.
(3)热交换器是实现冷热交换的装置.化学实验中也经常利用热交换来实现某种实验目的,如气、液热交换时通常使用的仪器是________.
(4)固体A为生石膏(CaSO4·2H2O)和不含结晶水且高温时也不分解的杂质.生石膏在120℃时失水生成熟石膏(2CaSO4·H2O),熟石膏在200℃时失水生成硫酸钙.为测定固体A中生石膏的含量,某科研小组进行了如下实验:称取固体A 180 g置于坩埚中加热,加热过程中固体质量随温度变化记录如下图:
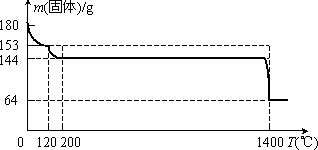
实验中每次对固体称量时须在冷却后进行.为保证实验结果的精确性,固体冷却时必须防止________.
将加热到1400℃时生成的气体通入品红溶液中,品红褪色.写出1400℃时的化学反应方程式________________.
③固体A中生石膏的质量分数=________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com